
作者:Mohamed A. Ellabban,1,2 Moustafa Elmasry,1 Islam Abdelrahman,1 Ghada Abdel Kader,3 Ingrid Steinvall,1 Folke Sjoberg,1 Amr A. Gomaa,2 and Islam Omar Abdel Fattah3
1Department of Hand Surgery, Plastic Surgery and Burns and Department of Biomedical and Clinical Sciences, Linköping University, 58183 Linköping, Sweden
2Plastic and Reconstructive Surgery Unit, Department of Surgery, Suez Canal University, Ismailia, 41522 Egypt
3Department of Human Anatomy and Embryology, Faculty of Medicine, Suez Canal University, Ismailia, 41522 Egypt
Mohamed A. Ellabban,
摘要
硝酸甘油、肉毒杆菌毒素A(BoTA)和氯吡格雷等多种药物可以改善皮瓣缺血和静脉充血损伤,从而达到有益的效果。80只大鼠遭受动脉缺血或静脉充血,并应用于双蒂U形上腹部浅下动脉(SIEA)皮瓣,同时给予硝酸甘油、BoTA或氯吡格雷治疗。7天后,处死所有大鼠进行皮瓣评估。与缺血性皮瓣(34.78%)相比,氯吡格雷治疗的皮瓣坏死面积百分比显著降低(24.49%);而硝酸甘油(19.22%)与静脉充血的皮瓣(43.26%)比较。缺血时,光镜和电镜评估显示,硝酸甘油导致角质形成细胞变性和胶原纤维紊乱。同时,服用氯吡格雷后,这些结构的完整性得到了改善。对于静脉充血,硝酸甘油和BoTA治疗减轻了表皮和真皮损伤;氯吡格雷引起凝固性坏死。使用BoTA和氯吡格雷的缺血性皮瓣中组织基因表达和血清血管内皮生长因子(VEGF)水平显著增加,静脉充血的皮瓣中使用硝酸甘油和BoTA氯吡格雷。在缺血和静脉充血的皮瓣中,3种治疗剂均可上调肿瘤坏死因子-α(TNF-α)的基因表达水平。在所有治疗方式中,其血清水平在静脉充血的皮瓣中显著升高,在缺血性皮瓣中显著降低。我们的分析表明,缺血性皮瓣的最佳治疗方案是氯吡格雷,而静脉充血的皮瓣则是硝酸甘油和BoTA。
学科名称:细胞生物学,药物发现,生物标志物,分子医学
首选
介绍
筋膜皮瓣通常用于创伤和肿瘤切除后组织缺损的功能恢复1。然而,导致覆盖缺陷的并发症,如皮瓣缺血和充血,可能是一种风险2。在动物研究中,大鼠皮瓣模型已被用于确定皮瓣存活因素,并测试可以改善其的治疗方案。随机模式皮瓣比轴向模式皮瓣更频繁地使用3。
2017年,Matsomouto等人3介绍了一种基于双侧上腹部浅下动脉(SIEA)和静脉(SIEV)的新型倒U型腹部筋膜皮瓣模型。两个SIEA中的一个的结扎将产生皮瓣缺血模型,两个SIEV中的两个将产生皮瓣充血模型。他们在新模型中显示出一致的皮瓣存活率,可用于评估各种制剂对皮瓣存活率的影响。
先前的研究表明,使用不同的药物制剂可以提高皮瓣对缺血和充血的耐受性。多种药物已被证明通过抑制炎症、清除自由基、改善血管生成和/或增加微血管网络,有利于提高皮瓣存活率。理想的治疗剂应有效且易于使用,发病率低,成本效益高。
众所周知,硝酸甘油软膏具有强大的局部血管舒张作用,并增加局部血流量,这可能会提高皮瓣的存活率,尽管它并不普遍用于预防皮瓣坏死,可能是由于一些研究中缺乏效果。然而,其他人在人类和动物的皮瓣存活方面都显示出了令人满意的结果。最近的研究表明肉毒杆菌毒素a(BoTA)对皮肤和肌肉皮瓣的存活有良好的效果。这种效果主要是由于血管扩张和皮瓣血液灌注增加,尤其是在血管周围注射时。其血管舒张作用已经通过自主神经阻滞被提出,从而增加到皮瓣组织的血流量。
另一种疗效良好的药物是口服氯吡格雷,这是一种强效抗血小板药物,可减少血小板活化和聚集。研究表明,抑制血小板聚集可能是减少皮瓣坏死的有效策略。此外,它还具有血管舒张作用。
本研究的目的是比较硝酸甘油、BoTA和氯吡格雷对反向U形双蒂SIEA皮瓣缺血和充血模型的有效性。
材料和方法
动物
在这项实验研究中,我们纳入了80只年龄在12至16周之间的雄性Sprague-Dawley大鼠,平均体重为210 ± 30g。将大鼠分组在单独的笼子中,置于通风良好的房间中,进行12小时的黑暗/光照循环,并随意使用自来水和啮齿动物颗粒。此外,在进行任何手术之前,将其放置2周的适应期。对动物进行温和处理,每天检查是否有任何不适或感染。所有手术都是在完全麻醉下进行的,术后服用镇痛药和抗生素。此外,还尽一切努力尽量减少动物的痛苦。
实验设计
将大鼠随机分为两个主要组之一,诱导皮瓣缺血组或诱导皮瓣静脉充血组(每组40只大鼠)。然后将每个主要组进一步随机分为四个亚组(每个亚组10只大鼠);对照组、硝酸甘油软膏治疗组、博达注射液治疗组、口服氯吡格雷治疗组。
外科手术
手术当天,通过腹膜内注射氯胺酮盐酸盐(Ketamax®,Troikaa,Gujarat,India)(50 mg/kg)和甲苯噻嗪(Xylajet®,ADWIA,Egypt)(10 mg/kg)18麻醉大鼠。在确认深度麻醉迹象后,将大鼠置于仰卧位。剃掉腹部的毛发,然后用聚维酮碘溶液清洗皮肤。
使用1cm宽的反向U形透明模板来标记未来解剖的皮瓣的轮廓。倒U型的顶部位于剑突和耻骨中间的中线处。此外,倒U型两端位于耻骨水平。然后抬高具有脂膜的皮肤,保留两侧供应的浅表下上腹部血管(图1A–C)。保留右侧的SIEA和SIEV作为椎弓根。在解剖显微镜(Olympus®,Tokyo,Japan)下,解剖SIEA并用不可吸收材料结扎,而缺血组的SIEV保持完整。在静脉充血组中,仅切开并结扎左侧SIEV,而保留完整的SIEA。最后,将皮瓣重新定位,并用4–0种不可吸收缝合材料缝合(图1D)3。
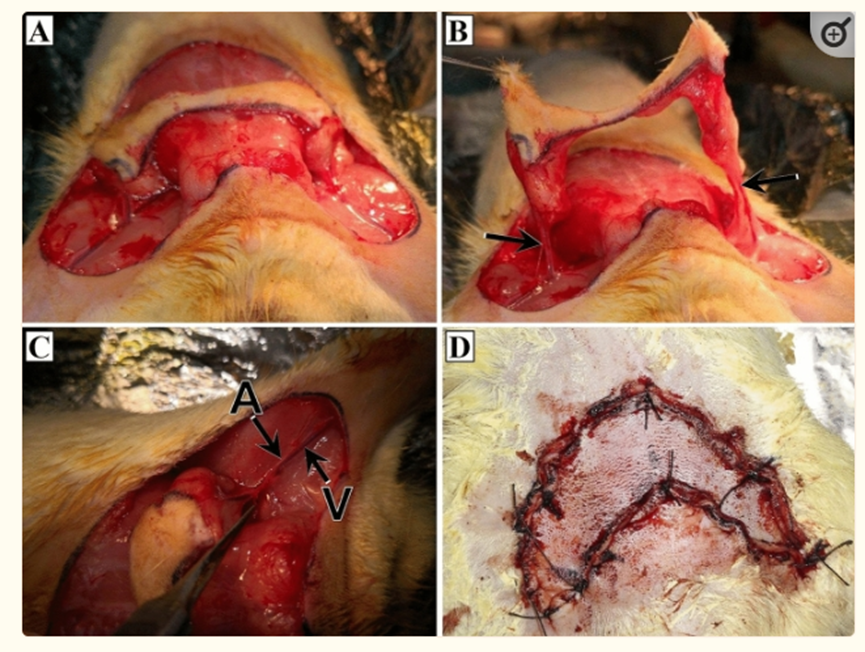
图1手术程序。(A) 切开后立即进行皮瓣移植。(B) 隆起的皮肤,其脂膜保留两侧供应的浅表下上腹部血管(箭头)。(C) 结扎前的左上腹部下浅动脉(A)和静脉(V)。(D) 用不可吸收缝合材料缝合后重新定位皮瓣。
治疗剂的给药
将2%硝酸甘油软膏(Nitro Bid®,Fougera,Altana Co.,Melville,NY,USA)直接局部涂抹在皮瓣区域的皮肤上,从手术当天到第719天处死,每8小时形成一层可见层。BoTA(肉毒杆菌素®,Allergan股份有限公司,加利福尼亚州欧文市,美国)2 IU(1 ml)一次直接注射到左腹浅下血管周围的软组织中,在皮瓣的左蒂处产生肿胀20。将75 mg硫酸氢氯吡格雷(Plavix®,赛诺菲-安万特,法国)片剂压碎并溶解在蒸馏水中,并在手术后立即开始口服灌胃给药,剂量为25 mg/kg/天21。
皮瓣存活评估
在手术当天(第1天)、第3天和第7天,用数码相机(Nikon®,Tokyo,Japan)拍摄所有大鼠的皮瓣。对照片进行了可见坏死迹象的评估。使用ImageJ®软件计算坏死和完整部分的表面积,并以cm2表示。皮瓣坏死面积的百分比计算为受影响的皮肤面积/皮瓣总面积 × 100.
组织病理学评估
第7天,所有大鼠均通过过量氯胺酮和甲苯噻嗪实施安乐死。在病理学研究中,切除皮瓣,并使用4%多聚甲醛固定健康和坏死区域之间过渡区的组织标本。在石蜡块中包埋后,用苏木精和伊红(H&E)22对4μm厚的切片进行染色。
透射电子显微镜
直径为1mm3的皮肤标本在2.5%戊二醛中固定2小时,然后用1%四氧化锇后固定1小时。使用分级浓度的酒精对标本进行脱水,然后将其包埋在树脂中。制备经甲苯胺蓝染色的半薄切片,在光学显微镜(Olympus®,Tokyo,Japan)下放大倍数为 × 1000来检测通过透射电子显微镜(TEM)检查的区域。切割超薄切片并用乙酸铀酰和柠檬酸铅双重染色,以在埃及开罗爱资哈尔大学电子显微镜单元使用TEM(JOEL®,Columbia,South Carolina,USA)进行检查23。
实时逆转录聚合酶链式反应
采用实时逆转录聚合酶链式反应(RT-PCR)检测皮瓣组织中血管内皮生长因子(VEGF)和肿瘤坏死因子-α(TNF-α)的mRNA表达。组织样品在−80°C下冷冻保存,直至RT-PCR分析。按照制造商的说明,使用TRIZOL试剂(上海裕盛生物技术有限公司,有限公司)从每个活检样本中提取RNA。使用SYBR PrimeScript RT-PCR试剂盒(Invitrogen,Carlsbad,CA,USA),按照制造商的方案,使用3-磷酸脱氢酶甘油作为内部对照,使用定量RT-PCR评估VEGF和TNF-α的表达。所用引物如下:
使用2-ΔΔCT方法分析相对mRNA表达20。
酶联免疫吸附测定
酶联免疫吸附试验(ELISA)用于评估血清VEGF和TNF-α水平。大鼠禁食过夜,处死后立即采集腹主动脉的血液样本,并放置直至凝固。通过在4°C24下以3000rpm离心15分钟来分离血清。根据制造商的说明,使用VEGF和TNF-α特异性试剂盒(R&D Systems,MN,USA)测量其水平。
统计分析
使用社会科学统计软件包(SPSS)第24版(SPSS®,美国芝加哥)进行统计分析。定量值以平均值(95%置信区间)表示。方差分析(ANOVA)和Tukey的事后检验用于比较研究组。小于的概率 0.05被认为是显著的。
道德声明
作者声明,本研究是根据ARRIVE指南进行报告的。动物的处理和护理是根据1986年英国动物(科学程序)法和相关指南,欧盟动物实验指令2010/63/EU进行的。该方案由苏伊士运河大学医学院研究伦理委员会批准(批准号:4488#)。
首选
后果
皮瓣坏死面积百分比
在诱导的皮瓣缺血亚组中,与对照、硝酸甘油和BoTA亚组相比,氯吡格雷亚组在第7天的坏死面积百分比显著降低(p < 0.001)。另一方面,与对照组相比,硝酸甘油亚组在第7天的坏死面积百分比显著增加(p < 0.001)(图2和表表11)。
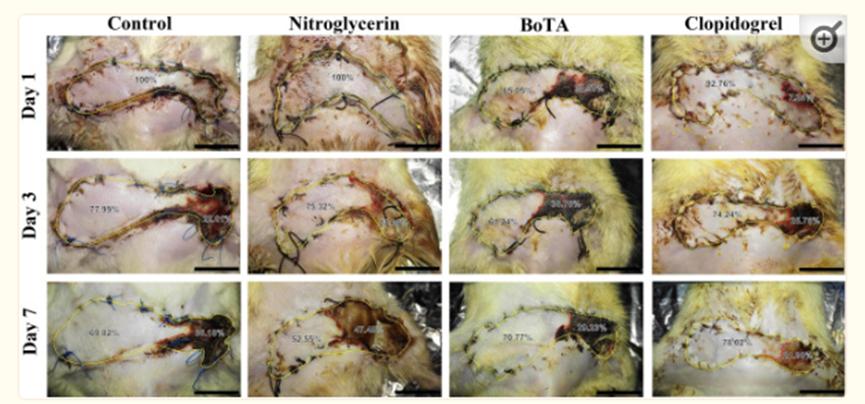
图2:术后第1、3和7天诱导皮瓣缺血亚组的皮瓣大体外观。黄色虚线勾勒出皮瓣总面积,红色虚线表示正常组织和坏死组织之间的分界。(比例尺 = 1.5厘米)。
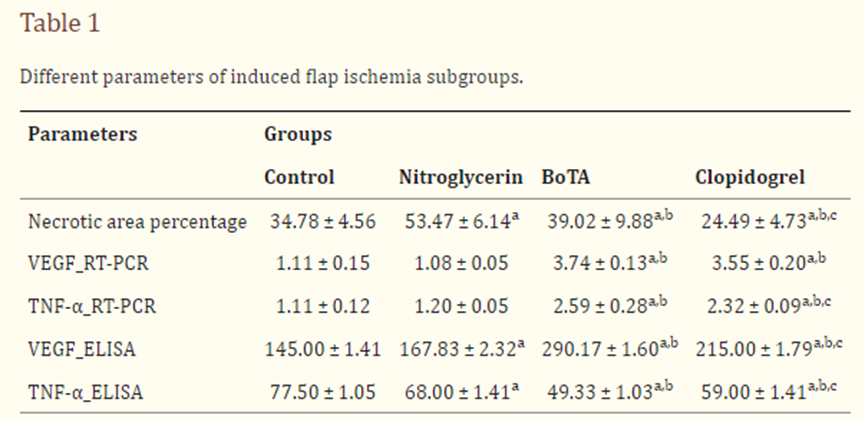
数值是平均值 ± SD.aP < 0.05与对照组比较,bP < 0.05与硝酸甘油组和cP < 0.05与BoTA组比较。统计分析采用单因素方差分析,然后进行Tukey的事后检验。BoTA肉毒杆菌毒素-A、TNF-α肿瘤坏死因子-α、VEGF血管内皮生长因子。
关于诱导的静脉充血亚组,与对照组相比,硝酸甘油和BoTA治疗在第7天的坏死百分比显著降低(p < 0.001)。此外,与BoTA和氯吡格雷组相比,硝酸甘油组的坏死面积百分比显著降低(p = 0.001和p < 分别为0.001)。然而,对照组和氯吡格雷组之间没有统计学差异(p = 0.301)(图3和表表2)。
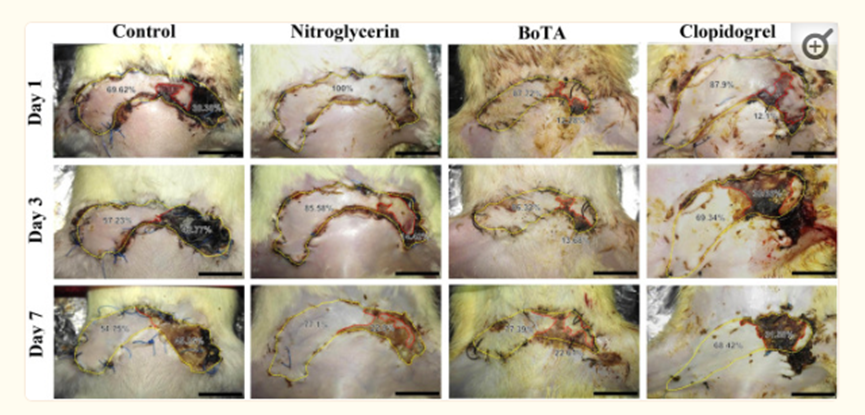
图3术后第1、3和7天诱导静脉充血亚组皮瓣的大体外观。黄色虚线勾勒出皮瓣总面积,红色虚线表示正常组织和坏死组织之间的分界。(比例尺 = 1.5厘米)。

组织病理学检查结果
在诱导的皮瓣缺血亚组的皮瓣切片中,对照、硝酸甘油和BoTA亚组的表皮和真皮较薄,胶原纤维紊乱。他们的毛囊和皮脂腺也萎缩(图4A–C)。相反,氯吡格雷亚组皮瓣显示表皮厚度增加,胶原纤维不规则程度最低,毛囊和皮脂腺发育良好(图4D)。
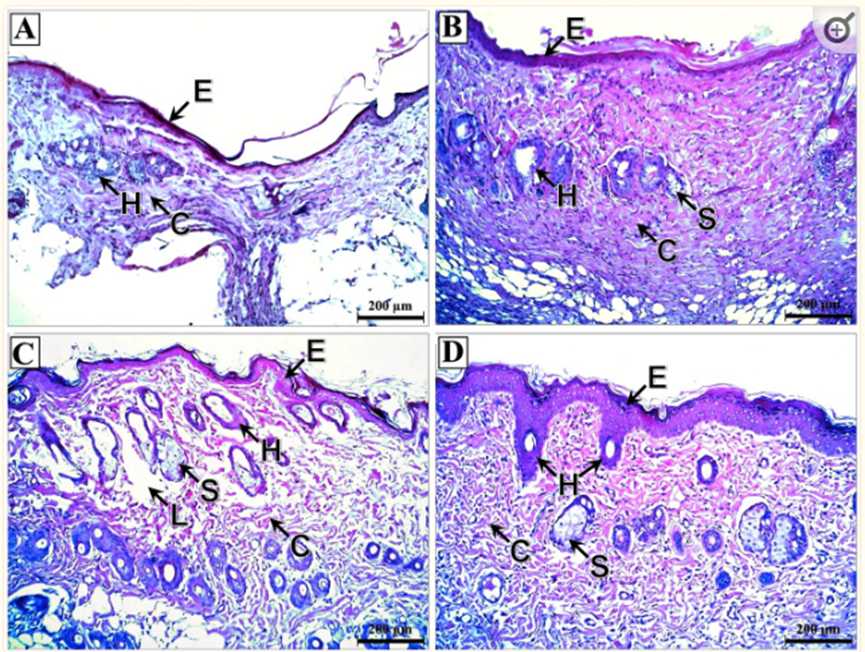
图4诱导的皮瓣缺血亚组的皮瓣切片的显微照片。(A) 对照亚组显示表皮(E)和真皮大量变薄,表皮层之间的界限消失,真皮胶原纤维广泛紊乱(C)。毛囊(H)严重萎缩,皮脂腺完全缺失。(B) 硝酸甘油亚组显示薄表皮(E),各层之间界限消失。真皮显示发育良好、中度紊乱的胶原纤维(C)和严重萎缩的毛囊(H)和皮脂腺(S)。(C) BoTA亚组显示相对较薄的表皮(E)和真皮,具有发育不足、无组织的胶原纤维(C),具有完全丧失的区域(L)。毛囊(H)和皮脂腺(S)大量退化。(D) 氯吡格雷亚组显示表皮厚度恢复(E),各层之间有明显的分界。真皮胶原纤维(C)有轻微的不规则性,毛囊(H)和皮脂腺(S)发育良好。(H&E; × 100——比例尺 = 200微米)。
关于诱导的静脉充血亚组,对照亚组的表皮广泛坏死,伴有大量炎症细胞浸润、不规则胶原纤维、脂肪浸润以及毛囊和皮脂腺退化(图第5A段)。然而,硝酸甘油和BoTA亚组显示表皮厚度恢复,胶原纤维规则,毛囊和皮脂腺完整(图5B,C)。在氯吡格雷亚组中,有表皮凝固性坏死区域,而真皮有不规则的胶原纤维、炎症细胞浸润、充血的血管以及退化的毛囊和皮脂腺(图5D)。
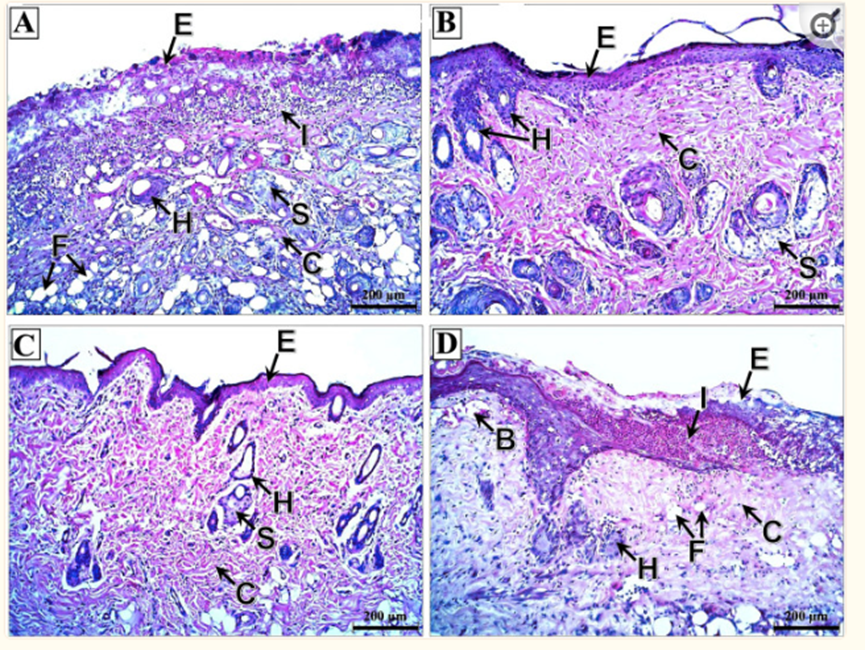
图5 诱导静脉充血亚组皮瓣切片的显微照片。(A) 对照亚组显示表皮大规模坏死(E),其细胞大部分完全丧失。真皮显示大量皮下炎症细胞浸润(I)、胶原纤维极度不规则(C)、脂肪浸润(F)以及毛囊(H)和皮脂腺(S)的严重退化。(B) 硝酸甘油亚组显示出相对较厚的表皮(E),然而,角质层大多丢失。真皮主要表现为规则的胶原纤维(C)和发育良好的毛囊(H)和皮脂腺(S)。(C) BoTA亚组显示相对较厚的表皮(E),角质层完全丧失。真皮显示中度不规则的胶原纤维(C)、大量退化的毛囊(H)和发育良好的皮脂腺(S)。(D) 氯吡格雷亚组显示表皮下炎性细胞浸润(I),表皮有大量凝固性坏死区域(E)。真皮胶原纤维不规则(C),脂肪浸润(F),血管充血(B),毛囊退化(H),皮脂腺完全缺失。(H&E; × 100——比例尺 = 200微米)。
电子显微镜发现
诱导的皮瓣缺血的皮瓣显示角质形成细胞具有常染色的不规则细胞核和肿胀的线粒体,线粒体具有相对规则的胶原纤维,这些胶原纤维在对照亚组的许多区域都不存在(图第6A、B段)。此外,硝酸甘油和BoTA亚组显示角质形成细胞过度退化,其细胞核退化,核膜缺失,细胞器丢失,细胞质空泡化,胶原纤维区域凝聚(图6C-G)。相反,氯吡格雷亚组的角质形成细胞除了具有规则的胶原纤维外,还具有规则的常染色细胞核、完整的线粒体、不同的细胞膜和桥粒(图6H,I)。
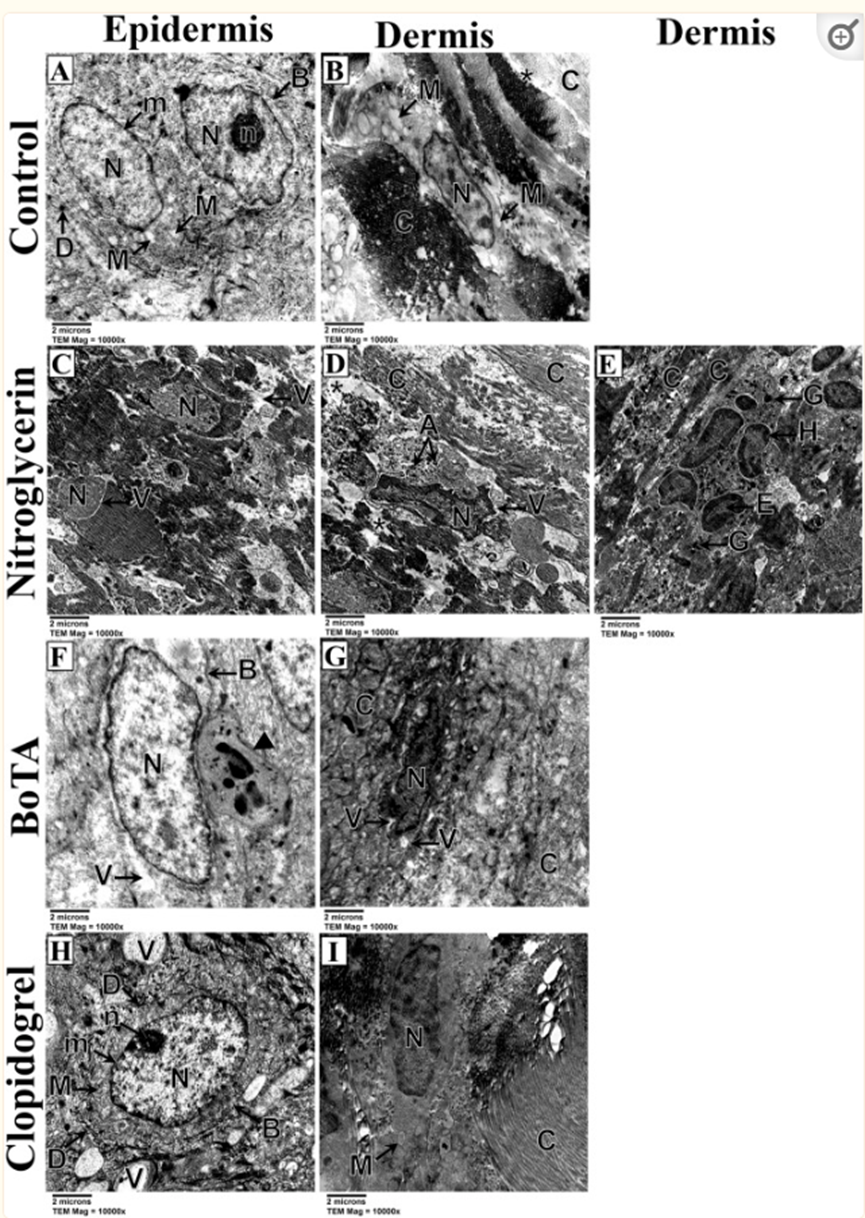
图6 诱导皮瓣缺血亚组皮瓣的电子显微照片;对照组(A,B)、硝酸甘油(C–E)、BoTA(F,G)和氯吡格雷(H,I)亚组。(A) 表皮显示角质形成细胞,常染色不规则核(N),不同的核膜(m)和其中一个明显的核仁(N)。线粒体肿胀,嵴缺失(M)。细胞边界(B)清晰可见明显的桥粒(D)。(TEM; × 10000--比例尺 = 2µm)。(B) 真皮显示成纤维细胞,具有相对规则的常染色细胞核(N)和水肿的线粒体,具有缺失的嵴(M)。胶原纤维是相对规则的,以水平和垂直的方式排列(C),然而,也有它们不存在的区域(星号)。(TEM; × 10000--比例尺 = 2µm)。(C) 表皮显示角质形成细胞具有大量退化的细胞核,在整个(N)上具有均匀的常染色质,并且没有核膜。细胞质表现出细胞器的损失和大量空泡,尤其是在细胞核周围(V)。细胞间的边界大多消失了。(TEM; × 10000--比例尺 = 2µm)。(D) 真皮显示具有不规则细胞核的成纤维细胞,显示外周染色质浓缩(N)和核周空泡化(V),以及细胞质凋亡体(a)。注意除了不存在的区域(星号)外,还存在高度堆积的胶原纤维区域(C)。(TEM; × 10000--比例尺 = 2µm)€真皮显示中性粒细胞,具有分叶细胞核,具有边缘异染色质(H)和中心亮常染色质(E)以及细胞质颗粒(G)。周围的胶原纤维显示出冷凝区域(C)。(TEM; × 10000--比例尺 = 2µm)。(F) 表皮显示具有常染色不规则核(N)的角质形成细胞。细胞质中有丢失的细胞器和细胞质空泡(V)。细胞边界明显(B),但桥粒不存在。注意角质形成细胞旁存在中性粒细胞(箭头),具有分叶细胞核和细胞质颗粒。(TEM; × 10000--比例尺 = 2µm)。(G) 真皮显示具有不规则细胞质空泡的成纤维细胞(V)和具有外周染色质凝聚的不规则细胞核(N)。注意存在高度不规则的胶原纤维(C)。(TEM; × 10000--比例尺 = 2µm)。(H) 表皮显示角质形成细胞,具有规则的椭圆形细胞核(N)、明显的核仁(N)和核膜(m),以及正常出现的具有明显嵴的线粒体(m)。细胞边界(B)高度清晰,桥粒发育良好(D)。注意细胞外空泡的存在(V)。(TEM; × 10000--比例尺 = 2µm)。(I) 真皮显示成纤维细胞,具有规则的常染色细胞核(N)和最小肿胀的线粒体,嵴缺失(M)。周围的胶原纤维高度规则且平行(C)。(TEM; × 10000--比例尺 = 2µm)。
诱导的静脉充血的对照亚组显示角质形成细胞具有退化的浓缩细胞核、肿胀的线粒体和细胞质空泡;然而,细胞边界和桥粒仍然是不同的。此外,对照亚组显示不规则的胶原纤维和中性粒细胞炎症浸润(图7A–C)。然而,除了具有常染色细胞核、完整线粒体和保存的桥粒和细胞膜的角质形成细胞外,硝酸甘油和BoTA亚组还具有发育良好的毛细血管和规则的胶原纤维(图第7D–H段)。氯吡格雷亚组显示胶原纤维和角质形成细胞退化,细胞核萎缩,线粒体肿胀,溶酶体和细胞质空泡(图7I,J)。
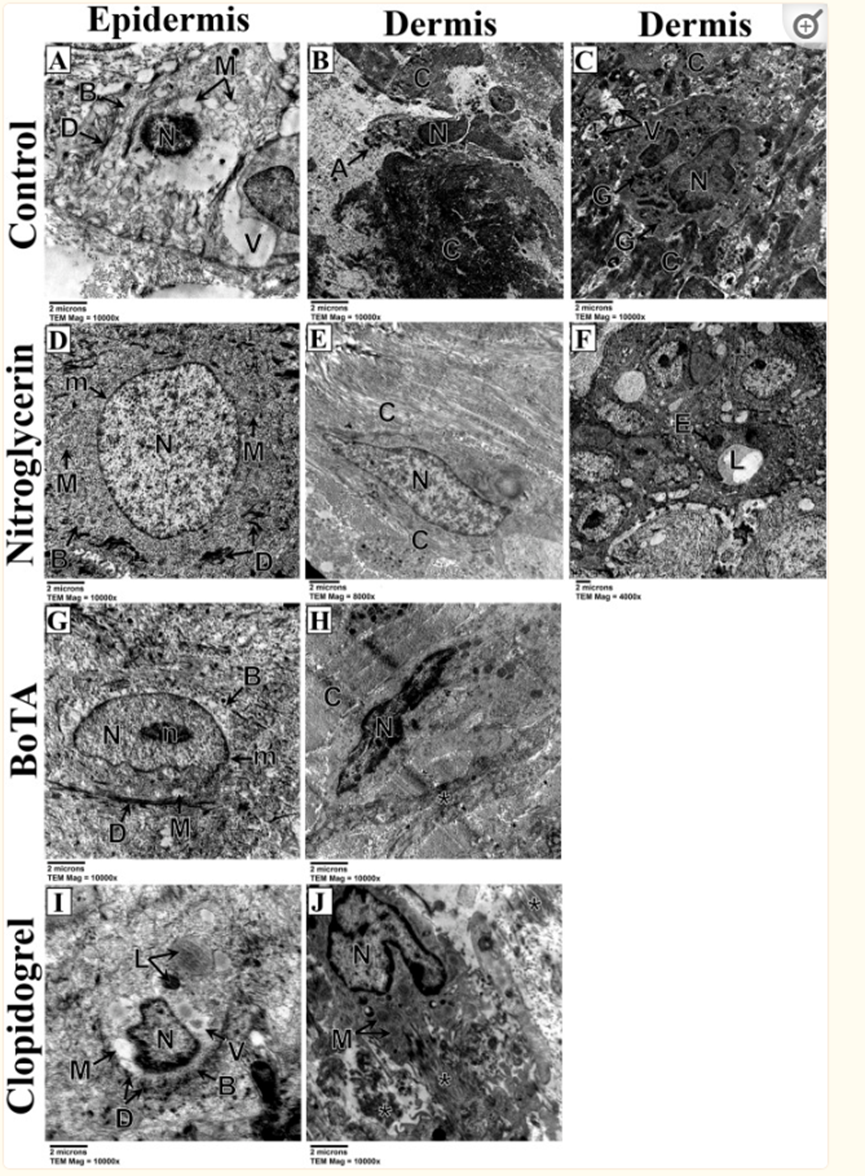
图7 诱导静脉充血亚组皮瓣的电子显微照片;对照(A–C)、硝酸甘油(D–F)、BoTA(G,H)和氯吡格雷(I,J)亚组。(A) 表皮显示角质形成细胞,其细胞核退化,染色质中央凝结(N),线粒体肿胀,嵴缺失(M)和细胞质空泡化(V)。细胞边界仍然是明显的(B),具有明显的桥粒(D)。(TEM; × 10000--比例尺 = 2µm)。(B) 真皮显示具有凋亡体的退化成纤维细胞(a)和具有高度浓缩染色质的细胞核(N)。周围的胶原纤维高度堆积且排列不规则(C)。(TEM; × 10000--比例尺 = 2µm)。(C) 真皮显示中性粒细胞,核(N)呈分叶状,胞质颗粒(G),空泡(V),周围有不规则胶原纤维(C)。(TEM; × 10000--比例尺 = 2µm)。(D) 表皮显示角质形成细胞,具有常染色的圆形核(N)和规则的核膜(m)。细胞质显示完整的线粒体和保留的嵴(M)。细胞边界明显(B),有许多桥粒(D)(TEM; × 10000--比例尺 = 2µm)。€真皮显示成纤维细胞,具有扁平规则的常染色细胞核(N)。周围的胶原纤维大多排列良好(C)(TEM; × 8000--比例尺 = 2µm)。(F) 真皮显示出发育良好的毛细血管,其具有管腔(L)并衬有内皮细胞(E)。(TEM; × 4000--比例尺 = 2µm)。(G) 表皮显示角质形成细胞,其具有常染色核(N)和基本规则的核膜(m),常染色核具有明显的核仁(N)。线粒体轻微肿胀(M),但嵴缺失。细胞边界清晰(B),有许多桥粒(D)。(TEM; × 10000--比例尺 = 2µm)。(H) 真皮显示成纤维细胞,细胞核大部分不规则,染色质高度浓缩(N)。周围的胶原纤维显示排列良好的纤维区域(C)和排列不良的纤维的其他区域(星号)。(TEM; × 10000--比例尺 = 2µm)。(I) 表皮显示高度退化的角质形成细胞,具有凋亡收缩的不规则细胞核(N)和高度空泡化的细胞质(V)。线粒体高度肿胀和空泡化(M)。存在密度不同的溶酶体(L)。尽管有明显的细胞边界(B),桥粒高度最小化(D)。(TEM; × 10000--比例尺 = 2µm)。(J) 真皮显示具有不规则细胞核的成纤维细胞,具有外周浓缩的染色质(N)。线粒体因嵴丢失而肿胀(M)。周围的胶原纤维不规则且退化(星号)。(TEM; × 10000--比例尺 = 2µm)。
实时逆转录聚合酶链式反应结果
根据诱导的皮瓣缺血亚组,与对照组和硝酸甘油组相比,皮瓣组织中VEGF mRNA的表达显著高于BoTA和氯吡格雷亚组(p < 0.001),BoTA和氯吡格雷亚组之间无统计学差异(p = 0.137)或在对照组和硝酸甘油组之间(p = 0.988). 另一方面,与对照组和硝酸甘油组相比,BoTA和氯吡格雷组的TNF-αmRNA表达显著增加(p < 0.001),与氯吡格雷组相比,BoTA亚组的表达水平显著增加(p = 0.047). 然而,对照组和硝酸甘油组之间没有统计学差异(p = 0.753)(表(表11)。
诱导的静脉充血亚组显示,与对照组相比,3个治疗组的VEGF和TNF-αmRNA表达水平显著增加(p < 0.001). 然而,根据VGEF的组织表达,3个治疗组之间没有统计学差异。此外,与BoTA组相比,硝酸甘油和氯吡格雷组的TNF-α表达显著增加(p < 0.001和p = 分别为0.003),两组之间无统计学差异(p = 0.298)(表(表22)。
酶联免疫吸附测定结果
关于诱导的皮瓣缺血亚组,与对照组相比,3个治疗亚组的血清VEGF和TNF-α水平显著升高(p < 0.001),然而,最高水平的VGEF出现在BoTA亚组,其中VGEF水平与硝酸甘油和氯吡格雷亚组相比显著升高(p < 0.001). 另一方面,氯吡格雷亚组的TNF-α水平最高,明显高于其他治疗组(p < 0.001)(表(表11)。
根据诱导的静脉充血亚组,与对照组相比,3个治疗亚组的VEGF和TNF-α血清水平显著升高(p < 0.001),与BoTA和氯吡格雷组相比,硝酸甘油组的VEGF血清水平显著升高(p < 0.001),两组间无统计学差异(p = 0.421). 然而,与氯吡格雷组相比,硝酸甘油组和BoTA组的血清TNF-α水平升高(p = 0.006和p < 0.001),而硝酸甘油和BoTA亚组之间没有统计学差异(p = 0.062)(表(表22)。
讨论
皮瓣的存活主要取决于其血管蒂通畅性25,26。因此,建议采用皮瓣手术技术来降低动脉/静脉闭塞和缺血的风险25。此外,许多治疗剂已被证明通过预防炎症、提供自由基清除、增加血管生成和/或富集微血管网络27来提高皮瓣的存活率。
到目前为止,这是第一项比较硝酸甘油、BTX-A或氯吡格雷治疗对2种类型的皮瓣血管损伤的影响的研究,包括大鼠带蒂上腹部皮瓣的动脉和静脉功能不全。
皮瓣手术最常见的并发症之一是由于未预测的血栓形成、血管痉挛和/或血管性不足而导致的远端坏死28。据观察,静脉血栓形成比动脉血栓形成更常见,具有更大程度的不可逆损伤,因此挽救率更低29。另一个损伤因素是血管痉挛,这是血管蒂皮瓣手术中常见的并发症,导致血管暂时性和不完全性阻塞。然而,它可能会延长,导致血栓形成,从而导致血管完全阻塞30。这种血管痉挛可能归因于血小板释放血清素和某些前列腺素31。通过上述机制,皮瓣缺血最终导致活性氧物质积聚,从而造成组织损伤32。皮肤的结构完整性主要由其胶原蛋白诱导,同时,成纤维细胞负责其前体的分泌:I型和III型原胶原33。因此,局部皮瓣缺氧会减少胶原蛋白的产生和成纤维细胞的复制,导致上皮化受损28。
在本研究中,动脉和静脉闭塞导致坏死区域的百分比在第7天分别增加到34.8%和43.3%。因此,人们观察到静脉阻断比动脉阻断更有害。这些结果与Matsumoto等人一致。3他们发现,到第3天,SIEA的单侧结扎导致38.2%的腹部皮瓣表面积坏死,而SIEV阻断的皮瓣的坏死率为57.7%,这也得到了组织病理学结果的证实。我们研究中的组织病理学和超微结构检查也证实了缺血和充血对皮瓣的危险影响,显示上皮变薄、真皮胶原降解以及角质形成细胞和成纤维细胞的退行性变化。在我们之前的研究中也报道了类似的发现,该研究显示了尼古丁诱导的缺血对大鼠背侧随机模式皮瓣的影响34。研究表明,皮瓣缺血会导致角蛋白分解变性、桥粒丢失、线粒体损伤和血管缺失。
硝酸甘油通过释放一氧化氮有效地引起血管舒张,导致血管平滑肌松弛,并增加组织灌注,主要作用于静脉,从而增加皮瓣的挽救反应35,36。另一个已知的理想效果是硝酸甘油发挥抗血栓作用37。Davis等人38报道,用背侧随机模式皮瓣治疗硝酸甘油软膏可将皮瓣坏死的百分比从对照大鼠的44.1%降低到硝酸甘油治疗大鼠的31.6%,当硝酸甘油与局部水杨酸三甲胺联合使用时,可将其降低到25.2%。在另一项研究中,Ghanbarzadeh等人39发现,2%硝酸甘油软膏将对照组的皮瓣坏死率从24%降至16.1%。然而,我们发现硝酸甘油最有益的治疗效果是在静脉充血的情况下,而在选择性动脉缺血的情况下效果甚微,坏死表面积的百分比分别为19.2%和53.5%。
在同样的情况下,我们发现硝酸甘油只有在静脉阻断的皮瓣下才能恢复表皮厚度、角蛋白分解特征以及真皮胶原和成纤维细胞的完整性。另一方面,硝酸甘油在硝酸甘油动脉闭塞亚组中具有有害作用。我们之前的工作还报道,根据组织病理学和超微结构评估,局部硝酸甘油软膏对背部随机模式皮瓣尼古丁诱导的缺血大鼠具有显著的挽救反应34。此外,Aral等人40还报道,局部应用NTG作为透皮贴剂可将大鼠背侧随意型皮瓣坏死的百分比从51.3%降低到39.9%。
在豚鼠血管模型中,先前已报道BoTA通过SNAP-25切割诱导血管舒张来减弱去甲肾上腺素的释放41。此外,BoTA诱导VEGF的释放,还可以增加皮瓣中一氧化氮合酶的表达13,42。此外,它还能改善伤口闭合、组织重塑和疤痕形成43。
在本研究中,组织病理学和超微结构显示,BoTA对静脉淤血皮瓣的改善效果优于缺血皮瓣。此外,坏死面积百分比显示,BoTA使动脉阻塞皮瓣的挽救反应恶化,对照组为39%,而对照组为34.8%。在Uchiyama等人13进行的另一项研究中,who报告称,在皮肤缺血-再灌注损伤开始前24小时皮内注射BoTA通过提供血管生成和预防小鼠缺氧诱导的组织损伤具有保护作用。Ghanbarzadeh等人39也在大鼠背侧随机皮瓣手术前2周皮内注射BoTA。与对照大鼠相比,坏死面积百分比从56%显著降低到24%。除BoTA外,与局部应用硝酸甘油软膏相结合,这一比例降至16.1%。更具体地说,Schweizer等人44通过解剖胸外侧动脉产生了背侧皮瓣动脉缺血的小鼠模型。他们在手术前24小时或手术期间在血管蒂附近皮下注射BoTA。皮瓣的血流量显著增加,与我们的结果相反,术前注射BoTA时,坏死表面积百分比从38%下降到16%,术中注射时,在术后5天评估时,坏死面积百分比下降到12%。
氯吡格雷是一种噻吩并吡啶衍生物,可抑制血小板聚集,是一种前药,需要称为P2C19的肝细胞色素P450酶转变为其生物活性代谢产物,并通过不可逆地阻断血小板上的P2Y12(ADP)受体来抑制血小板聚集45。Akan等人46对大鼠进行McFarlane皮瓣手术,术前单次口服氯吡格雷。对照组大鼠的坏死表面积百分比为53%,氯吡格雷治疗组大鼠则降至37%。Fatemi等人45也为大鼠提供了口服氯吡格雷治疗,但在术后7天,这导致坏死百分比从38%降低到28%。相比之下,Vieira等人17的结果显示,术后口服氯吡格雷7天,坏死率从51.61%降低到27.70%。在上腹部皮瓣模型中,Fichter等人47给大鼠服用氯吡格雷7天。本研究中的氯吡格雷使坏死率从81.13%降至36.47%。上述出版物中显示的结果与我们的结果一致,但仅在动脉闭塞组中显示坏死百分比降低了10.3%。然而,在静脉充血的情况下,这一比例仅降低了4.1%。损伤后,血管平滑肌细胞立即产生大量新生内膜,增加血管壁厚度48。然而,氯吡格雷通过抑制血小板活化和血小板-单核细胞结合,有效抑制血管紧张素II诱导的血管炎症、内膜增生和重塑49。同时,血液流量与血管50的半径的立方体成比例。因此,氯吡格雷可通过减少内膜厚度来增加动脉管腔口径,从而间接增加至皮瓣的动脉血流量。
在本研究中,除硝酸甘油组外,接受治疗的动脉闭塞亚组的VEGF组织基因表达、血清水平和TNF-α组织mRNA表达均显著增加。然而,与缺血皮瓣相比,3个治疗组的TNF-α血清水平有所下降。另一方面,在接受3种治疗方式的静脉闭塞组中,VEGF和TNF-α组织基因表达和血清水平显著增加。
VEGF信号通路主要参与血管生成,除了在内皮细胞增殖、血管舒张和增加血管通透性51,52中的作用外,它还作为新生血管疾病的主要治疗靶点发挥着至关重要的作用。因此,皮瓣中VEGF水平的增加通常与皮瓣存活率的增加有关53。另一方面,TNF-α由角质形成细胞、血管内皮细胞和成纤维细胞在损伤时产生,启动炎症白细胞向损伤组织的募集。此外,TNF-α在成纤维细胞活性、角质形成细胞和内皮细胞的调节以及参与受损组织愈合的细胞外基质蛋白和基质金属蛋白酶的合成中发挥作用54。众所周知,TNF-α还能刺激血管生成物质的局部释放,如碱性成纤维细胞生长因子、VEGF和血小板衍生生长因子亚基B,从而触发内皮细胞的增殖和迁移,从而引发血管生成55。这可能表明硝酸甘油、BoTA和氯吡格雷可以通过刺激血管生成和细胞外基质的合成来增加皮瓣的存活率,而细胞外基质在愈合过程中是必不可少的。
我们的研究表明,皮瓣缺血和静脉充血具有巨大的有害影响,包括角质形成细胞的细胞核和线粒体的损伤,而在皮瓣缺血时,氯吡格雷具有有利的作用,这反映在对细胞核和线粒体影响最小。另一方面,通过硝酸甘油治疗,静脉充血的皮瓣得到了高度改善,显示出细胞核和线粒体保留。然而,在缺血皮瓣中进行治疗后,细胞核严重退化,细胞器丢失。
这项研究有一些局限性。首先,我们无法对3种治疗方案使用相同的给药途径,这可能解释了它们治疗反应水平的差异。其次,我们不能直接测量不同研究组皮瓣的实际血流量,将其作为皮瓣存活的重要决定因素。最后,我们没有根据组织病理学、VEGF和TNF-α基因表达以及血液水平评估评估皮瓣对治疗药物的生存反应的时间过程。
尽管存在这些局限性,但我们的研究结果提供了证据,证明缺血性皮瓣的最佳治疗选择是氯吡格雷,而BoTA和硝酸甘油治疗可增加坏死皮瓣面积百分比。另一方面,静脉充血的皮瓣对硝酸甘油的缓解反应最大,其次是BoTA,然后是氯吡格雷。
结论
总之,我们的研究结果强调氯吡格雷在增加抢救反应方面是有效的,但仅适用于缺血性损伤的皮瓣,而不适用于静脉功能不全的皮瓣;其中硝酸甘油和BoTA是提高存活率的理想选择。
本信息并非旨在或暗示作为专业医疗建议的替代;不应在任何医疗紧急情况下使用,也不应用于
任何医疗状况的诊断或治疗。所有医疗紧急情况请拨打120。
1. 烧伤病人住院难,出院才是更艰难的开始。烧伤后挛缩是烧伤的常见结果,比愈合难处理数十倍。
2. 疤痕挛缩,美学不佳,预防大于治疗,专业科学的压力治疗复健可以极大改善预防问题的发生,不合规性的康复方案导致预防无效或情况更加严重会面临更严峻的重建手术
3. 重建手术不进行科学的压力治疗复健会导致手术效果不佳甚至失败。尽管名医或名机构整形外科完全松解了挛缩,即使配有理疗师也并非专业,技术断层会导致挛缩不断复发。
烧烫伤康复一站式解决平台,烧烫伤压力衣定制,硅酮支具定制,3D面罩定制,烧烫伤残疾康复
复整形重建咨询。24小时求助定制微信电话 18116590229 24小时求助定制电话18116590229




