
Teruo Murakami1 and Sadayuki Shigeki2,*
1Laboratory of Biopharmaceutics and Pharmacokinetics, Faculty of Pharmaceutical Sciences, Hiroshima International University, Higashi-Hiroshima 731-2631, Japan; moc.liamg@rmsuneg
2Department of Rehabilitation, Faculty of Rehabilitation, Hiroshima International University, Higashi-Hiroshima 731-2631, Japan
摘要
瘢痕疙瘩(KD)和增生性瘢痕(HTS)是由于一些有家族史和遗传因素的人的皮肤损伤愈合过程受损而形成的,它们长得很高,有色素,血管化和细胞化增加。由于疼痛、瘙痒、挛缩、美容问题等,这些疤痕大大降低了患者的生活质量(QOL),这取决于疤痕的位置。满足患者生活质量的治疗/预防仍在开发中。在这篇文章中,我们综述了治疗KD和HTS的药物治疗,包括预防术后复发(尤其是KD)。药物治疗包括使用单一药物的单一治疗和使用多种药物的联合药物治疗,其中药物是口服、局部和/或通过病变内注射给药。此外,KD/HTS的药物治疗有时与手术切除和/或物理治疗相结合,如冷冻治疗、激光治疗、放射治疗(包括近距离放射治疗)和硅胶/片材。关于KD/HTS的每种单一药物治疗的临床有效性的结果并不总是一致的,而是分散在研究人员中。同时靶向多个部位的多模式联合药物治疗比单一药物治疗更有效。使用PubMed、Google Scholar和在线搜索引擎搜索文献。
关键词:瘢痕疙瘩、增生性瘢痕、药物治疗、物理治疗、术后复发、多模式联合治疗
首选
1.简介
伤口愈合涉及三个不同但重叠的阶段:炎症、增殖和重塑阶段。然而,网状真皮损伤的调节愈合过程,或对真皮损伤的过度组织反应,会诱导瘢痕疙瘩(KDs)或增生性瘢痕(HTSs)。KD和HTS都会随着血管化和细胞数量的增加而升高和着色,这些疤痕伴随着患者的疼痛、瘙痒和挛缩等症状。此外,根据疤痕的位置,疤痕可能会因视觉上明显和不舒服而大大降低患者的生活质量。在正常的伤口愈合中,胶原蛋白,一种促炎因子,被用来修复受损的组织。在KDs和HTSs中,转化生长因子-β(TGF-β)的活性很高,胶原产生过剩,有许多成纤维细胞和新形成的血管,导致疤痕组织隆起、着色和增厚。然而,KDs和HTSs的生物学特性明显不同。KDs生长并突出到原始伤口的边界之外,但HTSs突出到原始创伤的边界之内。升高的HTS最终会随着时间的推移而收缩,预计有一天会自发愈合。相反,KDs在受伤后会随着时间的推移而扩增,预计不会自发愈合。遗传因素参与KDs,但不参与HTS。到目前为止,KD和HTS形成的确切机制尚不清楚,临床选择仍然有限,这些疤痕仍然是顽固性疾病。到目前为止,还没有一种治疗的黄金标准能让患者的生活质量完全满意;然而,显示出良好结果的可用治疗方法正在增加。例如,据报道,与单一药物治疗相比,使用多种药物的联合药物治疗和/或与物理治疗相结合的药物治疗,如冷冻治疗、激光治疗、放射治疗和硅胶/硅胶片材,可获得更好的结果。
在这篇文章中,我们回顾了KD和HTS在生物学特性上的差异,用于治疗KD和HTS的各种药物的药理作用(单药物治疗),使用多种药物的药物治疗的组合,药物治疗与物理治疗(包括手术切除)的组合,以及预防KD和HTS术后复发的药物治疗。如KD、HTS、治疗、管理和/或预防。目前仍在研究中、临床报道较少的新药,如反义药物和抗体药物也涉及其中。此外,还涉及仅在特定地区使用的药物,如曲尼司特和赛瑞托。Tranilast(N-[3,4-二甲氧基肉桂酰基]-邻氨基苯甲酸;Rizaben)是一种口服抗过敏药物,已批准在日本和韩国使用。Saireito是一种口服的日本草药,在日本也用于治疗KDs和HTSs。因此,曲尼司特和赛瑞托的临床数据大多以日语发表。此外,许多草药被认为仅在特定地区用于治疗和/或预防KDs/HTS,在这种情况下,临床数据可能大多以当地语言发布,这意味着很少有英文参考文献。最后,我们讨论了药物治疗的一些要点,以提高临床疗效,因为研究人员之间报告的每种药物治疗的临床数据并不总是一致的,可能是由于药物剂量不同、配方不同、治疗周期不同、临床疗效评估方法不同等原因。因此,可能很难验证每一条信息的准确性;然而,关于各种药物的信息,包括有前景的候选药物和常用药物及其使用方法,将为开发更安全、更临床有效的药物治疗提供有价值的信息。
首选
2.瘢痕疙瘩与增生性瘢痕生物学特性的比较
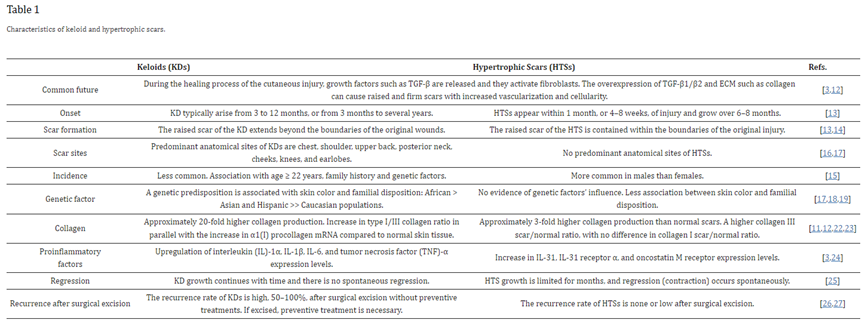
皮肤损伤是由刺激引起的,如烧伤、昆虫叮咬、皮肤穿刺、手术、纹身、创伤、疫苗接种等,如果愈合过程正常,伤口会随着时间的推移而愈合。然而,相比之下,如果要调节愈合过程,就会诱导血管化和细胞化增加的瘢痕,如KDs和HTSs。伤口愈合过程分为以下三个阶段:止血/炎症、增殖和成熟/重塑,这些愈合阶段按照时间顺序重叠。在皮肤损伤的愈合过程中,会产生各种促炎因子,如TGF-β1/β2,以及细胞外基质(ECM),如胶原蛋白、弹性蛋白、透明质酸(HyA)和蛋白多糖,以修复伤口。如果愈合过程被调节,各种细胞因子和ECM过表达,形成具有凸起和牢固疤痕的KDs/HTSs。作为促进这些疤痕形成的风险因素,涉及多种因素,如:局部因素(伤口/疤痕的张力)、全身因素(如高血压、妊娠)、遗传因素(性别、单核苷酸多态性、肤色等)、生活方式因素(包括吃辣食或洗热水澡)等[2,3,5,10,11,12,13]。尽管KDs和HTSs的产生主要是由于TGF-β1/β2和胶原的过度表达,但这两种疤痕类型也涉及明显不同的生物学特性。在表1中,列出了一些特性,如疤痕的发生、疤痕的形成(外观)、疤痕部位、发病率、遗传因素、胶原类型、增强疤痕的促炎因素、自发消退的可能性以及疤痕手术切除后复发的可能性。关于疤痕的发生,据报道,KDs在损伤后3个月至几年内发展,很少成熟,并且不遵循与正常和HTSs相同的进化、稳定和消退模式。相反,HTSs通常在伤口闭合后的4-8周内出现,并在接下来的6-8个月内发展,之后进展通常停止并变得静止。KD的凸起疤痕延伸到原始伤口的边界之外,但HTS包含在原始损伤的边界内[13,14,15]。KDs优先在皮肤张力高的部位诱导,如胸部、肩部、上背部、颈部后部、脸颊、膝盖和耳垂,但HTS可以在任何地方诱导,并且没有主要的解剖部位[16,17]。KDs和HTSs在中国的发生主要集中在9-20岁的个体(HTS:77.2%;KD:81.8%);男性是HTSs的危险因素(调整后p<0.001),KDs与家族史相关(调整后p<0.050)。关于遗传因素,据报道,KD的形成具有很强的遗传易感性,并且在某些种族中KD发展的患病率很高。与高加索人相比,来自非洲、西班牙裔和亚裔背景的人患KDs的可能性更高。KD在白化病患者中不发生,这表明黑素细胞可能在KD的形成中发挥作用。此外,人类白细胞抗原的不同等位基因在KD形成中的作用也有报道[17,18,19,20]。基底膜区结构的差异,如真皮中的胶原结构,以及HD、HTSs和正常皮肤之间肥大细胞的频率也有报道[21]。KD和HTS疤痕的增加是由于ECM,特别是胶原蛋白的过量产生,并且KD和HTS的胶原蛋白的数量和组成不同。据报道,KDs中的胶原蛋白产量增加了20倍,HTSs增加了3倍,导致出现更大的异常疤痕[12]。当在来自正常皮肤、正常疤痕、HTSs和KDs的培养的皮肤成纤维细胞中检测I型和III型胶原的合成时,与其他组相比,KDs中I/III型胶原比例显著升高,与正常皮肤组织相比,α1(I)前胶原mRNA也增加[22]。在HTSs中,III型胶原瘢痕/正常比值更高,但I型胶原疤痕/正常比值没有差异[3]。KDs和HTSs的网状层包含炎症细胞、数量增加的成纤维细胞、新形成的血管和胶原沉积物。此外,在KDs中,各种促炎因子如白细胞介素(IL)-1α、IL-1β、IL-6和肿瘤坏死因子(TNF)-α上调[2]。在HTS中,与正常组织相比,烧伤后HTS组织中IL-31、IL-31受体α(IL-31RA)和肿瘤学抑制素M受体(OSMR)的表达水平增加[23,24]。关于疤痕的消退,具有较高密度和真皮成纤维细胞增殖活性的KDs的体积继续增加并侵入周围组织。相反,具有较高密度和较低增殖活性的HTSs显示出自发消退的趋势[25]。KDs有多种治疗方法,包括手术切除单药治疗;然而,尽管HTSs在手术切除后的复发率较低[11,26,27],但在没有术后预防性治疗的情况下,单独手术切除后KDs的复发率相当高(50-100%)。
3.瘢痕疙瘩和增生性瘢痕的药物治疗
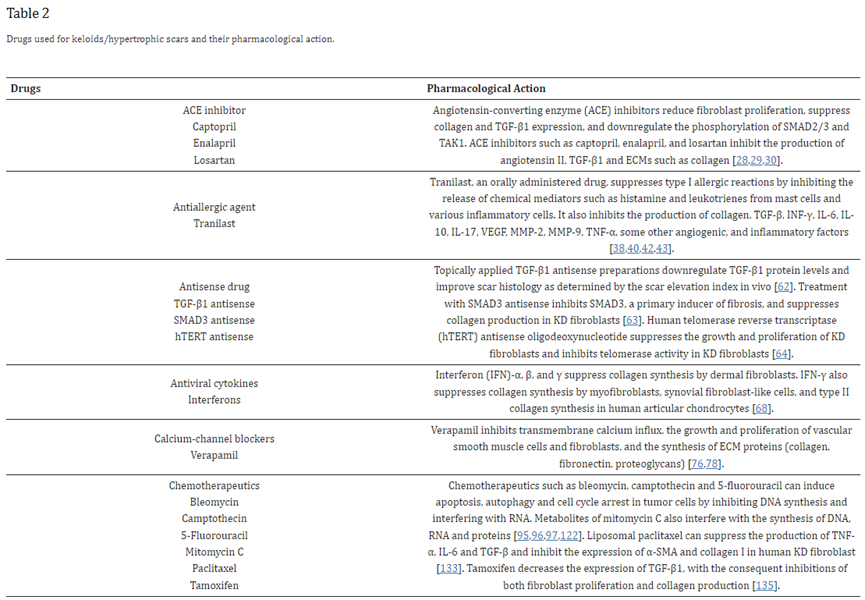
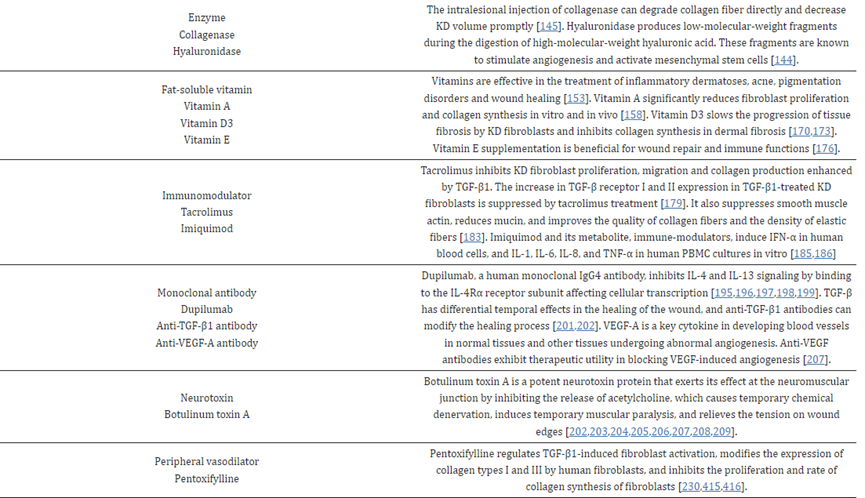
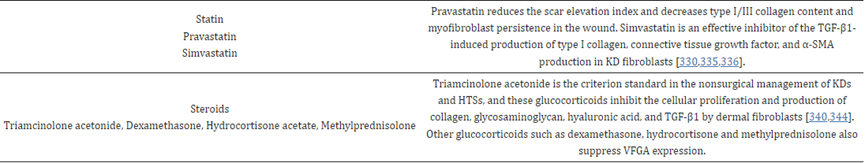
为了治疗KDs和HTSs,已经采用了各种治疗模式,包括药物治疗,如使用胶带/膏药和软膏的局部应用、病灶内注射、口服药物和不使用药物的治疗,如休息/固定治疗(胶带、硅胶布)、压迫治疗(绷带、支架、衣服)、手术、放射治疗、激光治疗、化妆治疗、心理健康护理等[27]。在这篇文章中,我们重点介绍了KDs和HTSs的药物治疗。伤口愈合过程分为以下三个阶段:止血/炎症阶段、增殖和成熟/重塑。在正常的伤口愈合中,在ECM的凋亡和重塑介导的新组织生物合成和降解之间实现了平衡。相反,在KDs和HTSs的过度愈合过程中,会诱导调节机制的功能障碍,即持续的炎症、过度的胶原合成和/或缺乏的基质降解和重塑[10]。诱导了增强纤维化的细胞因子(如TGF-β1/β2、血小板衍生生长因子(PDGF)、胰岛素样生长因子(IGF-I)、IL-4、IL-10等)的过度产生/激活,以及在止血/炎症和细胞增殖阶段增强纤维化的ECM(如胶原、纤连蛋白和糖胺聚糖),以及在成熟/重塑阶段减弱纤维化的TGF-β3、INF-γ、IL-12、胶原酶、金属蛋白酶(MMP)等的产生减少[3,5,10]。主要用于治疗KDs和/或HSs的药物对过度产生纤维化增强细胞因子(如TGF-β1/β2)和ECMs(如胶原蛋白)具有抑制作用。表2中列出的药物是血管紧张素转换酶(ACE)抑制剂、抗变态反应剂、反义药物、抗病毒细胞因子、生物组分、钙通道阻滞剂、化疗药物、水解酶、脂溶性维生素、免疫调节剂、单克隆抗体、神经毒素、外周血管舒张剂、光敏剂、植物性药物、他汀类药物和类固醇。
3.1. ACE抑制剂(卡托普利、依那普利、氯沙坦)
ACE抑制剂通常用于治疗高血压和心脏问题,因为这些药物可以通过抑制体内的ACE和降低血压来放松血管。在KD/HTS治疗中,ACE抑制剂在体外和体内减少成纤维细胞增殖,抑制胶原和TGF-β1的表达,并下调SMAD2/3和TAK1的磷酸化,通过抑制TGF-β1/SMAD2/3途径和TGF-α1/TAK1途径抑制瘢痕形成,其中SMAD/SMADs是TGF-β超家族受体的信号转导子[28,29,30]。在KD成纤维细胞中,有效浓度的卡托普利降低了所有胶原代谢、TGF-β1、PDGF-BB和热休克蛋白47(HSP47)的表达以及细胞增殖[31]。在有烧伤后疤痕的患者中,局部应用5%卡托普利(每天两次,持续6周)显示KD病变有中度至显著改善,并显著减少了发红、结垢和瘙痒[32]。在二度或三度烧伤治疗后出现HTSs和瘙痒的患者中,与安慰剂组相比,局部应用1%依那普利软膏导致的疤痕明显小于安慰剂组的疤痕,瘙痒评分明显较低[33]。使用兔耳损伤模型也报道了口服依那普利的疗效,在该模型中,皮肤损伤后早期口服依那普利可减少HTS的形成,可能是因为其对III型胶原产生的下调作用[34]。氯沙坦乳膏治疗可抑制TGF-β1、胶原和Smad的表达,并在体外和体内降低Smad的磷酸化(小鼠疤痕模型)[29,35]。研究了5%氯沙坦钾软膏对HTSs和KDs患者的疗效,氯沙坦治疗显著降低了患者的血管性和柔韧性,KD和HTS患者的温哥华疤痕量表(VSS)评分(根据血管性、高度、柔韧性和色素沉着评估疤痕)均显著下降[36]。关于口服氯沙坦治疗(从烧伤后第1天开始,持续28天),据报道,在氯沙坦治疗的伤口中发现的广泛移植物损失很可能是全层烧伤伤口临床结果不佳的原因,并且在移植前不应开始氯沙坦治疗,以防移植物损失[37]。
3.2. 抗过敏剂(曲尼司特)
Tranilast(Rizaben®,Kissei Pharmaceutical Co.,有限公司,日本东京)是一种抗过敏剂,用于治疗各种炎症疾病,如过敏性鼻炎、哮喘、特应性皮炎、支气管哮喘、过敏性结膜炎、KDs和HTSs。Tranilast在日本和韩国被批准用于治疗KDs和HTSs。曲尼司特的剂型包括口服制剂、鼻喷雾剂和滴眼液。曲尼司特通过抑制肥大细胞和各种炎症细胞释放组胺和白三烯等化学介质来抑制I型过敏反应。它还抑制胶原、TGF-β、干扰素(INF)-γ、IL-6、IL-10、IL-17、血管内皮生长因子(VEGF)、MMP-2和MMP-9、TNF-α以及其他一些血管生成和炎症因子的产生[38,39,40,41,42,43,44,45]。当评估曲尼司特(300mg/天,持续12周)在KDs或HTSs患者中的临床效果和有效性时,最终的改善、安全性和有效性总评分分别为66.7%(中度或更好)、82.9%和61.3%(中度或更好)。详细地说,超过40%的患者瘙痒和自发性疼痛的改善程度超过2个等级,压痛的改善程度约为30%。此外,疤痕的扩大趋势和红斑的改善程度分别为约50%和30%,超过2个级别。11.4%[46]的患者报告了不良反应,如轻度消化道症状,在停药或服用额外药物后恢复。同样,263名患有KDs或HTSs的日本患者口服曲尼司特(5 mg/kg/天,持续12周)后表现出显著改善[44,47]。除了口服外,曲尼司特还可以通过直肠[48]、经皮[49,50,51,52]和滴眼液给药,包括在角膜和眼睑皮肤上给药[53,54,55,56]。当曲尼司特(12 mg,溶于1.5 mL乙醇/水混合物中)通过离子电渗装置(2 mA,来自离子电渗设备的电源模块,每周一次,持续30分钟)经皮递送至受影响的HTS部位时,仅在一次或两次治疗后,患者的疼痛和瘙痒症状明显减轻,患者之间存在一些差异。当在30分钟离子电渗后的一到两小时内切除HTS的疤痕时,曲尼司特在疤痕中的回收率为给药剂量的0.02%-0.2%,这表明离子电渗给药比口服和局部应用曲尼司特更有益[49]。
3.3. 反义药物(TGF-β1、SMAD3和TERT的反义寡核苷酸)
封闭靶向基因的反义寡核苷酸被设计用于调节靶向有义RNA的功能(信号传导)和/或表达。TGF-β1在KD的形成中起着核心作用。TGF-β1治疗。反义在体外诱导KD成纤维细胞凋亡并抑制KD成纤维纤维细胞增殖[57]。此外,TGF-β1反义治疗显著增加了KD成纤维细胞培养物中肝细胞生长因子/散射因子(HGF/SF)的表达[58],显著下调了SMAD2和SMAD4的表达以及基质MMPs的分泌,并上调了SMURF2、MMP-2、-3、-9和-13以及MMP-1和-2的表达,但对体外KD成纤维瘤中的SMAD3和SMAD6没有影响[59,60,61]。
局部应用TGF-β1。反义制剂下调TGF-β1。通过体内瘢痕升高指数确定的蛋白质表达水平和改善的瘢痕组织学[62]。用基于阳离子脂质纳米颗粒的SMAD3反义处理KD成纤维细胞抑制了纤维化的主要诱导物SMAD3,并抑制了KD成纤维纤维细胞中I型胶原的产生,这表明这种递送治疗具有抑制纤维化疾病中胶原沉积的治疗潜力[63]。用人端粒酶逆转录酶(TERT)反义寡核苷酸(1.0mol/L)处理KD成纤维细胞72 h后,成纤维细胞生长受到抑制,增殖能力下降,诱导成纤维细胞凋亡,hTERT和bcl-2mRNA表达低于对照组。抑制KD成纤维细胞中的端粒酶活性是一种重要途径,可能在抗KD治疗中发挥关键作用[64]。
3.4. 抗病毒细胞因子(干扰素)
干扰素(IFN)是一组天然存在的生物反应调节剂,具有抗病毒、抗增殖、分化和增强免疫的特性[65]。用刀豆球蛋白A或脂多糖激活的人外周血单核细胞(PBMC)分别产生主要含有IFN-γ的淋巴因子或主要含有IF-β的单核因子,这些IFN可以抑制胶原的产生[66]。瘢痕疙瘩成纤维细胞的融合培养物比正常成纤维细胞产生更多的胶原(171%、187%和204%)、更多的糖胺聚糖(153%和141%)和更少的胶原酶(26%和31%)。当瘢痕疙瘩成纤维细胞在体外用IFN-α2b处理时,胶原、糖胺聚糖和标准化胶原酶活性的量分别为对照水平的64–107%、96–97%和86–96%[67]。IFN-α、β和γ抑制真皮成纤维细胞的胶原合成。IFN-γ还抑制肌成纤维细胞、滑膜成纤维细胞样细胞的胶原合成和人类关节软骨细胞的II型胶原合成[68]。据报道,治疗后,IFN-α2b降低了HTS和正常成纤维细胞中的胶原蛋白合成和I型信使RNA水平,但这些变化仅在约72小时后才明显,并且HTS成纤维细胞在停止治疗后48小时内完全从IFN-α2b对I型前胶原信使RNA的影响中恢复。这表明肥大的成纤维细胞可能对其作用不太敏感[69]。在IFN-α2b处理的HTS成纤维细胞中,MMP-1和胶原酶mRNA的组织抑制剂分别增加了81%和54%。在IFN-γ处理的成纤维细胞中,HTS中MMP-1 mRNA的组织抑制剂增加了78%,正常真皮成纤维细胞增加了56%,但胶原酶mRNA分别减少了59%和42%[70]。脂质体包裹的IFN-α2b(2000单位/mL)显著降低了真皮成纤维细胞40%的增殖,I型和III型的mRNA水平分别降低了约60%和约30%的前胶原[71]。研究人员中INF临床疗效的差异可能来自于INF在瘢痕组织中的掺入(分布)变化。INF的更多掺入(分布)预计将表现出更高的药理活性。
在临床试验中,病灶内注射IFN-γ可使瘢痕尺寸减少至少50%,并使其变平,在剂量为0.05 mg/周的情况下持续10周,没有显示出严重的毒性作用[72]。用病变内重组人IFN-γ(0.01或0.1 mg/一个病变部位)治疗显示,治疗部位的大小减少,平均高度减少30%,而对照部位为1.1%[68]。同样,病灶内注射IFNs显示KD的大小和胶原生成显著减少[73,74]。HTS患者接受了全身IFN-α2b治疗,与同一患者的正常真皮相比,他们的成纤维细胞和肌成纤维细胞总数普遍减少,凋亡细胞百分比显著增加[75]。
3.5. 钙拮抗剂(维拉帕米)
在KDs和HTSs中,观察到ECM胶原和蛋白多糖的过量产生,并且大分子的细胞分泌是一个钙依赖性过程。钙拮抗剂如VER和硝苯地平可以抑制ECM蛋白的合成。钙拮抗剂抑制跨膜钙流入、血管平滑肌细胞和成纤维细胞的生长和增殖以及ECM蛋白(胶原、纤连蛋白、蛋白聚糖)的合成[76,77,78]。VER增强人类皮肤成纤维细胞中胶原酶的分泌,表明VER增强I型胶原的分解[79]。此外,VER具有抗氧化活性,可增强一氧化氮的产生。一氧化氮在伤口愈合过程中促进成纤维细胞、角质形成细胞、内皮细胞和上皮细胞的增殖[80]。钙拮抗剂在皮肤科的应用主要基于其作为血管舒张剂和抑制肌肉收缩(如面部皱纹和疼痛的平滑肌瘤)的特性[81]。此外,钙拮抗剂可以改变KD和正常人真皮成纤维细胞的细胞形状并诱导前胶原合成[82]。在体外研究中,钙拮抗剂已被发现可减少ECM的产生,诱导前胶原合成,并抑制IL-6、VEGF和成纤维细胞的增殖[83]。
在临床上,接受局部VER治疗的患者表现出良好的疤痕质量(80%的乳房成形术疤痕和75.2%的腹部成形术疤痕),而不使用愈合调节剂的患者分别表现出48%和51.2%的满意度,表明使用局部VER可以避免整形术后KDs和HTSs[84]的发展。通过病灶内注射(0.03 mg/kg,每7-10天,6次)结合压力服给药VER,以改善烧伤引起的KDs和HTSs的状况。当通过各种参数(如色素沉着、厚度、血管分布和柔韧性)评估治疗效果时,发现VER非常有用。此外,未发现不良反应[85]。在KD患者中,每隔3周向病变内注射VER,直到病变完全变平,或最多注射6次,其中55%的患者表现出极好或良好的改善,除注射部位疼痛外,无明显副作用。VER治疗后,VEGF和MMP-9的表达显著下降[86]。耳垂KD通常难以治疗,复发率高。复发性耳垂KD采用核心皮瓣和病变内注射VER治疗。结果表明,这种治疗方法是治疗复发性耳垂KDs的可靠且具有成本效益的方法,复发率低(28.6%),患者满意度高(80%)[87]。在非洲人群中,对病变内注射VER(2.5 mg)和TAC(40 mg)治疗KD的疗效进行了比较。TAC分别在6周和12周内完全缓解了疼痛和瘙痒,而在接受VER治疗的患者中没有完全缓解。然而,对于小尺寸KD[88],VER注射与TAC相当有效。同样,当将VER的疗效和安全性与TAC进行比较时,在治疗KDs和HTSs方面,VER产生的不良事件比TAC少。这些结果表明,病变内VER可以作为病变内TAC的更安全的替代品[89,90,91,92]。另一组报告称,尽管TAC的药物不良反应比VER更普遍[93],但TAC的瘢痕血管性、柔韧性、高度和宽度的减少速度比VER更快。另据报道,与TAC治疗(40 mg/mL,与VER的给药方案相同)不同,VER治疗(2.5 mg/mL,三周间隔,共18周)没有出现治疗事件或显著改善,其中VSS在3个月随访结束时进行了评估[94]。
3.6. 化学疗法(博来霉素、5-氟尿嘧啶、丝裂霉素C、紫杉醇、三苯氧胺)
化学治疗剂,包括烷化剂、抗代谢剂、拓扑异构酶抑制剂、抗生素、有丝分裂抑制剂和蛋白激酶抑制剂,可诱导肿瘤细胞凋亡、自噬和细胞周期停滞[95,96]。化疗诱导的细胞凋亡表明癌症化疗药物可以诱导组织中的程序性细胞死亡[97]。除了类固醇注射外,BLM、5-FU和丝裂霉素C(MMC)等化学疗法已被认为是手术后瘢痕治疗和瘢痕预防的有效方式,因为这些药物靶向瘢痕组织中的成纤维细胞,并诱导细胞凋亡或调节蛋白质产生[98,99]。
3.6.1. 博来霉素
在临床上,为了治疗KDs和HTSs,通过多种表面穿刺技术给予抗癌剂BLM。44%的患者完全扁平化,22%的患者显著扁平化,14%的患者充分扁平化,但20%的患者未观察到扁平化,有14%的患者复发。得出的结论是,这种治疗是治疗KDs和HTS[100]的一线治疗方式。许多研究小组也报道了病灶内BLM治疗KDs和HTSs的有效性。在这些研究中,通过各种技术给予BLM以减轻注射疼痛,包括在皮肤表面使用多次穿刺法、电穿孔或无针喷射注射器[10101102103]。另外,KD患者接受病变内BLM治疗(平均4次)。完全扁平化达到70.8%,高度显著扁平化达到8.3%,其中局部副作用为疼痛(100%)、水泡(78.3%)、溃疡(5.8%)和色素沉着(56.7%)。最后一次治疗后6、12、15和18个月的KDs复发率分别为3.8、15.4、45.5和50%[104]。KDs患者(n=314)在手术剃刮后每月注射BLM,然后再上皮化。总的来说,87%的患者对完全扁平化非常满意,11%的患者对显著扁平化中度满意,2%的患者复发[105]。KDs和HTSs患者每3周接受一次病灶内注射曲安奈德(20 mg/mL)或BLM(1.5 mg/mL)治疗,最多6次。尽管诱发的副作用不同,但两个治疗组的疗效没有显著差异。结论是病灶内BLM与曲安奈德一样有效;然而,由于疼痛、溃疡和色素沉着等不良事件,应谨慎使用BLM[106]。
3.6.2. 羟基喜树碱
羟基喜树碱(HCPT)是一种天然植物生物碱,已被证明可诱导成纤维细胞凋亡,其中涉及内质网应激反应和线粒体功能障碍[107]。在椎板切除术后兔模型中,在椎板切除区植入HCPT脂质体可抑制胶原分泌并诱导成纤维细胞凋亡,从而防止硬膜外瘢痕的粘连[108]。类似地,HCPT通过激活兔体内的肌醇需要激酶1信号通路,诱导成纤维细胞凋亡并防止关节内瘢痕粘连[109]。在不同疾病中存在的各种类型的纤维化组织中检测到微小RNA(miR)23b3p的异常表达。HCPT治疗显著增加了miR 23b 3p的表达水平并加速了成纤维细胞凋亡,表明HCPT诱导的miR 23a 3p表达上调促进了成纤维纤维细胞凋亡[110]。10,11-亚甲二氧基核苷酸(MD-CPT)抑制KD。MD-CPT负载的HyA纳米乳液的透皮递送抑制了KD成纤维细胞的增殖,而不会对正常皮肤成纤维细胞造成严重毒性[111]。
3.6.3. 5-氟尿嘧啶(5-FU)
结节性KDs是由于I型和III型胶原的不规则产生而在创伤部位形成的纤维病变。5-FU是一种氟化嘧啶类似物,可作为抗代谢剂,抑制胸苷酸合成酶并干扰核糖核酸(RNA)合成。在临床上,病灶内注射5-FU在治疗KDs方面表现出令人满意的效果,导致疤痕体积减少和症状改善(90%的患者得到改善)[112]。5-FU是TGF-β/SMAD信号传导的有效抑制剂,能够以JNK依赖的方式阻断TGF-β诱导的、SMAD驱动的COL1A2基因表达上调[113]。在KD成纤维细胞的原代细胞系中,用低剂量5-FU(低至1 mg/mL)处理诱导KD成纤维纤维细胞的增殖、G2/M细胞周期停滞和凋亡的显著抑制,但不会立即导致细胞死亡。这些结果支持使用低剂量5-FU作为治疗KD疤痕的潜在方式[114]。与非胶原蛋白合成相比,5-FU导致Dupuytren成纤维细胞胶原产生的剂量依赖性、选择性和特异性降低。5-FU治疗成纤维细胞选择性抑制胶原合成,而5-FU处理不影响I型和III型前胶原mRNA[115]。当5-FU以每周50–150 mg的剂量在病变内注射到KDs中,最多注射16次时,33.3%的患者的KD扁平化程度超过75%,约一半的患者的治疗KD扁平化率超过50%。副作用为疼痛(所有患者)、色素沉着过度(所有病人)和溃疡(4.2%的病人)[116]。5-FU被认为是治疗KD和HTS的一种安全实用的替代方案[117]。病灶内注射5-FU在85%的KD患者中显示出超过50%的改善,尽管有一名患者反应不佳。以前未经治疗的小病变改善最大。主要不良反应为疼痛(所有患者)、色素沉着(全部患者)和组织脱落(30%的患者)。47%(9/19)的患者在1年内对治疗有反应,观察到复发[118]。局部应用5-FU负载的羧甲基壳聚糖纳米颗粒对人类KD成纤维细胞显示出显著的抑制作用,抑制率为16%[119]。含有5-FU和TAC的单针自由气动喷射注射(PJI)可以显著提高HTS的高度和柔韧性。PJI受到患者的青睐,可以作为传统针头注射的补充,尤其是对针头恐惧症患者[120]。含有TAC和5-FU的双层溶解微针表现出双相释放特性。在HTS治疗中,它导致I型胶原(Col I)和TGF-β1的mRNA和蛋白表达下调[121]。
3.6.4. 丝裂霉素C(MMC)
MMC的代谢产物与DNA交联结合,从而干扰DNA、RNA和蛋白质的合成。MMC因此能够减少成纤维细胞增殖[122]。根据培养基中MMC的浓度,在所有测试浓度(浓度范围从0.0004 mg/mL到4 mg/mL)下,连续暴露于MMC会在7天内导致成纤维细胞死亡[123]。局部MMC(0.5 mg/mL)5分钟可延迟大鼠手术伤口的愈合至治疗后第四周[124]。KD疤痕切除后,用1 cc MMC 0.4 mg/mL的纱布敷5分钟。所有患者对结果都满意,尽管仅在两例患者中观察到KD完全消失[125]。在伤口闭合之前,切除KD疤痕并将MMC(0.4mg/mL)施加到切除的床上5分钟。局部应用MMC在预防术后KD复发方面没有差异[126]。10名患者切除了全部或部分KD刮胡子,止血后局部应用MMC(1 mg/mL)3分钟。这种KD治疗对大多数患者有效[127]。病灶内MMC(1 mg/mL)治疗KDs和HTSs是有效的。许多研究人员也报道了类似的结果,其中得出的结论是,剃刮术后局部应用MMC治疗KDs和HTS[12812130]是安全有效的。局部和病灶内MMC均能有效治疗耳廓KD,其中局部MMC比病灶内注射显示出更好的VSS评分和患者满意度[131]。
3.6.5. 紫杉醇(PCT)
紫杉醇(PCT)通过诱导细胞凋亡来杀死癌症细胞。PCT结合微管并导致微管动力学的动力学抑制(稳定)[132]。此外,PCT治疗抑制人KD成纤维细胞中TNF-α、IL-6和TGF-β的产生,并抑制α-SMA和I型胶原的表达。与单独的PCT相比,负载PCT胆固醇的脂质体显示出更好的抑制细胞增殖、迁移和侵袭的能力,并有效地促进细胞凋亡和阻滞G2/M期的细胞周期[133]。在HTS兔耳模型中,PCT减少了HTS的形成。在用>400 mg/L PCT溶液处理的兔耳模型中发现局部坏死[134]。
3.6.6. 三苯氧胺
三苯氧胺(TAM)是一种非甾体抗雌激素药物,通常用于治疗癌症,可降低TGF-β1的表达,从而抑制成纤维细胞增殖和胶原蛋白的产生[135]。在KD成纤维细胞中,TAM通过减少TGF-β的产生来减少KD成纤维纤维细胞胶原的合成。与对照组相比,在4µM的TAM下,总TGF-β活性降低了49%,在8µM的TAM下,TGF-β的活性降低了85%[136]。与胎儿成纤维细胞相比,KD成纤维细胞显示TGF-β1的产生增加。TAM通过降低TGF-β1的表达来改善KD的伤口愈合[137]。在正常成人皮肤成纤维细胞中,在10至20µM的TAM浓度下,晶格收缩程度是剂量依赖性的,但在50至100µM的浓度下,成纤维细胞聚集的胶原晶格的收缩被完全抑制。成纤维细胞对收缩的剂量和时间依赖性抑制表明,TAM可能在治疗异常真皮瘢痕方面具有潜在的适用性[138]。在临床上,TAM以剂量依赖的方式延迟正常人真皮成纤维细胞的细胞增殖速率,浓度高达12µg/mL,更高的浓度,接近50µg/mL时,似乎对细胞生长有毒性影响。生长因子产生的分析显示,碱性FGF和VEGF水平降低,但TGF-β1水平没有变化[139]。有HTSs病史的患者接受了不同皮肤切口的手术,根据标准方案在术后服用TAM片,并评估了HTSs的发展。结论是,TAM似乎是预防术后HTSs复发的有效药物[140]。病变内注射TAM可促进炎症刺激和胶原纤维的减少,并显著减少产生胶原的成纤维细胞的数量[141]。局部应用2%TAM软膏(每天两次,持续8周)可增加血管生成并降低纤维化组织厚度,而不会改变烧伤皮肤区域的疤痕表面积。这表明TAM可以通过减少挛缩和防止HTSs和KDs的形成来加速伤口愈合过程[142]。
3.7. 酶(胶原酶、透明质酸酶)
在具有凸起和牢固疤痕的KDs/HTS中,胶原蛋白、弹性蛋白、HyA和蛋白多糖等ECM过度产生[143]。胶原酶和透明质酸酶都可以通过分别水解高分子量胶原(肽)和HyA(糖胺聚糖)来产生低分子量片段[144]。
3.7.1. 胶原酶
据报道,病灶内注射胶原酶可以降解胶原纤维并降低KD体积,尽管体积可能会随着时间的推移恢复到相同(或更大)的水平。胶原酶注射的副作用是注射部位疼痛、肿胀、起泡、溃疡和瘀斑[145]。在临床上,耳垂KDs患者在注射后的12个月内每天接受病灶内注射胶原酶和压迫耳环的治疗。所有患者的耳垂KD大小平均减少了50%。副作用包括注射部位肿胀、压痛和一处溃疡,在2周内自行消退。得出的结论是,病灶内胶原酶加压治疗耳垂KD是一种安全且适度有效的治疗方法[146]。
3.7.2. 透明质酸酶
在美容整形手术中,透明质酸酶通常用于过度矫正和不对称,其中透明质酸蛋白酶的剂量相当多样化和异质[147]。据报道,HyA在瘢痕组织中的分布、数量、分子量和特征与正常组织不同[21148]。已知透明质酸酶产生的HyA的低分子量片段可刺激血管生成和激活间充质干细胞[144]。在皮肤病学中,透明质酸酶的使用可有效增强向局部部位的药物递送,包括KDs/HTSs,治疗与粘蛋白沉积相关的疾病,以及其在外科手术中的潜在用途[149]。在临床上,透明质酸酶在消除HyA体积过剩方面非常有效,皮内注射透明质酸蛋白酶可以在几个小时内消除患者的不适和不美观的肿块[150]。用透明质酸酶软膏治疗术后瘢痕可显著改善瘢痕组织的功能和美容外观。检测了透明质酸酶软膏在面部不同部位术后HTSs患者术后HTS治疗中的有效性,其中透明质酸蛋白酶在离子电渗的帮助下经皮递送。通过VSS评分评估疤痕情况。治疗1个周期后,VSS总分降至5.14±0.9,治疗2个周期后从治疗前的10±1.5降至0.85±0.9[151]。在KDs的治疗中,病灶内TAC、病灶内TAC-透明质酸酶和病灶内射频TAC-是有效的方法。在这些治疗中,就安全性而言,病变内TAC和透明质酸酶的组合比其他两种更好,副作用最少[152]。
3.8. 脂溶性维生素(维生素A、维生素D3、维生素E)
维生素是人体皮肤的天然成分,是抗氧化剂系统的一部分,可以保护皮肤免受氧化应激。含有视黄醇(维生素A)、L-抗坏血酸(维生素C)、α-生育酚(维生素E)和烟酰胺的产品具有强大的抗氧化和抗炎特性。它们可有效治疗炎症性皮肤病、痤疮、色素沉着障碍和伤口愈合[153]。在本节中,综述了亲脂性、脂溶性维生素如维生素A、D3(胆钙化醇)和E治疗KD/HTS的疗效。
3.8.1. 维生素A
维生素A缺乏会阻碍修复。维甲酸(与维生素A化学相关的维生素)使类固醇延迟的修复恢复正常。维生素A倾向于抑制细胞培养中的成纤维细胞,并刺激类固醇处理的巨噬细胞在组织中启动修复行为[154]。维生素A和维甲酸对愈合伤口中胶原积聚和纤维增生的刺激作用是由于成纤维细胞分化和胶原合成增强[155]。一篇综述文章报道了维生素A主要通过核维甲酸受体、类维甲酸X受体和过氧化物酶体增殖物激活受体发挥作用。维甲酸调节皮肤内许多细胞类型的生长和分化,其缺乏会导致上皮角化异常。在受伤组织中,维生素A刺激表皮更新,增加上皮再形成率,并恢复上皮结构[156]。
在临床上,每天局部应用0.05%的视黄酸溶液可以轻微到显著地减少KD/HTS疤痕的大小,并减少大多数患者的瘙痒等主诉[157]。在人类成纤维细胞中,类视黄醇,尤其是全反式视黄酸(维甲酸),会显著减少成纤维细胞增殖和胶原合成[158]。烧伤后,疤痕皮肤缺乏弹性,尤其是在HTSs中。用维甲酸(全反式维甲酸)局部治疗可以改善皮肤的外观和质量(即质地、膨胀性、颜色和水合作用),这将提高患者的生活质量[159]。在受伤前或受伤后三天内使用泼尼松(40 mg或更大)可抑制伤口愈合,但局部或全身给予维生素A可逆转泼尼松的抑制作用[160]。高剂量维生素A,如10000 IU/kg/天,而非低剂量维生素A(如1000 IU/kg/日),可显著逆转皮质类固醇对肠吻合愈合的抑制作用,无论是术前还是仅术后给予[161]。维生素A的全身给药改善了慢性类固醇患者的伤口愈合。在使用类固醇治疗的大鼠的伤口愈合模型中,在伤口闭合前应用维生素A 10分钟,并在伤口闭合之前单独放置凝胶泡沫海绵,这两种方法都会增加断裂强度和拉伸强度[162]。糖皮质激素(皮质类固醇)会导致手术切口裂开,增加伤口感染的风险,并延迟开放性伤口的愈合。尽管维生素A不能逆转糖皮质激素对伤口收缩和感染的有害影响[163],但维生素A可以恢复炎症反应,促进上皮化以及胶原和基质物质的合成。在大鼠中,皮下注射甲基强的松龙可显著降低伤口液中的TGF-β和IGF-I水平以及组织中的羟脯氨酸含量。口服全反式和9-顺式维甲酸部分逆转甲基强的松龙诱导的TGF-β和IGF-I的下降,并显著增加羟脯氨酸含量,使其接近正常水平。这些数据表明,类固醇和类视黄醇对伤口愈合中的生长因子和胶原沉积具有拮抗作用[164]。
3.8.2. 维生素D
维生素D3是一种强效抗炎剂,在皮肤中产生,其产生受到多种因素的影响,其中黑色素的含量是至关重要的。色素沉着的增加已被证明会减少皮肤中维生素D3的合成量。KD在深色皮肤的人群中更为普遍,如非裔美国人。除了调节钙稳态外,维生素D在细胞增殖、分化、癌症进展、炎症和纤维化中发挥重要作用。在KD成纤维细胞中,维生素D减缓组织纤维化的进展,并抑制真皮纤维化中的胶原合成。此外,维生素D3还以剂量依赖的方式减少KD成纤维细胞的细胞增殖、胶原合成和凋亡诱导。维生素D的活性依赖于维生素D受体(VDR),即VDR降低大多数KD疤痕的蛋白质水平。补充维生素D或钙后,VDR表达降低恢复到对照值[16516616716819710717]。在KD成纤维细胞中,1,25-二羟基维生素D3(1,25D)抑制TGF-β1诱导的I型胶原、纤连蛋白和α-SMA的表达,并调节TGF-β诱导的纤溶酶原激活物抑制物-1和基质MMP-9的表达[172]。在临床上,维生素D的活性形式1,25(OH)2D3抑制KD成纤维细胞的增殖,并且维生素D受体多态性与KD的形成之间存在相关性。因此,维生素D可能发挥部分由基质MMPs介导的抗纤维化作用[173]。KD患者在病灶内注射维生素D(200000 IU/1 cm病灶,每周,3-4次)治疗后,VSS评分显著降低[170]。据报道,病灶内注射维生素D是治疗KD的一种很有前途的选择,因为它易于获得,成本低,安全性好[174]。
3.8.3. 维生素E(α-生育酚)
在KD表面使用硅(聚二甲基硅氧烷)板治疗KD是有效的,因为皮下组织的过度水合作用。在HTSs或KDs患者中,在两个周期(1个月和2个月)结束时,在硅板中添加维生素E的治疗产生的评分明显高于单独使用硅板的治疗[175]。维生素E(α-生育酚)通过细胞信号和基因表达影响伤口愈合,并影响耐甲氧西林金黄色葡萄球菌(MRSA)感染,而补充维生素E有利于伤口修复和免疫功能[176]。
3.9. 免疫调节剂(他克莫司、咪喹莫特)
他克莫司是一种钙调神经磷酸酶抑制剂,是一种主要用于预防器官移植后排斥反应的免疫抑制剂,也用于各种炎症性皮肤病。在皮肤疾病中,他克莫司是通过局部应用短期使用的,因为口服他克莫斯的使用受到限制,因为它具有严重的不良反应,如感染、高血压和神经毒性[177]。咪喹莫特是一类新的免疫反应刺激剂,可增强先天和后天免疫途径(特别是1型辅助T细胞介导的免疫反应),从而产生抗病毒、抗肿瘤和免疫调节活性,并首次被批准用于外生殖器和肛周疣的局部治疗[178]。
3.9.1. 他克莫司
在KD成纤维细胞中,增殖和迁移显著高于正常成纤维细胞,他克莫司抑制TGF-β1增强的增殖、迁移和胶原产生。他克莫司还抑制TGF-β1处理的KD成纤维细胞中TGF-β受体I和II表达的增加,表明他克莫斯通过下调TGF-β接收器有效阻断KD成纤维纤维细胞中的TGF-β/Smad信号通路[179]。此外,他克莫司显著下调人脐血管内皮细胞和HTS成纤维细胞中人血管生成因子VEGF-A、FGF-2、PDGF-β和TGF-β1的表达。他克莫司介导的血管生成抑制可以降低关键纤维化标志物的基因表达,包括α-SMA和胶原1和3[180]。
在兔耳模型中,发现皮内注射他克莫司(0.5 mg/cm2)可有效预防KDs和HTSs,不会引起全身或局部副作用[181]。此外,在兔耳模型中,局部使用0.03%和0.1%他克莫司软膏可在短期(30天)内降低炎症变化的严重程度,并积极改变疤痕的宏观方面[182]。同样,在兔耳HTS模型中,0.3%他克莫司软膏可有效抑制TGF-β和SMA,减少粘蛋白,改善胶原纤维的质量和弹性纤维的密度[183]。他克莫司常用于治疗银屑病;然而,其临床应用受到其透皮给药速率等的限制。开发了一种基于HyA的给药系统,称为阻断贴片(BP),以增加他克莫司的经皮给药。负载他克莫司的BP在体内显示出令人满意的透皮释放能力,并在小鼠银屑病样皮炎中显示出良好的抗炎能力[184]。
3.9.2. 咪喹莫特
咪喹莫特及其代谢产物在体外诱导人血细胞中的IFN-α以及人PBMC培养物中的IL-1、IL-6、IL-8和TNF-α[185186]。此外,咪喹莫特还诱导人血细胞中的IL-1α、IL-1受体拮抗剂、IL-1β、IL-10、粒细胞-巨噬细胞集落刺激因子(GM-CSF)、粒细胞-CSF(G-CSF)和巨噬细胞炎症蛋白-1α[187]。咪喹莫特对包括INF-α、INF刺激基因和IL-6在内的各种细胞因子的诱导也已报道使用小鼠[188189]。
在临床上,每天睡前使用5%咪喹莫特乳膏一次,持续8周。使用咪喹莫特时未观察到复发,但所有KD在停用咪喹莫特后4周内完全复发[190]。如后所述,局部咪喹莫特经常用于预防KD手术切除后的复发。
3.10. 单克隆抗体(Dupilumab、抗TGF-β1抗体、抗-VEGF-A抗体)
抗体疗法,也称为免疫疗法,使用单克隆或多克隆(多特异性)抗体是一种针对参与疾病过程的特定蛋白质并标记其被体内免疫系统破坏的医学治疗方法。基于抗体的蛋白质用于分析、纯化和富集靶蛋白,并介导或调节生理反应[191]。在临床上,靶向抗原的抗体治疗是更重要的生物治疗方法之一,这在很大程度上是由于抗体框架的稳定性、特异性(靶向性)和适应性。单克隆抗体形式的衍生物,如双特异性抗体、抗体-药物偶联物和抗体片段,已证明在治疗人类疾病方面有效,特别是在免疫学和肿瘤学领域[192]。KD是一种纤维增生性皮肤疾病,由皮肤损伤后的长期炎症引起,其特征是真皮网状层中的胶原积聚和血管增殖(血管生成增强)[193]。在KD或HTS组织中发现细胞因子,如TGF-β、IL-6、基质MMP、IGF-1和B细胞。开发靶向这些细胞因子的生物抗体可能是预防和治疗KDs/HTS[194]的潜在策略。
3.10.1. Dupilumub
IL-4和IL-13是标志性的2型细胞因子,它们通过与共享IL-4Rα链的两种受体(IL-4R a)结合而发挥作用。由于IL-4和IL-13在过敏性疾病的发病机制中起着重要作用,阻断IL-4和IL-3信号是治疗过敏性疾病一种强大而有效的策略。Dupilumab(Dupixent®)是一种全人类单克隆抗体,可识别IL-4Rα并阻断IL-4和IL-13信号[195196197198199]。在临床上,一名患有严重带状疱疹感染的患者口服杜匹鲁布治疗,许多疤痕变平,但一些疤痕进一步发展。当通过病灶内注射杜匹鲁单抗进一步治疗大且最顽固的KD时,在2个月内观察到更显著的改善[198]。同样,一名患有数个KDs的患者对口服四环素和局部病灶内皮质类固醇有反应,接受皮下杜匹单抗治疗(每两周一次)。随着治疗次数的增加,病变的升高和红斑减少[199]。相反,当两名弥漫性KD患者接受dupilumab治疗三个月时,没有观察到任何改善,一名患者出现临床恶化。结论是,需要进一步研究Th2细胞因子阻断作为KDs潜在治疗选择的效用[197]。
3.10.2. 抗TGF-β1抗体
在培养的KD成纤维细胞中,与正常真皮成纤维细胞相比,1型胶原、基质MMP-1、MMP-2和TIMP-1组织抑制剂的产生分别增加了3倍、6倍、2.4倍和2倍。KD成纤维细胞的迁移活性也增加了2.5倍。向KD成纤维细胞培养物中添加抗TGF-β1抗体将增加的生产和迁移活性降低到正常真皮成纤维细胞的水平[200]。在一项动物研究中,在早期、中期和晚期用抗TGF-β1、2和3抗体对兔耳伤口进行皮内治疗。早期治疗组的治疗伤口显示伤口愈合延迟,疤痕肥大没有减少。中晚期治疗组(从受伤后7天开始)的疤痕肥大程度均显著降低[201202]。在一篇综述文章中,据报道,当应用于术后切除的KD时,IFN-α2b的使用显示出18%的复发率。5%咪喹莫特可将剃毛后KDs的复发率在6个月时降至37.5%,在12个月随访时降至0%。TGF-β1反义寡核苷酸在体外和动物模型中显示出对TGF-β介导的瘢痕形成的有效和持久的抑制作用。每天注射针对TGF-β1和TGF-β2的中和抗体显示瘢痕形成的成功减少[203]。
3.10.3. 抗-VEGF-A抗体
VEGF-A是一种抗血管生成IgG,是正常血管发育以及肿瘤和其他经历异常血管生成的组织中血管发育的关键细胞因子。VEGF在调节瘢痕组织产生中也发挥着重要作用,高VEGF水平与正常、HTS和KD瘢痕的瘢痕形成有关,而VEGF的抑制导致瘢痕组织沉积[204]。在一项体外研究中,将抗TGF-β1、PDGF、抗内皮素1(ET-1)、抗VEGF和抗碱性FGF中和抗体分别添加到毛细血管内皮细胞的培养基中。HTS中发生的内皮功能障碍有助于成纤维细胞抑制和瘢痕消退,TGF-β1、PDGF和碱性FGF水平的降低在这些过程中比VEGF和内皮素1(ET-1)发挥更重要的作用[205]。在一项动物研究中,评估了抗VEGF抗体修饰的脂质体凝胶(PAE-BEV唇凝胶)在预防和治疗HTS方面的功效,其中PAE-BEV-唇凝胶在兔耳中表现出较慢的透皮递送速率、显著的皮肤滞留效果和优越的生物利用度。与其他组相比,局部PAE-BEV唇凝胶治疗显示出较低的疤痕增殖率、更少和更疏松的胶原纤维和纤维肌细胞、更多规则的软骨细胞、更少钙化的组织和更少的炎症细胞。PAE-BEV唇对兔耳HTS的预防和治疗有一定的作用[206]。在临床上,抗VEGF抗体已证明在阻断VEGF诱导的血管生成方面具有治疗作用[207208]。
3.11. 神经毒素(肉毒杆菌毒素,BTX)
BTX是一种源自肉毒杆菌的强效神经毒素蛋白,它抑制神经肌肉接头处乙酰胆碱的释放。将少量BTX注射到特定的过度活动的肌肉中会引起局部肌肉放松,从而平滑覆盖的皮肤并减少皱纹[209]。BTX-A型(BTX-A)也用于单药治疗或联合治疗中KDs和HTSs的治疗和预防。BTX-A的作用机制尚未阐明,但BTX-A涉及对伤口张力的作用、对胶原的作用和对成纤维细胞的作用[210]。在体外KD成纤维细胞中,添加BTX-A改变了S100钙结合蛋白A4、TGF-β1、VEGF、MMP-1和血小板衍生生长因子亚基A(PDGFA)基因的表达水平[211]。BTX-A抑制向肌成纤维细胞的增殖和分化[212]。另据报道,BTX-A可通过减少成纤维细胞增殖、调节TGF-β的活性以及减少KD衍生和HTS衍生的真皮成纤维细胞中促纤维化细胞因子的转录和表达来减少皮肤纤维化[213]。在KD组织中,肌成纤维细胞标志物α-SMA、I型胶原和III型胶原的表达增加,BTX-A降低α-SMA和I型胶原及III型胶原表达,增强脂肪细胞标志物PPARγ和C/EBPα的表达,并增加脂滴的积聚[214]。
临床上,KD患者接受病变内皮质类固醇(A组)或病变内BTX-A(B组)治疗。观察到病变的体积、高度和发红评分显著降低(A=B),病变明显软化(A>B),所有患者的主观主诉显著减少(A<B)。A组的三名患者(25%)出现明显的皮肤萎缩和毛细血管扩张,表明与病灶内皮质类固醇相比,病灶内BTX-A表现出更高的疗效和安全性,客观参数也有相当的改善[215]。据报道,BTX-A是预防HTS的一种合适的潜在疗法。BTX-A组和对照组(使用非BTX-A)的疤痕宽度、患者满意度和视觉分析得分均存在显著差异[216]。同样,BTX-A在预防术后疤痕(包括KD/HTS)和改善东亚人面部疤痕的外观方面比非治疗更有效[217]。比较病变内TAC、BTX-A及其联合治疗KD病变的临床疗效。病灶内类固醇与BTX-A的联合注射似乎优于单独治疗,并提供了更安全、更有效、副作用更少的最佳益处[218]。当比较病变内BTX-A和5-FU在KD治疗中的临床疗效时,BTX-A比5-FU更好地使病变变平。在BTX-A治疗组中,与中型和大型病变相比,小型病变的临床反应没有统计学上的显著差异,尽管在5-FU治疗中,小型和中型病变的反应明显好于大型病变[219]。通过VAS评分、VSS评分、疤痕厚度、瘙痒程度和患者满意度评估,在KDs和HTSs的治疗中,皮质类固醇与BTX-A联合使用比单独使用皮质类固醇更有效[220]。在患有烧伤后KDs/HTSs的儿童中,与对照组(未治疗)相比,病灶内注射BTX-A(每月一次,持续6个月)显著改善了相关的瘙痒、疼痛、柔韧性、红斑和疤痕厚度[221]。在一篇综述文章中,BTX-a被注射到KD和HTS中(1个疗程/月),持续3个疗程,并通过VSS、观察者疤痕评估量表(OSAS)和患者疤痕评估量量表(PSAS)评分评估临床疗效。得出的结论是,BTX-A可能是治疗KDs和HTSs的良好治疗方法,具有显著的临床和组织学改善[222223]。
3.12. 外周血管扩张剂(戊酮可可碱)
戊酮可可碱(PTF)是甲基黄嘌呤可可碱的类似物,是一种血液流变剂,其主要作用包括增加红细胞柔韧性、降低血液粘度、增加微循环流量和组织灌注,从而改善四肢缺血性肌肉的氧气供应[2224225]。PTF最初被开发用于四肢慢性闭塞性动脉疾病引起的间歇性跛行患者。此后,该药物还被用于治疗各种皮肤病,包括外周血管病、血管炎和血管病、色素性purpuric皮肤病、坏死病、KD、HTS等[226]。在体外,PTF抑制成纤维细胞、胶原、糖胺聚糖和纤连蛋白的产生,并增加正常人真皮成纤维细胞的胶原酶活性[66727]。在Graves眼病和胫前黏液水肿患者的培养成纤维细胞中也观察到PTF对增殖和糖胺聚糖合成的抑制作用[228]。此外,PTF对从成熟烧伤疤痕中分离的成纤维细胞的收缩和增殖产生剂量依赖性抑制[229]。在源自烧伤后瘢痕的人类成纤维细胞培养物中,PTF(1 mg/mL)降低了成纤维细胞的细胞数量增殖和收缩,并选择性地抑制了III型胶原的合成,尽管I型胶原合成的抑制在无瘢痕皮肤组中更为明显[230]。此外,在体外,PTF抑制KD、硬皮病和变形成纤维细胞的增殖和胶原合成速率[231]。研制了用于皮肤创伤愈合的PTF/壳聚糖膜(PTF/CSF)。在小鼠伤口中,具有更高浓度的PTF(4 mg/mL)的PTF/CSF在第2天将面积减少了60%[232]。在临床上,烧伤患者接受病灶内PTF作为烧伤后口腔周围HTSs的辅助治疗。病灶内PTF(1 mg/mL,每周五次,每周一次)治疗烧伤后HTS有效[230233]。比较病变内PTF、TAC及其联合治疗KD的疗效。PTF和TAC的组合产生了明显更好的结果,TAC诱导的副作用风险较低[234]。
3.13. 光敏剂前药(5-氨基乙酰丙酸、甲基氨基乙酰丙酸)
光动力疗法(PDT)是一种涉及光敏剂、氧气和光的联合作用的有治疗前景的方法,已成为治疗多种实体瘤和传染病的有治疗前途的方法。在治疗皮肤疤痕时,PDT通过增强上皮再形成、促进血管生成以及调节皮肤稳态来刺激伤口愈合[235]。在最近的一篇综述文章中,据报道,使用5-氨基乙酰丙酸(5-ALA)作为光敏剂的PDT已被开发为皮肤伤口的一种有前途的非侵入性治疗方法,如皮肤癌症、慢性腿部溃疡和侵蚀性脓疱性皮肤病,其中20%的5-ALA溶液、600 nm至670 nm之间的波长(红光)、120 J/cm2的能量密度、每周一次的频率和三次疗程是最广泛选择的治疗参数[236]。
5-ALA和氨基乙酰丙酸甲酯(M-AL)是前药,在细胞内代谢形成光敏分子原卟啉(PpIX)。当PpIX被可见红光激活时,会产生细胞毒性ROS和自由基。这种光毒性作用可导致恶性和非恶性过度增殖组织被破坏,体积缩小,最终消失[235237]。此外,局部ALA诱导的PDT通过增强上皮再形成、促进血管生成以及调节皮肤稳态来刺激伤口愈合[238]。在一项体外研究中,使用5-ALA和M-AL评估了在5 J/cm2和10 J/cm2的红光(633±3 nm)下使用和不使用简并波的PDT对KD成纤维细胞的细胞毒性作用。发现PDT与简并波刺激相结合可显著增强对KD成纤细胞的细胞毒作用[239]。使用M-AL和5-ALA作为细胞内光敏剂的前体,评估PDT对从不同病变部位(顶部、中间和边缘)获得的KD成纤维细胞的细胞毒性作用。KD成纤维细胞PDT后的细胞毒性取决于病变部位、光敏剂的前体和te光能,尽管PDT对靶向KD治疗有效[240]。制备了5-ALA负载的纳米乙醇体(5-ALA-ES)凝胶。发现5-ALA-ES可增加5-ALA在体外的透皮给药和在体内对兔HTS组织的渗透。使用5-ALA-ES凝胶和兔HTS模型评估PDT的疗效。5-ALA-ES凝胶的PDT通过促进HTSs成纤维细胞凋亡、重塑胶原纤维和增加MMP3表达来改善HTS[241]。检测用5-ALA-PDT处理的HTS成纤维细胞。5-ALA-PDT通过抑制介导HTS形成的TGF-β1信号通路的激活来抑制成纤维细胞收缩并促进细胞死亡[242]。
在临床上,一名KD患者对各种常规治疗(包括局部硅胶片、类固醇霜、类固醇注射和手术切除)有4年的阴性反应史,在5个月内使用M-AL进行PDT治疗。KD疤痕的大小显著缩小,表面变得平坦光滑,美容效果尚可[243]。M-AL-PDT在三种不同条件下对KDs患者的疗效进行了评估:现有的KD疤痕、手术后的去核和手术后的全切除。因此,PDT通过减少血流量、增加柔韧性以及降低胶原蛋白和血红蛋白水平来减少KDs中的疤痕形成。在9个月的随访中,20名患者中只有1名出现KD复发[244]。用高浓度单剂量5-ALA-PDT治疗面部化脓性汗炎引起的严重HTS。该治疗可以有效、安全地改善严重HTS,随访11个月内未观察到复发[245]。5-ALA和HyA的复合物在体外表现出显著增强的皮肤滞留以及内源性光敏剂(原卟啉IX)的产生和积累的增加。在临床上,5-ALA-HyA复合物有效地降低了疤痕的厚度和升高指数,并且疤痕与未损伤的组织紧密匹配。此外,5-ALA-HyA治疗显著下调α-SMA和TGF-β1的基因表达水平[246]。评估5-ALA-PDT联合微针或CO2晶格激光与病灶内倍他米松注射液治疗增生性痤疮疤痕患者的临床疗效、复发率和安全性。两种PDT与病灶内注射倍他米松显示出同等的临床效果,但在随访期的6个月内复发率较低[227]。一名患者在术后第一天接受5-ALA-PDT治疗,每周一次,共五次。在为期两年的随访中,发现早期5-ALA-PDT可降低血管密度并改善ECM沉积[247]。评估了5-ALA-PDT联合5-FU注射液和TAC溶液治疗痤疮HTSs的临床疗效和安全性。治疗后,瘢痕病变缩小变平,瘢痕变软,随访6个月无复发[248]。
3.14. 植物基药物(芦荟、积雪草、姜黄素、绿茶、金丝桃苷、LoureirinA/B、洋葱提取物、白藜芦醇、Saireito、紫草素、大黄素、格拉布里丁、山奈酚、雷公藤、乌贝子)
各种植物性药物,包括源自植物来源的纯材料和粗材料,在临床环境中被广泛用于治疗各种疾病,包括皮肤伤口,如KDs和HTSs,以及癌症。据报道,许多用于KD和HTS治疗的本地植物性药物来自不同地区,如:非洲[249]、巴尔干地区(东南欧)[231]、南巴尔干和东地中海地区[250]、中国[251252]、格鲁吉亚-土耳其边境[253]、日本[254]、萨尔塔省(阿根廷)[255]和塞尔维亚东南部[256]。报道了一些有效治疗HTSs的中药植物来源及其主要活性化合物的例子,如:高良姜、积雪草。,大黄、人参。(人参皂苷Rb1)、黄芩(黄芩苷)、银杏(槲皮素)、刺五加(川芎)、丹参(隐丹参酮)、红豆杉(Taxus wallichiana Zucc)。(PCT)、Stephania tetrandra S.Moore(粉防己碱)和山奈(Kaempferia galanga L.)【252】。在本节中,回顾了可用于处理KDs/HTSs并来源于植物的一些活性化合物和/或粗材料(提取物)。
3.14.1. 芦荟
芦荟。f.(百合科)是一种著名的传统药用植物,因其潜在的抗氧化、抗炎和伤口愈合活性而在世界各地使用[257]。芦荟由对伤口愈合过程有益的基本成分组成,如氨基酸、维生素C和E以及锌,据报道,芦荟的主要生物活性多糖是乙酰甘露聚糖[258259]。在一项使用正常人类真皮成纤维细胞的体外研究中,在芦荟花和芦荟凝胶之间观察到针对微纤维相关糖蛋白4的对皮肤伤口愈合的协同作用[257]。
在临床上,擦伤的脸一侧用标准的聚环氧乙烷凝胶伤口敷料治疗,另一侧用饱和稳定芦荟的聚环氧丙烷凝胶敷料治疗。芦荟部位的伤口愈合快了约72小时,这可能是由于细菌污染、随后的KD形成和/或色素变化的减少[260]。在接受正中胸骨切开术的患者中,比较了含有15%草药提取物的硅胶在洋葱提取物、积雪草提取物、芦荟提取物和纸桑提取物中预防或改善HTS的效果。与安慰剂相比,硅胶加草药提取物凝胶在高度和柔韧性方面显著改善了疤痕[261]。在硅胶片、软石蜡和聚酯敷料等伤口敷料中添加芦荟已成为一种理想的方法[226263]。在接受过手术的患者中,比较了使用含有芦荟或洋葱提取物的硅胶预防术后KDs和HTSs的疗效。含有芦荟或洋葱提取物的硅胶片都能有效预防术后疤痕。[262]. 综述了芦荟治疗烧伤疗效的一些临床数据[263]。
3.14.2. 积雪草
积雪草是一种药用植物,3000年前就已经被用作“灵丹妙药”。该植物含有一些五环三萜类化合物作为活性化合物,如积雪草苷、积雪甲苷、积雪酸和马德卡西酸,其中积雪酸和马德卡西酸分别是积雪草苷和马德卡西苷的苷元,常用于伤口愈合。在这些化合物中,积雪草苷和积雪草苷是中国药典中积雪草的标志性化合物,这些三萜化合物具有多种药理性质,包括伤口愈合、抗炎、抗氧化、抗过敏和抗纤维化活性。因此,这些化合物被广泛用于治疗皮肤异常,包括烧伤,并被认为在抗衰老、皮肤水合作用、胶原蛋白合成、紫外线防护和治愈疤痕方面具有美容功效[264]。在KD成纤维细胞中,积雪草苷以时间和剂量依赖的方式降低成纤维细胞增殖,抑制I型和III型胶原蛋白和mRNA表达,在转录和翻译水平上降低TGF-βRI和TGF-βRII的表达,并增加Smad7蛋白和mRNA的表达。积雪草酸通过PPAR-γ激活抑制TGF-β1诱导的胶原表达、Smad 2/3磷酸化和纤溶酶原激活物抑制物-1(PAI-1)在人类KD成纤维纤维细胞中的表达,表明积雪草酸是负责KD管理的活性成分之一[265266]。Madecassoside还抑制成纤维细胞从KD迁移,增强伤口愈合并减少KD的形成,这表明该化合物在治疗和/或预防HTSs和KDs方面有很大的用途[267]。积雪草苷和积雪草苷的这些活性表明,积雪草可能在治疗和/或预防HTS和KD方面具有潜在用途[265268]。
在临床上,评估了在乳膏中使用积雪草提取物预防中厚皮片供皮部位瘢痕形成的疗效,其中乳膏在上皮化完成后至少2周施用。Centella乳膏改善了色素沉着参数和比较总VSS评分[269]。在既往患有HTS或KD的受试者中,评估了补充积雪草(Gotu Kola)的天然提取物centellicum®(Horphag Research有限公司,Geneva,Switzerland)对外科伤口愈合的影响。结论是,补充Centellicum®是安全的,不会干扰其他伴随治疗。其耐受性良好,且对治疗的依从性最佳[270]。最近,制备了用于治疗HTS的唾液酸包埋转移体凝胶(AATG),AATG显示在2、4和8周时没有不良皮肤反应,黑色素指数显著降低,皮肤净弹性增加[271]。
3.14.3. 姜黄素类(姜黄素)
姜黄素是一种在姜黄中发现的香料,由于其抗炎和抗氧化活性而被广泛使用。在自然界中,姜黄素由姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素组成,姜黄素类化合物已被发现可抑制纤维化。姜黄素在较高浓度(50100µmol/L)下可显著抑制成纤维细胞中的细胞增殖和I型胶原合成,尽管在较低浓度(12.5µmol/L)时,姜黄素显示出增强细胞增殖的趋势[272]。在一项使用KD成纤维细胞的体外研究中,细胞摄取姜黄素以剂量依赖的方式阻断了KD成纤维纤维细胞中ECM的过度产生和TGF-β1/p-SMAD-2的水平[273]。在一项动物研究中,在受伤前,将溶解在1%乙醇中的粗姜黄素或纯姜黄素(6μg/kg、30μg/kg或60μg/kg)静脉注射给兔。纯姜黄素治疗显著促进非缺血性伤口愈合,增加上皮再形成和肉芽组织形成,并显著降低促炎细胞因子IL-1和IL-6以及趋化因子IL-8[274]。
3.14.4. 绿茶提取物(儿茶素特别是(-)-表没食子儿茶素-3-没食子酸盐,EGCG)
绿茶(山茶)、未发酵茶和成分儿茶素具有多种药理活性,如抗氧化、抗癌、降血糖、抗菌、抗病毒、神经保护、血管生成和抗纤维化特性。例如,绿茶可以辅助治疗糖尿病、阿尔茨海默病、传染病、口腔癌症和皮炎,并在日常生活中的卫生保健和疾病预防中发挥重要作用[275]。绿茶中表现出抗菌特性的重要成分是儿茶素,四种主要的儿茶素是(-)-表儿茶素(EC)、(-)表儿茶素-3-没食子酸盐(ECG)、(–)-表没食子儿茶素(EGC)和(–)表没食子子茶素-3-没食子酸酯(EGCG)[275]。在这些儿茶素中,EGCG对人类病理和生理过程具有多种有效作用,如抗癌、抗氧化、抗炎、抗胶原和抗纤维化作用[276]。
绿茶提取物和EGCG单独抑制肥大细胞刺激的I型胶原表达,可能通过干扰KD成纤维细胞中的PI-3K/Akt/mTOR信号通路[277]。此外,EGCG在体内KD模型中抑制生长和胶原产生,表明EGCG可以通过抑制STAT3信号通路来抑制KD的病理特征[278]。在兔耳HTS模型中,EGCG显著抑制HTS的形成以及TGF-β1、Col I、Col III、α-SMA和eNOS的mRNA表达。这表明EGCG是一种有用的HTS治疗药物,通过抑制纤维化基因表达和抑制血管生成发挥作用[279]。
在体内KD模型中,EGCG治疗也抑制了生长和胶原蛋白的产生,表明EGCG通过抑制STAT3信号通路抑制KD的病理特征[278]。在原位人KD组织中,EGCG显著降低KD体积(到第4周为40%),增加细胞凋亡(从第1周至第4周≥40%),并降低增殖(到第2周≤17%)。在离体评估中,EGCG诱导表皮收缩,降低mRNA和蛋白质水平的胶原蛋白I和III,耗尽98%的KD相关肥大细胞,并在第4周降低细胞数量和血管计数的百分比[280]。
3.14.5. Hyperforin
贯叶金丝桃(Hypericaceae),也称为圣约翰草,其活性成分如金丝桃苷和金丝桃素,具有广泛的药用用途,特别是作为抗抑郁、伤口愈合和抗菌剂。穿孔H.的临床研究根据疾病类型分为三大类:精神、内分泌和皮肤问题[281282]。
众所周知,穿支H.或hyperforin可以用作传统的抗抑郁药,因为它们抑制神经元对血清素、去甲肾上腺素多巴胺、γ-氨基丁酸(GABA)和L-谷氨酸的摄取[282]。此外,穿孔H.制剂(如油或酊剂)的局部应用可用于治疗轻微伤口和烧伤、晒伤、擦伤、瘀伤、挫伤、溃疡、肌痛和许多其他疾病[283]。在皮肤问题类别中,它用于成纤维细胞[284]。在2D和3D体外真皮构建体中,hyperforin通过减少人类真皮成纤维细胞的增殖,在5–10µM的浓度下将人类真皮成细胞的活力降低至70%[285]。接受手术分娩的妇女用穿支H.软膏或安慰剂软膏治疗,每天三次,持续16天。对照组术后未进行任何干预。在产后40天进行评估时,局部应用H.穿支软膏是安全的,可以促进剖宫产伤口愈合,并最大限度地减少疤痕和相关疼痛和瘙痒的形成[286]。
3.14.6. Loureirin A/B
Loureirin A/B是龙血树(Dracaena cochinchinensis)的主要活性成分,可抑制KD成纤维细胞的增殖、迁移和TGF-β1诱导的肌成纤维细胞分化[287288289]。龙血树树脂是从云南龙血树中提取的一种龙血树脂。它自古以来就被许多文化用作药物。在大鼠切除和切口伤口模型中,与对照组相比,用含有龙血藤素B的龙血藤乙醇提取物治疗显示出明显更好的伤口收缩和更好的破皮强度[290]。
3.14.7. 洋葱提取物,Contractubex®凝胶
洋葱提取物已被用于处理KD/HTS。槲皮素是洋葱中的主要活性化合物,具有很强的抗氧化和抗癌特性。槲皮素抑制成纤维细胞增殖、胶原产生以及KD和HTS衍生成纤维细胞的收缩,并阻断KD成纤维细胞中IGF-I的信号转导和TGF-β/Smad信号通路[291]。Contractubex®凝胶是一种市售的外用制剂,由10%的洋葱提取物、每1g凝胶50/U的肝素钠和1%的尿囊素组成[292]。
使用单独的洋葱提取物(第1组)、单独的硅胶片(第2组)或洋葱提取物和硅胶片的组合(第3组)对患有HTSs或KDs的患者进行6个月的治疗。洋葱提取物与闭塞性硅敷料的组合被认为能有效降低疤痕高度[293]。在接受过手术的患者中,比较了含有芦荟或洋葱提取物的硅胶在预防术后KDs和HTSs方面的功效。含有芦荟或洋葱提取物的硅胶片均能有效预防术后疤痕[262]。将含有5%洋葱提取物和5%HyA的普鲁兰基凝胶(治疗-1)或单独的硅胶(治疗-2)局部应用于新的术后伤口。治疗-1显著降低了患者的VSS评分、POSAS评分、瘙痒和发红,并显示局部炎症明显减少,这可能导致患HTS或KD的概率降低[294]。接受胸部手术的患者使用Contractubex®凝胶进行局部治疗。当通过疤痕大小、疤痕色素沉着和HTSs或KDs的复发率进行评估时,Contractubex®凝胶可用于胸部手术后的疤痕治疗[292]。在大鼠中,进行皮肤活检以形成全层伤口,并在10天后每天局部应用Contractubex®凝胶、单独的肝素或单独的尿囊素。免疫组织化学和超微结构观察表明,与肝素单药和尿囊素单药治疗相比,Contractubex®凝胶显著提高了伤口愈合质量,减少了疤痕形成[295]。使用激光去除纹身,并用Contractubex®凝胶治疗疤痕区域。当地经验显示,近25%的患者出现瘢痕(KD或HTS)。Contractubex®凝胶组的瘢痕形成率在统计学上显著低于对照组[296]。HTS患者接受了Contractubex®凝胶或皮质类固醇局部治疗,其中局部给药Contractubex™凝胶明显比皮质类固醇治疗更有效。此外,与局部应用皮质类固醇相比,Contractubex®凝胶治疗的不良事件显著减少[297298]。使用Contractubex®凝胶对患者进行洋葱提取物治疗腹部HTS形成的疗效检查。在手术切除原发性剖腹产疤痕后,使用Contractubex®凝胶[299]对VSS的血管性、色素沉着和身高分量表获得了更好的结果。然而,相比之下,一些研究小组报告了以下内容:比较了硅胶、硅胶片和Contractubex®凝胶治疗烧伤后HTSs的疗效。硅胶产品,无论是凝胶还是片状,在处理HTS[300]方面都优于Contractubex®凝胶。另外,在硅胶、Contractubex®凝胶和无干预组中,作为主观疤痕参数的血管性、柔韧性、色素沉着和高度在上肢急性损伤后伤口的HTSs中没有统计学差异
3.14.8. 白藜芦醇
白藜芦醇是最著名的多酚类己烯酚,存在于葡萄、蓝莓、桑椹、花生、覆盆子、大黄和其他几种植物中。白藜芦醇对免疫系统的影响与不同自身免疫和慢性炎症疾病的广泛健康益处有关[302]。白藜芦醇通过将细胞周期阻滞在G1期并诱导成纤维细胞凋亡来显著抑制细胞生长;它还降低羟脯氨酸(或胶原)水平,并下调人类HTS成纤维细胞中I型和III型前胶原mRNA的表达水平[303]。在一项体外研究中,白藜芦醇处理KD成纤维细胞以剂量依赖的方式降低I型胶原、α-SMA和HSP47的表达。此外,白藜芦醇减少TGF-β1的产生并抑制其增殖,并诱导KD成纤维细胞凋亡,对正常皮肤成纤维细胞没有任何不良影响[304]。缺氧促进KD成纤维细胞增殖并抑制其凋亡,但白藜芦醇可逆转缺氧对KDs的影响,抑制KD成纤维纤维细胞中的胶原合成,并通过下调缺氧诱导因子(HIF)-1α促进细胞凋亡[305]。
3.14.9. Saireito(或Sairei-to)
Saireito(或Saireito)是日本传统草药(Kampo),在临床上用作口服药物来治疗KD/HTS。Saireito提取物颗粒(Kracie Saireito extract Grants®)可商购。据报道,saireito对成纤维细胞抑制活性的机制是由于抑制TGF-β1诱导的Smad2/3磷酸化[254306307]。在烧伤、创伤或手术后的KDs或HTSs患者中,将赛瑞托治疗KDs/HTSs的临床疗效与曲尼司特(Rizaben®胶囊100 mg)进行比较,其中赛瑞托的剂量为2.3 g,每天3次,持续12周,曲尼司t的剂量为100 mg,每天3次达12周。赛瑞托和曲尼司特组的改善率很高,分别为54.3%和47.5%。saireito组的脸红、硬结和肿胀等症状的早期改善比曲尼司特组更显著[308]。
3.14.10. 紫草素
紫草干根等中草药的活性成分之一紫草素具有抗增殖、抗炎和抗血管生成的活性。紫草素具有诱导ROS、抑制外泌体释放和诱导细胞凋亡的作用[309]。紫草素抑制p63(一种II型整合膜蛋白)、细胞角蛋白10、α-SMA、TGF-β1和I型胶原的表达,这些在HTS的形成中起着重要作用,这表明紫草素作为一种新型疤痕治疗具有潜在的用途[310]。此外,紫草素通过HTS衍生成纤维细胞的自噬促进HTS修复,其中潜在机制可能与AMP活化蛋白激酶/哺乳动物雷帕霉素靶点(mTOR)信号通路有关[311]。在体外的人类皮肤成纤维细胞中,紫草素通过细胞外信号调节激酶/Smad信号通路减少TGF-β1诱导的胶原产生,并通过下调α-SMA表达减弱TGF-β1-诱导的细胞收缩[312]。
烧伤皮肤表现出Warburg样代谢的证据,如KDs。针对这种改变的代谢可以改变正常瘢痕形成的轨迹,这表明使用紫草素预防异常瘢痕形成的临床可能性[313]。开发了可溶性紫草素HyA微针以增强皮肤渗透性。在一项使用HTS成纤维细胞的体外研究中,递送系统显著降低了HTS成纤维纤维细胞的活力和增殖,并下调了纤维化相关基因(即TGFβ1、FAP-α和COL1A1)[314]。
3.14.11. 大黄素
大黄素是广泛使用的中草药大黄的主要成分,已被用于治疗多种疾病的炎症。大黄的乙酸乙酯提取物含有大黄素(一种天然蒽醌衍生物)、大黄酸和没食子酸作为活性化合物,对HTS成纤维细胞具有抗增殖活性。通过瘢痕升高指数、胶原结构和炎症评估,大黄素显著减轻了小鼠伤口模型中的HTS炎症[315316]。在兔耳HTSs中,与非治疗对照组相比,大黄素凝胶显著降低了HTSs的硬度以及TGF-β和IL-1的表达。此外,大黄素凝胶降低了HTSs的硬度,并抑制了局部成纤维细胞的增殖[317]。此外,大黄素可通过抑制TGF-β1信号传导,进而抑制大鼠炎症、HSP47表达、肌成纤维细胞分化和ECM沉积,发挥其抗纤维化作用[318]。另据报道,大黄素通过抑制大鼠伤口模型中的巨噬细胞极化来减弱HTS的形成和纤维化,这与抑制巨噬细胞中的神经源性基因座notch同源物(notch)和TGF-β途径有关[299]。
3.14.12. 其他植物性药物(格拉必定、山奈酚、雷公藤红、五倍子)
据报道,从光甘草中分离出的一种典型的黄酮类化合物光桥蛋白可以阻断癌症中粘着斑激酶(FAK)-类固醇受体共激活子(Src)复合物的形成;它还表现出对HTS病理的治疗作用,可能是通过FAK/Src的共同失活,这进一步导致FAK-Src去缔合[319]。此外,玻璃桥蛋白可以通过诱导细胞凋亡和减少胶原生成来抑制人类KD成纤维细胞的增殖[320]。
山奈酚,也称为山奈酚-3或山奈,是一种黄酮类化合物,天然存在于茶以及许多常见的蔬菜和水果中,包括豆类、西兰花、卷心菜、葡萄、草莓、番茄、柑橘类水果、苹果和葡萄柚[321]。山奈酚通过靶向HTS中的TGF-β受体I型,抑制增生性瘢痕中成纤维细胞胶原的合成、增殖和活化[322]。
雷公藤红素在传统中药雷神藤中具有活性,通过诱导ROS的产生和激活c-Jun N-末端激酶(JNK)信号通路,改善与KD形成和生长相关的KD成纤维细胞的病理特征[323]。此外,在一项使用NIH/3T3细胞的体外研究中,雷公藤红,一种具有生物活性的五环三萜化合物,通过降低MMPs、VEGF和碱性FGF的表达来抑制NIH3T3细胞的生长[324]。
在一项使用KD衍生成纤维细胞的研究中,五倍子软膏水溶液通过下调I型和III型前胶原的表达来限制KD成纤维细胞增殖,从而减少KD组织中的胶原沉积[325]。五味子是一种被称为收敛药的传统中药。在KD小鼠模型和人KD衍生的成纤维细胞中,五倍子软膏通过抑制成纤维细胞增殖和促进成纤维细胞凋亡来抑制KD的形成[326]。在一项使用KD衍生成纤维细胞的体外研究中,五倍子软膏以时间和剂量依赖的方式抑制KD衍生成细胞的增殖[327]。
3.15. 他汀类药物(辛伐他汀、洛伐他汀、普伐他汀、阿托伐他汀)
他汀类药物,如辛伐他汀、洛伐他汀、普伐他汀和阿托伐他汀,是世界各地广泛使用的治疗高胆固醇血症的降胆固醇药物。除了降脂作用外,他汀类药物还以其多效性和抗炎活性而闻名,因为他汀类药物可以缓解由各种病理损伤引起的组织纤维化[382329]。在高加索患者中,胸骨正中切开术和体外循环心脏大手术后,HTSs的形成率为29.7%。Logistic回归分析证实了年龄调整后他汀类药物的保护作用,其中更高剂量的他汀类药物显示出更强烈的保护作用。因此,通过正中胸骨切开术,他汀类药物的使用可以有效预防心脏手术后HTSs的复发[328]。
3.15.1. 辛伐他汀
在一项使用KD成纤维细胞的体外研究中,辛伐他汀(一种用于降低胆固醇水平的3-羟基-3-甲基戊二酰辅酶a还原酶抑制剂)抑制了TGF-β1诱导的I型胶原、CTGF和α-SMA的产生[330]。在常氧、缺氧或TGF-β1处理下,观察辛伐他汀对KD成纤维细胞增殖、凋亡和蛋白表达的影响。辛伐他汀在缺氧条件下显著诱导KD成纤维细胞凋亡,降低I型胶原和CTGF,并增加金属蛋白酶组织抑制剂(TIMP)-1,其中在常氧条件下48小时没有显著作用。此外,辛伐他汀在TGF-β1处理下显著抑制CTGF的表达[331]。在兔HTS模型中,制备辛伐他汀和普伐他汀的局部乳膏制剂,并评估其减少瘢痕肥大和减轻真皮纤维化的能力。单独局部应用10%辛伐他汀乳膏,而不是2%辛伐他汀和10%普伐他汀乳膏,与单独使用载体乳膏相比,显著减轻了瘢痕的肥大。数据表明,局部使用10%辛伐他汀乳膏可拮抗真皮纤维化并减少肥大[332]。
3.15.2. 阿托伐他汀、洛伐他汀、普伐他汀
使用无动物的人类组织工程HTS模型[333]报道了阿托伐他汀治疗HTS以及5-FU和TAC的有效性。在人Tenon’s囊成纤维细胞中,阿托伐他汀抑制增殖和迁移,并诱导细胞凋亡。此外,阿托伐他汀下调TGF-β2的表达水平,以及SMA、p38、Smad3、纤连蛋白、I型胶原和III型胶原的蛋白水平[334]。在兔耳HTS模型中,在创伤后第15、20和25天用低、中或高剂量的病灶内辛伐他汀、洛伐他汀或普伐他汀进行治疗。低剂量(40μM)辛伐他汀、洛伐他汀和普伐他汀分别显著降低疤痕升高21.9%、25.8%和22.8%,低剂量辛伐他汀显示CTGF表达显著降低。相反,中剂量(120μM)和高剂量(400μM)他汀类药物组没有显著改变瘢痕升高[335]。在兔耳模型中,6.5%浓度的辛伐他汀和普伐他汀脂质体局部治疗(术后第6-28天)显著降低了伤口中的瘢痕升高指数,也降低了I/III型胶原含量和肌成纤维细胞的持久性。此外,普伐他汀脂质体治疗降低了瘢痕组织中编码CTGF、I型胶原和III型胶原的转录物的表达水平[336]。
3.16. 类固醇(曲安奈德、地塞米松、醋酸氢化可的松、甲基泼尼松)
糖皮质激素及其衍生物,如TAC、地塞米松(DEX)、醋酸氢化可的松和甲基强的松龙,广泛用于治疗炎症性疾病、自身免疫性疾病和癌症。糖皮质激素也表现出广泛而有效的生理和治疗作用。它们的重要作用是通过许多不同和互补的机制调节基因转录,靶基因包括大多数炎症介质,如趋化因子、细胞因子、生长因子及其受体。然而,由于副作用的诱导,如皮肤病和免疫副作用,以及糖皮质激素耐药性,它们的临床应用受到限制[373338]。
3.16.1. 曲安奈德(TAC)
据许多研究人员报道,病变内TAC注射仍然是非手术治疗的金标准[89,93,94]。TAC是一种具有抗变态反应活性的合成糖皮质激素(一类皮质类固醇),在临床上,除了口服、静脉内、肌肉内和吸入给药外,该药物还被注射到各种局部受影响的部位,例如关节内、软组织内、滑膜内、局部皮内、鼻内、耳道、食管部位等。在皮肤病(如KDs和HTSs)伴有凸起皮肤疤痕的情况下,病灶内给药是最广泛使用和有效的治疗方式[339]。在一项体外研究中,TAC在无血清体外模型中显著增加了人KD成纤维细胞碱性FGF的产生,并降低了TGF-β1的产生[340]。TAC在特发性腕管综合征中下调促纤维化基因和ECM调节因子,如TGF-β、胶原和整合素[341]。此外,TAC降低了COL1、COL3和α-SMA的蛋白质和mRNA表达水平,并以剂量依赖的方式抑制了人类HTS成纤维细胞的增殖、侵袭和迁移,并且TAC的病灶内注射显著降低了具有瘢痕组织的小鼠的瘢痕比例[342]。在植入人类KDs的裸鼠中,病变内TAC显著增加KDs的凋亡[343]。糖皮质激素的药理效力显示出剂量依赖性,在更高的剂量(浓度)下观察到更大的效力,尽管也会引起副作用[342]。KD目前的护理标准是病灶内类固醇,如TAC[6]。在KD瘢痕中,真皮中的前α1(I)I型胶原mRNA水平显著升高。与未经治疗的皮肤相比,KD切除后立即进行病灶内TAC注射可降低前α1(I)胶原转录物。在TA处理的皮肤中,胶原束更薄、密度更低[344]。比较了病变内TAC和VER治疗HTSs和KDs的临床疗效。两种药物在随访3周和1年后都减少了疤痕的血管性、柔韧性、高度和宽度,但没有减少疤痕的色素沉着和长度。TAC的药物不良反应比VER更严重[93]。KD患者采用病灶内TAC治疗,每周1次,疗程4周。最后一次治疗后,与治疗前相比,真皮组织层厚度降至39.0%[345]。评估了病灶内切除术后病灶内TAC注射治疗耳廓KD的临床效果。在24个月的随访期内,复发率为5%,95%的患者身高和体积显著降低。这种低复发率与术后放射治疗相当[346]。使用Antera3D®成像系统评估病变内TAC注射在KD治疗中的疗效,并观察到KD尺寸和症状(如瘙痒和疼痛)的减少,即使治疗具有最小的局部副作用[347]。据报道,手术切除后立即皮下注射TAC,可以安全、持久、经济高效地治疗剖腹产KD疤痕,并预防KD复发[348]。
3.16.2. 地塞米松(DEX)
DEX是一种与人类糖皮质激素受体(GR)结合的合成糖皮质激素,是最有效的抗炎糖皮质激素之一,通过与GR的相互作用诱导KD消退,并抑制原代KD成纤维细胞培养中内源性VEGF表达和成纤维细胞增殖[349]。此外,在疾病组织中长期培养KD的器官中,DEX显著降低了KD的体积和细胞数量,并诱导表皮收缩[350]。将DEX和绿茶多酚(GTP)掺入电纺聚合物超细纤维网中作为共递送系统,在植入人类KD组织的裸鼠中评估KD作为外科敷料的治疗效果。治疗3个月后的组织学分析显示,负载DEX/GTP的纤维网显著诱导KD中胶原纤维的降解[351]。比较了糖皮质激素在氢化可的松、甲基强的松龙、地塞米松、TAC和泼尼松中预防烧伤患者HTSs的有效性。在总体表面积(TBSA)为0–19%的烧伤患者中,甲基强的松龙可降低HTS诊断的风险。在不依赖TBSA的烧伤患者中,甲基泼尼松与HTS诊断降低有关。在20-39%TBSA烧伤或40-100%TBSA烧伤的患者中,泼尼松显示出发生HTS诊断的风险增加。甲基泼尼松与不依赖TBSA的烧伤患者的HTS诊断降低有关。在20-39%TBSA烧伤或40-100%TBSA烧伤的患者中,DEX显示出发展为HTS诊断的风险增加[352]。
3.17. 再生医学(脂肪移植、富含血小板的血浆、脂肪衍生的基质血管部分、脂肪衍生干细胞、间充质干细胞、透明质酸)
伤口愈合是一个复杂的过程,取决于各种类型的细胞、生长因子、细胞因子和ECM元素的存在。组织再生技术通过再表皮化、表皮-基质细胞相互作用、血管生成以及对增生性瘢痕和瘢痕疙瘩的抑制显著增强皮肤修复[353]。涉及的重要细胞包括表皮干细胞、成纤维细胞的真皮前体、脂肪衍生干细胞(ASC)和骨髓细胞。这些细胞的活性受到各种生长因子的严格调节,如表皮生长因子(EGF)、成纤维细胞生长因子(FGF)、PDGF、TGF和IL[354]。这些表明,涉及细胞、组分和生长因子的生物组分与伤口愈合密切相关。在从HTSs培养物中分离的体外原代真皮成纤维细胞中,从培养的4到13天,与富血小板血浆(PRP)共培养的成纤维细胞的TGF-β1mRNA表达显著低于贫血小板血浆(PPP)处理的成纤维纤维细胞。PRP组的结缔组织生长因子(CTGF)水平和mRNA表达低于PPP组[355]。因此,基于自体血小板的浓缩物代表了越来越受欢迎的各种医疗、外科和美容干预的辅助品。它们的有益潜力取决于向靶组织输送高浓度生长因子的能力[356]。此外,血小板是线粒体的重要供体,血小板衍生的线粒体可以通过减少血管内皮细胞氧化应激引起的细胞凋亡来促进伤口愈合[357]。各种再生医学方法的效率不断提高,如富含血小板的血浆、细胞治疗、基质血管部分、外泌体和干细胞条件培养基,其重点是个性化的、针对患者的治疗。据报道,再生医学是一种副作用最小的有效方法,可用于治疗HTSs和KD[3353358359360]。
3.17.1. 脂肪移植
在疤痕治疗中,需要注射脂肪移植物(脂肪组织)。脂肪组织是一种含有间充质干细胞储备的结缔组织,这种治疗可以减轻疼痛并增加疤痕弹性[361362]。脂肪移植加速热损伤小鼠的血运重建并减少纤维化[363]。自体脂肪移植在乳房手术、面部年轻化、隆臀、Romberg综合征以及抽脂后遗症的治疗中有许多临床应用,表明自体脂肪移植是矫正面部疤痕的好方法,而不是传统的疤痕手术切除[362]。脂肪组织可以安全地移植到疤痕中,以改善严重疤痕后的难治性神经性疼痛,如烧伤[3364365366367]。基于这些结果,人们认为用脂肪移植治疗烧伤等严重疤痕可以防止损伤部位KDs和/或HTS[3368369]的诱导。
3.17.2. 富血小板血浆(PRP)
自体PRP是管理皮肤移植供体部位的有效佐剂。PRP可以减少疼痛和瘙痒,并改善皮肤移植供体部位的伤口愈合[370]。当PRP在术中注射给对可的松注射或放疗没有反应的KD患者时,53%的患者的KD疤痕完全消退,29%的患者在2年时完全复发。平均VSS评分从2年时的8.18±2.38提高到3.82±1.98,表明PRP注射作为切除术的辅助治疗是一种有效和安全的方法,用于治疗传统治疗难治的KD疤痕[371]。当用病变内A型肉毒杆菌毒素(BTX-A)、PRP或TAC治疗KD疤痕时,BTX-A和PRP都有机会在KD治疗中获得比传统TAC注射更好的美容效果[372]。然而,也有报道称,从皮肤弹性、鼻唇沟改善或患者满意度来看,PRP显著缩短了术后恢复时间,但并不能改善患者的预后[337]。KDs患者接受病灶内曲安奈德、维拉帕米(VER)、5-氟尿嘧啶(5-FU)或PRP治疗。当通过患者和观察者疤痕评估(POSAS,评估疼痛、瘙痒、色素沉着、硬度、厚度、疤痕平整度、血管形成、柔韧性、缓解等)评分进行评估时,其疗效如下:VER>曲安奈德=PRP>5-FU[374]。
3.17.3. 脂肪来源的基质血管分数(SVF)
脂肪来源的基质血管部分(SVF)和间充质干细胞(MSC)都可以显著降低HTS的临床和组织学参数,尽管MSC在重塑HTS方面比SVF更有效[375]。在接受SVF增强自体脂肪移植物治疗的患者中,1年后观察到63%的轮廓恢复维持,尽管在接受离心脂肪移植物处理的对照组中这一比例仅为39%[362]。在兔耳模型中比较BTX-A和SVF凝胶用于HTS治疗时的疗效,其中BTX-A显示出比SVF凝胶更好的抗瘢痕功效[376]。在裸鼠人源化皮肤移植模型中,比较SVF和人脂肪组织来源的MSC在重塑HTS方面的治疗效果。SVF和MSC都显著降低了治疗小鼠皮肤中的胶原蛋白含量和真皮厚度,但MSC似乎比SVF更有效[375]。在中深度急性烧伤中,与最终进行植皮的对照组相比,用SVF和HyA支架治疗后,病例区域愈合更快。这两个区域都显示出HTS发展的趋势,而患者满意度视觉模拟量表(VAS,疼痛评定量表之一)在病例侧为7,在对照侧为2[377]。KD患者接受SVF或TAC(对照组)治疗。SVF治疗组未观察到不良事件,而TAC治疗组仅观察到一名患者出现溃疡(II级不良事件)。结论是,自体脂肪来源的SVF在中低收入国家用于治疗KD是可行和安全的[378]。
3.17.4. 脂肪来源干细胞(ASC)
干细胞是一种未分化的细胞群体,其特征是具有广泛增殖(自我更新)的能力;它们通常来源于单个细胞(克隆),并分化为不同类型的细胞和组织(强效)[379]。来源于ASCs条件培养基的肽抑制胶原,而HTS成纤维细胞中的ACTA2或平滑肌肌动蛋白(SMA)mRNA通过与丙酮酸羧化酶(PC)蛋白结合促进伤口愈合并减少胶原沉积,丙酮酸羧化蛋白酶抑制小鼠模型中PC蛋白的表达[380]。ASC处理显著提高了KD真皮成纤维细胞中环氧合酶-2(COX-2)mRNA和蛋白的表达,这将在介导ASC条件培养基诱导的细胞凋亡和抗增殖作用中发挥关键作用。在裸鼠模型中,ASC条件培养基注射后翻译的KD组织中花生四烯酸、COX-2和前列腺素E2(PGE2)的表达高于对照[381]。当用ASC外泌体培养KD成纤维细胞时,KD成纤维纤维细胞的增殖率、迁移率、胶原合成水平、α-SMA、TGF-β1和Smad3的相对mRNA和蛋白表达水平降低,凋亡率增加,这取决于ASC外泌物的浓度[382383]。在兔模型中,在伤口愈合过程中将含有人ASC细胞外小泡(0.1mL)的培养基注射到耳朵中形成的伤口中。与单独的培养基相比,该治疗在术后第28天阻止了HTSs的形成,并抑制了胶原沉积和肌成纤维细胞聚集[384]。ASC成为缓解HTS的潜在解决方案[385]。
3.17.5. 间充质干细胞
间充质干细胞分泌多种生长因子和细胞因子,诱导血管生成,减少炎症,促进成纤维细胞迁移和胶原生成[386]。骨髓源性MSCs减弱与KD和HTS成纤维细胞相关的增殖和促纤维化表型,并通过旁分泌信号机制抑制ECM合成[387]。研究最多的MSCs类型是从人类脐带血、脂肪组织和骨髓中分离的MSC[388]。SVF和人脂肪组织来源的MSCs都显著降低HS的临床和组织学参数,并且人MSCs比SVF更有效。MSCs是再生医学中有价值的细胞来源,据报道,从MSCs获得的条件培养基可以抑制炎症。例如,从羊膜来源的MSCs获得的条件培养基显著抑制KD成纤维细胞的增殖,以及TGF-β诱导的KD和正常成纤维细胞中α-SMA和KD成纤维纤维细胞中I型胶原的上调[389]。在KD植入模型中,人MSC条件培养基抑制人KD衍生成纤维细胞的增殖和胶原合成,并减少炎症和纤维化[390]。当通过降低KD体积、症状和1:3型胶原比例以及增加IL-10水平来评估病变内脐带来源MSC(UC-MSC)与KD治疗相关的治疗效果时,病变内注射UC-MSC和UC-MSC条件培养基比病变内TCA更有效[391]。
MSCs的治疗效果归因于TGF-β3和肝细胞生长因子(HGF)的高表达,这是重要的抗纤维化介质,以及基质MMP-2和MMP-2/TIMP-2组织抑制剂比例的高水平,这反映了负责纤维化吸收的重塑活性[375]。来源于人类脂肪MSC的外泌体通过体外和体内实验减弱胶原的沉积、成纤维细胞向肌成纤维细胞的反分化以及HTS的形成[392]。在临床上,骨髓和UC骨髓间充质干细胞都有效地改善了烧伤愈合,如通过HTSs的晚期并发症以及疤痕的色素沉着不足和色素沉着过度所评估的,其中接受常规早期切除和移植物治疗的患者的HTSs复发率为40%,接受骨髓间充体干细胞治疗的患者为15%,接受UC骨髓间质干细胞治疗患者为20%[393]。MSC治疗KDs和HTSs的有效性通过宏观和组织学表现以及免疫组织化学进行评估。在所有使用MSC或MSC条件培养基治疗的病例中观察到结果的改善,没有并发症[394]。应用自体脂肪组织来源的间充质干细胞治疗烧伤后瘢痕。当通过VSS评分进行评估时,手术后6个月,平均VSS评分从治疗前的7.88分(4-11分)降至2.34分(1-4分)[395]。当通过KD体积和症状的减少、1:3型胶原比例和IL-10水平的增加来评估UC-MSC和MSCs条件培养基的临床疗效时,在KD治疗中,病变内注射这些MSCs比TAC更有效[391]。在一篇综述文章中,对MSC条件培养基进行了静脉内、腹膜内、皮下、皮内、病变内或局部测试。MSC条件培养基可改善动物和人类的伤口愈合、毛发恢复、皮肤再生、特应性皮炎和银屑病[396397]。
3.17.6. 透明质酸(HyA)
透明质酸(HyA)是ECM的主要成分之一,是一种由交替的N-乙酰-D-葡糖胺和D-葡糖醛酸部分组成的糖胺聚糖。HyA是结缔组织中普遍存在的成分,在结缔组织中形成基质,并在维持基质结构和水分平衡中发挥重要作用[339]。此外,HyA在调节各种生物过程中发挥着多方面的作用,如皮肤修复、癌症诊断、伤口愈合、组织再生、抗炎作用和免疫调节,HyA已被用作化妆品和营养化妆品的必要成分之一[398]。在组织再生过程中,HyA被认为是关键参与者之一。HyA可以通过特定的HyA受体调节炎症、细胞迁移和血管生成,这是伤口愈合的主要阶段[399]。据报道,通过液体喷射注射给予外源性HyA对皮肤病是一种有益的治疗方法[400]。在一项体外研究中,HyA降低KD成纤维细胞培养物中的增殖活性、I型胶原原表达、TGF-β1表达和TGF-β1-释放[401]。在临床上,HyA与可的松的联合治疗显示KD患者在几个月后完全消退,没有复发[402]。此外,博来霉素(BLM)和HyA的组合允许在没有疼痛的情况下递送BLM,起效快,生物利用度好,并在体外抑制人类HS成纤维细胞的增殖和TGF-β1的分泌[403]。每月接受类固醇注射的多个胸骨KDs患者在第一次注射类固醇的同一天额外注射BTX-A/HyA。当通过VSS和VAS评分进行评估时,微针递送BTX-A/HyA可提高患者满意度[404]。在一篇综述文章中,HyA因其独特的粘弹性、生物相容性、生物降解性、非免疫原性和对皮肤的生物医学益处而被报道为局部和经皮递送的有效载体[405]。
3.18. 曲安奈德与其他药物的临床疗效比较
在兔耳HTS模型中比较病变内TAC、5-FU和BTX-A治疗HTS的临床疗效。与单药治疗相比,TAC和5-FU的疗效相似,但BTX-A对已建立的HTSs无效[406]。比较病灶内TAC和5-FU治疗KDs的临床疗效。5-FU治疗的患者出现副作用,如色素沉着、注射部位疼痛(95%的患者)和浅表溃疡。因此,在KD的治疗中,TAC似乎是5-FU的一种耐受性更好、毒性更小的替代品[407]。相反,在KD患者中,TAC组和5-FU组在6个月时的缓解率没有统计学上的显著差异(分别为60%和46%)。与5-FU组相比,TAC组的局部不良反应(如萎缩和毛细血管扩张)明显更高[408]。比较病变内TAC和VER治疗HTSs和KDs的疗效。VER由于其低成本和较少的不良影响,值得在广泛的抗HTSs药物中得到更好的定位[89]。此外,据报道,在治疗KD/HTS时,与病变内TAC相比,病变内VER成本极低,不良反应较少,因此有几种治疗可能性与TAC替代或同时用于较大(或多个)疤痕[94]。比较病变内TAC(10 mg/mL)和VER(2.5 mg/mL)预防切除后KD复发的疗效,患者每月接受一次(四次)。VER是安全的,但在预防切除后KD复发方面不如TAC有效[409]。同样,将病变内TAC与病变内VER治疗KDs的临床疗效进行比较。与VER[410]相比,TAC在高度和柔韧性方面有了更好的改善。比较TAC和VER治疗KD和HTS的疗效和安全性。在他们之间,身高、血管分布、柔韧性和色素沉着程度的降低没有显著差异。得出的结论是,当TAC导致不良结果时,VER可能被用作替代治疗[91]。比较TAC与5-FU、VER、PRP治疗KD的临床疗效。当通过POSAS评估疗效时,VER是最有效的,PRP与TAC一样有效,没有严重的副作用。5-FU治疗KD的疗效较差[374]。其他报告如下:单独手术切除和术后注射TAC或INT-α2b后KD复发率分别为51.1%(对照组)、58.4%和18.7%,表明术后注射TAC并不能有效减少KD复发次数[411]。比较病变内TAC和BLM治疗KD的临床疗效。当在24周随访时通过POSAS评估疗效时,BLM比TAC更有效[412]。在一篇综述文章中,比较了病变内TAC和BTX-a注射液治疗HTS和KD的疗效。当通过VAS评估时,BTX-A注射比病灶内皮质类固醇或安慰剂注射更有效[413]。比较病灶内TAC和依那普利治疗KD/HTS的临床疗效,并用VSS和POSAS进行评价。TAC和依那普利均显示出相同的临床效果,表明依那普利可能。

3.19. 曲安奈德与其他药物的联合药物治疗
可以认为,如果药物组合在药理学上足够,使用多种药物的联合药物治疗的临床疗效可能优于使用每种药物的单一药物治疗。适当的联合药物治疗可以同时靶向多个受影响的部位,并发挥相加和/或协同的药理作用。对于KD/HTS治疗,有各种联合药物疗法的报道。在本节中,对一些用于KD/HTS治疗的联合药物疗法进行了综述。
3.19.1. 曲安奈德与5-氟尿嘧啶的联合用药
在体外调节KD成纤维细胞中,TAC抑制细胞增殖并诱导G1细胞周期停滞,但不诱导细胞凋亡。在TAC中加入5-FU可改善瘢痕消退并减少KD的复发[417]。这可能表明,多种具有不同药理作用的药物的联合使用可以提高治疗效力。在临床上,经常注射5-FU在疤痕稳定和消退期间是有效的。TAC和5-FU联合应用似乎更有效,疼痛更小。在注射治疗的同时加入脉冲染料激光治疗被发现是最有效的[418]。比较三种方式治疗KDs和HTSs的临床疗效:单独TAC(第1组)、TAC+5-FU联合TAC+5-FU+脉冲染料激光(PDL)(第3组)。TAC+5-FU的总体疗效与TAC+5-FU+PDL相当,但TAC+5-FU+PDL的组合更容易被患者接受,并产生更好的结果[419]。同样,比较了病灶内TAC+5-FU联合TAC单药治疗KDs和HTSs的临床疗效。TAC+5-FU联合用药的总体疗效与单独使用TAC相当,但患者更容易接受该联合用药,并产生更好的效果[420]。另外,另一组比较了病灶内TAC+5-FU与单独病灶内TAC联合治疗KD的临床疗效。TAC+5-FU联合治疗优于病灶内TAC单药治疗[421]。TAC抑制细胞增殖并诱导G1细胞周期停滞。5-FU诱导G2细胞周期停滞和凋亡,并在联合治疗中发挥主要作用,导致更显著的细胞增殖抑制、凋亡、I型胶原(Col-1)抑制和基质MMP-2诱导[417]。在KDs的治疗中,5-FU单药治疗以及MMC、BLM和类固醇注射单药治疗的大多数病例的疤痕改善≥50%。病灶内5-FU+类固醇联合注射产生了统计学上显著的改善。5-FU的单次治疗复发率为0至47%,BLM为0至15%,类固醇注射为0至50%。手术切除和辅助5-FU或类固醇注射的联合治疗显示复发率较低;分别为19%和6%[99]。比较病变内TAC+5-FU、5-FU+VER、依那普利单独、VER单独和部分二氧化碳激光治疗KD的临床疗效。TAC+5-FU联合治疗瘢痕软化程度和平均缩小程度最高,其次为5-FU+VER;然而,其他方式显示出较少的效果,尽管所有这些治疗都能解决KD的疼痛和瘙痒[422]。比较病灶内TAC+5-FU(治疗A)和病灶内TAC+BLM(治疗B)治疗小KD的疗效。与治疗A(30名患者中优良反应50%、良好反应10%、尚可反应10%和不良反应6.66%)相比,治疗B的KD体征和症状得到了更大的改善(30名病人中优良反应76%、良反应10%、可反应6.66%和不良反应66.6%)。此外,B组的VSS评分和复发率具有统计学意义[423]。比较5-FU单独与5-FU+TAC联合治疗KD的临床疗效。5-FU作为单一药物和与TAC联合使用,在减少KD大小方面同样有效,联合用药组减少了副作用[424]。将TAC和5-FU联合治疗HTSs和KDs的疗效和安全性与单独使用TAC和单独使用5-FU的疗效和安全相比较。TAC和5-FU的联合治疗显示出比单独TAC和单独5-FU更高的疗效[425]。在一篇综述文章中,比较了TAC单药治疗和TAC+5-FU联合治疗HTS和KD的疗效和安全性。TAC和5-FU的组合更适合于治疗HTSs和KSs,疤痕高度和患者满意度有更大的改善,副作用更少[426427]。此外,据报道,在KD和HTS的治疗中,病灶内TAC和5-FU联合治疗比TAC单一治疗更有效、更安全[90]。建议TAC+5-FU联合治疗对硅树脂产品、冷冻治疗或单独使用病灶内皮质类固醇无反应的KDs。评估5-FU(50 mg/mL)和TAC混悬液(40 mg/mL)(3:1)联合治疗12个月的客观数据,如疤痕的高度、体积、穿透深度、POSAS和皮肤科生活质量指数(DLQI)。每KD药物混悬液的注射量随着访视时间的延长而减少。本研究的结果证实了5-FU和TAC联合治疗KD的有效性和安全性[428]。在一篇综述文章中,据报道,TAC与疤痕调节剂如5-FU、BLM和BTX-a的组合具有增加的疗效和更少或类似的不良事件。特别是,TAC和5-FU的组合在所有支持其用于HTS和KD治疗的组合中显示出最强和最一致的证据[429]。
3.19.2. 曲安奈德与维拉帕米的联合用药
在背部植入人HST片段的裸鼠中,比较钙通道阻滞剂(VER)、类固醇和INF联合方案治疗HTSs的疗效与类固醇单一疗法的疗效。联合方案治疗小鼠的HTS成纤维细胞数量在第10天显著减少,如下所示:(无药物)16.6×105;(单用类固醇)1.5×105;×105(p<0.05)。此外,成纤维细胞聚集的胶原晶格(FPCL)在4周时的收缩率如下:(无药物)15.4%;(单独使用类固醇)65%;和(联合方案)分别为原始大小的73.4%(p<0.05)[430]。比较TAC单独、VER单独及TAC与VER联合治疗KDs的临床疗效。与VER相比,TAC表现出更显著和更快的改善,但这与更高的不良反应率有关。两种药物的组合可以增强其机制,而不会产生不必要的副作用[431]。羟丙基β-环糊精(HP-β-CD)微针中TAC和VER的组合显著降低了HTSs的厚度,以及HTSs中羟脯氨酸(HYP)和TGF-β1的表达,并改善了胶原纤维的排列,减少了真皮充血和增生[432]。在KD患者中比较病变内单独使用曲安奈德和曲安奈德与VER联合使用的临床疗效。两组都显示出显著的改善,但联合用药组的皮肤发红消退更快,所需疗程更少[433]。
3.19.3. 曲安奈德与其他药物(博莱霉素、肉毒杆菌毒素A、干扰素、戊酮可可碱、富含血小板的血浆)的组合
使用TAC(4 mg)和BLM(0.375 IU)联合治疗1 cm2疤痕表面是治疗KDs和HTSs的可接受程序[434]。比较BLM纹身和冷冻治疗结合病灶内TAC注射治疗KDs和HTSs的临床疗效,其中冷冻治疗和病灶内TAC注射联合治疗是HTSs和KDs最常见的传统治疗方法。结论是,在治疗较大的KDs和HTSs(尺寸>100 mm2)方面,BLM纹身可能比冷冻治疗结合病灶内TAC注射更有效[435]。另外,评估了TAC和BLM联合应用治疗难治性KD和HTS的疗效。联合应用有效地治愈了KDs和HTSs。尽管治疗后大KDs显示局部复发,但随着进一步治疗,复发消失[436]。检查了用于治疗难治性KD的病变内TAC(13.3 mg/mL)和病变内BLM(1单位/mL)混合物的临床疗效。这种组合为对传统疗法反应不佳的个体提供了一种很有前途的治疗选择,其中良好反应为78.8%,尚可反应为21.2%,不良反应(<25%的平坦化)为0%。观察到溃疡、色素沉着、色素沉着不足、继发感染和毛细血管扩张等副作用[437]。在耳KD的治疗中,先进行手术刮除,然后进行病变内TAC和肉毒杆菌毒素A,96-100%的患者表示满意(满意和非常满意)[438]。TAC(1μg/mL)或IFN-γ(1.000–10.000 IU/mL)单药治疗2天,在体外诱导正常健康和KD成纤维细胞的增殖潜力严重降低。TAC和IFN-γ的组合对KD成纤维细胞中I型胶原的合成表现出更强的抑制[439]。比较病变内TAC和PRP联合治疗(治疗A)和单独TAC(治疗B)在KD治疗中的疗效。治疗A的美容效果更好,TAC诱导的副作用发生率更低,尤其是萎缩和色素沉着不足[440]。在用PRP治疗各种疤痕的过程中,当单独使用PRP时,中度改善是最常见的(36%)结果。相反,当病变内PRP与激光或微针相结合时,大多数患者的结果显著(分别为33%和43%)或良好(分别为32%和23%)[441]。与单独注射TAC相比,在TAC注射后1周接受病变内PRP的患者的身高、色素沉着、柔韧性和总体VSS评分显著改善(病变内TAC 20 mg/mL,4次,间隔3周)[440]。在治疗KD瘢痕方面,比较了单独病灶内PTF、单独病灶内TAC以及TAC和PTF联合治疗的疗效和安全性。TAC和PTF的联合治疗KD的效果明显更好,并降低了TAC诱导的副作用风险,其中PTF单药治疗的疗效低于病灶内TAC[292]。一般来说,联合药物治疗显示出更大的临床疗效和更少的副作用。在综述文章中,阐述了联合药物治疗的疗效。使用各种数据库分析了不同注射和局部治疗策略对HTSs和KDs的疗效。表面在累积排名(SUCRA)曲线下预测的疗效顺序为:TAC+BTX-A(82.2%)>TAC+5-FU(69.8%)>BTX-A的67.3%>5-FU+硅胶(59.4%)>TAC+硅胶(58.3%)>5-FU(49.8%)>BLM(42.0%)>TAC(26.7%)>VER(26.2%)>硅胶(18.3%)。作者建议病灶内注射TAC+BTX-a和TAC+5-FU的联合治疗[442]。另外,据报道,病灶内TAC+BTX-A注射液联合治疗KD和HTS最有效,如下:TAC+BTA>TAC+5-FU>VER,BLM>BTX-A,TAC,5-FU[443]。
3.20. 药物治疗与物理治疗相结合
为了治疗KD/HTS疤痕,可以使用物理疗法,如冷冻疗法、激光疗法、放射治疗(包括近距离放射治疗)和硅胶/薄片。这些物理疗法本身对治疗KD和HTS是有效的。此外,药物治疗有时与物理治疗相结合,无论是否进行手术切除,以提高治疗KD/HTS的临床疗效[6,7,8,9444]。
3.20.1. 药物治疗结合手术切除和冷冻治疗
在KD/HTS中病灶内注射液氮可以冷冻和坏死疤痕的小区域[445]。这种疗法只有两个小缺点:不能进行组织学控制,并且必须通过局部给药抗生素来保护非出血性人工坏死2-3周。据报道,在治疗良性表皮色素沉着病变方面,液氮冷冻治疗优于氩冷冻治疗和CO2激光治疗[446]。另外,使用氩气系统进行冷冻治疗被证明对KD有效,体积减少,复发率低[447]。与液氮装置相比,氩气装置在体内显示出较低的末端温度和较快的冷冻速率,但在治疗后与液氮装置相比较,导致更多的色素沉着不足[428]。冷冻治疗KD在体积减少和减轻疼痛和瘙痒方面显示出良好的效果。然而,尚未确定完全的疤痕根除,并观察到复发[448]。与单独冷冻治疗相比,病灶内冷冻治疗和术后硅胶片的联合使用在硬度、疼痛和不适方面显示出更好的效果[449]。局部病灶内冷冻疗法的治疗,在病灶内KD切除后和伤口闭合前立即在术中对皮瓣内侧应用液氮,显示出良好的美学和症状效果[450]。液氮病灶内冷冻治疗对耐药KD的疗效不如KD切除后近距离放疗。在原发性KD中,病灶内冷冻治疗降低了KD体积。因此,它可以用于KD患者和特定病例[445]。使用浅表冷冻疗法、部分激光和病灶内TAC注射的联合KD治疗比单独单一疗法更安全、更有效[451]。间隔一个月进行三次冷冻治疗,两次冷冻-解冻周期为30–40 s冷冻时间和两分钟解冻时间,结果KD完全平坦,5年后无复发[452]。
病灶内冷冻治疗结合病灶内TAC治疗非耳廓KD可能产生最有希望的结果。据报道,这应被视为一线治疗[453]。其他研究小组报告称,喷雾型(−79°C)冷冻疗法作为单一疗法无效,应与病灶内皮质类固醇或BTX-a联合使用,以获得治疗厚KD的良好结果[454]。
3.20.2. 药物治疗结合手术切除和激光治疗
使用585 nm闪光灯泵浦的脉冲染料激光(PDL)的治疗效果与单独使用病灶内5-FU以及皮质类固醇和5-FU联合使用的疗效相当[455]。比较单独TAC(第1组)、TAC+5-FU(第2组)、以及TAC+5-FU和585nm闪光灯泵浦的脉冲染料激光器(第3组)的效率。第2组的总体疗效与第3组相当,但第3组的组合更容易被患者接受,并产生更好的结果[419]。部分消融激光在皮肤的不同深度产生消融区,增强物质的透皮递送。HTSs患者的部分激光和术后立即给予皮质类固醇的组合导致平均总体改善[456]。使用2940nm消融性部分铒激光器,在透明膜敷料的遮挡下局部施用倍他米松乳膏,每天两次。改善的中位百分比为50%。平均随访8个月,复发率为22%[457]。研究了分级CO2激光和激光辅助药物递送与局部TAC软膏联合治疗KD。该治疗在治疗后22个月显示出良好的美容效果[458]。激光辅助给药(LADD)通常使用消融分数激光器(CO2或铒:YAG激光器),因为它们能够产生微观消融通道。LADD是一种很有前途的技术,可以增强局部分子的吸收,如皮质类固醇、光敏剂和免疫疗法药物(咪喹莫特或5-FU),同时增加激光的协同作用[459]。最广泛使用的激光器是脉冲染料激光器(PDL)和分数激光器。据报道,理想情况下,所有希望接受增生性和萎缩性瘢痕治疗的患者都应考虑使用局部和病灶内药物以及脉冲染料激光和部分激光的联合方法。KD疤痕往往对标准治疗具有耐药性,因此应考虑其他方式[460]。部分CO2激光和病灶内维拉帕米与病灶内曲安奈德治疗KDs一样有效,尽管与曲安奈德相比,激光和维拉帕米的作用时间更长[461]。激光辅助5-FU局部给药往往显示出比激光辅助局部给药盐酸维拉帕米更高的疗效,但没有显著性,激光治疗后TGF-β1的表达显著降低[462463]。BTX-A是一种很有前途的治疗HTS和KDs的方法,与部分CO2激光相结合可以提高BTX-A在HTS治疗中的疗效[446]。发现CO2 10600 nm和E:YAG 2940 nm的部分消融激光在红斑、高度和柔韧性方面产生了最佳结果,而闪光灯泵浦的脉冲染料激光(PDL)585 nm的得分略低于此[465]。分数CO2和Nd-YAG激光器的组合具有协同效应,在KD的管理中最有效,其中分数CO2比Nd-YAG更有效,Nd-YAG最无效[466]。在PRP的情况下,与PRP单一疗法相比,PRP与另一种药物或物理疗法的联合治疗似乎更有效。在治疗烧伤衍生的HTSs中,PRP是消融部分CO2激光器的有效辅助手段,PRP和消融部分CO2激光的组合被证明比单独的消融部分二氧化碳激光器更有用[467]。在KD患者中评估了分数CO2激光与分数CO2激光联合TAC或三氯乙酸的临床疗效。由于CO2激光和TAC的结合,观察到VSS评分和KD疤痕厚度显著而有效地降低[448]。将部分CO2激光和局部TAC联合治疗KD的疗效(a组)与病灶内TAC单药治疗(B组)进行比较。63.6%和72.7%的患者的KDs完全消退,A组和B组1年的复发率分别为9.1%和18.2%[468]。比较冷冻治疗与病灶内皮质类固醇联合治疗和部分CO2激光联合局部皮质类固醇治疗KDs的疗效。两种方案均表现出良好的疗效,复发率最低;然而,第二种方案在美学上优于治疗[469]。与单独注射TAC相比,脉冲染料激光和TAC联合治疗术后复发的KD缩短了相对治愈时间,减少了TAC注射次数,提高了临床疗效[470]。
3.20.3. 药物治疗结合手术切除和放射治疗
放射治疗是可用于KDs的治疗方法之一,经过几十年的临床实践,放射治疗技术已从表面X射线发展到近距离放射治疗[471472]。切除术后的外照射,通常与其他治疗相结合,复发率低于10%。各种激光已被用于治疗KD,其复发率具有很大的可变性,但总的来说,复发率与传统手术相似。与冷冻破坏一样,当与其他治疗相结合时,激光消融复发率通常会提高[473]。在>10 Gy的放射治疗后,KDs的复发率随着放射治疗方案的生物有效剂量(BED)的变化而降低,而BED值>30 Gy时,复发率<10%。放射治疗应在手术后2天内进行[474]。单独切除(n=28)、切除后外束放疗(EBR)和间质高剂量率近距离放射治疗后KD的复发率分别为44%、19%和23%[475]。手术后最长7小时进行铱192近距离放射治疗时,复发率为23.6%。一个研究组报告称,在1×6 Gy+2×4 Gy后,38例中只有1例复发,而在3×6 Gy后没有复发。另一个研究小组报告称,生物等效剂量>60(5个部分为20 Gy)的治疗比低剂量方案产生了更好的局部控制。据报道,联合治疗——尤其是手术切除和术后放疗——是预防复发的最佳方法。切除耐药KD后,建议采用生物等效剂量约20 Gy的高剂量率近距离放射治疗,总的完全复发率为8.3%。据报道,联合治疗,尤其是手术切除和术后放疗,是预防复发的最佳方法[476]。在1年随访中,完全切除、植皮、术中一次性注射曲安奈德、立即放疗和持续加压治疗的成功率为87.5%[477]。病灶内注射TAC和5-FU可以有效地减少小的和年轻的KDs的厚度并改变其硬度。在三次病灶内注射TAC和5-FU后,锶-90近距离放疗与TAC和5-氟尿嘧啶的联合治疗可以有效地将小规模KD复发率从65.7%(无近距离放疗)降低到44.4%[478]。近距离放射治疗和电子束放射治疗是治疗的黄金标准,因为近距离放射疗法提供的放射治疗更侧重于局灶组织,以显著降低复发率并更好地保护正常组织[471]。在有效治疗耳廓KD的基础上,个体化手术结合术后早期放疗和TAC注射是一种理想的治疗方法,可以确保良好的耳廓外观,同时降低并发症和复发的发生率[479]。
3.20.4. 药物治疗结合手术切除和硅胶/片材
在KD/HTS处理中,比较了硅胶填充垫和硅胶片材对硅胶的处理效果。垫子和挡板都是有效的[480]。据报道,硅树脂产品,如片材和凝胶,被推荐为预防和治疗疤痕的金标准、一线、非侵入性选择。硅弹性体片材是一种有吸引力的治疗选择,因为它易于使用,不良反应风险低[481]。在KDs/HTS[482]的治疗中,硅胶片材在统计学上显著减少了疤痕厚度并改善了颜色。施用4.5个月后,当比较硅胶和非硅胶敷料组之间的瘢痕大小、硬结和KDs/HTSs症状时,两个治疗组之间没有显著差异,并且两种敷料在治疗KDs和HTSs方面同样有效[483]。硅凝胶片材的应用显著提高了HTS的平均基线表面温度[484]。硅酮材料,如硅酮封闭片材和硅酮凝胶片材,可以防止HTS和KD的形成。关于硅胶治疗的作用,人们认为疤痕部位的闭塞会导致伤口床的水合作用和疤痕相关细胞过度活动的抑制[454886]。此外,由于皮肤角膜层的水合作用以及细胞因子介导的成纤维细胞和角质形成细胞之间的细胞信号调节,这种物理疗法可以改善疤痕的颜色、大小、红斑、柔韧性、疼痛和瘙痒[482]。特别是,早期应用硅胶片可显著改善术后瘢痕形成的预防[487]。评价了局部使用硅胶和局部使用甲基强的松龙乳膏预防Pfannenstiel切口后HTS和KD形成的临床疗效。所有组(对照组、硅酮组和甲基强的松龙组)的身高、色素沉着、血管性、柔韧性和总修饰VSS得分均显著降低。甲基强的松龙组患者满意度较高[488]。
3.21. KD/HTS瘢痕手术切除后复发的预防
KDs的增长会随着时间的推移而持续,预计不会出现自发回归,这与HTS[25]的情况不同(表1)。为了彻底治疗KD疤痕,手术切除可能是必不可少的。然而,在没有预防性治疗的情况下进行KDs手术切除后,KDs的复发率相当高,为50-100%[26,24744]。当比较单独切除(对照组)和术后注射TAC或IFN-α2b的KDs复发率时,对照组的复发率为51.1%,TAC组为58.4%,IFN-α2b组为18.7%,表明TAC不能抑制复发率[411]。相反,其他研究人员报告称,病灶内注射IFN-α2b后KD的复发率为54%,病灶内曲安奈德后复发率为15%。作者得出结论,IFN-α2b在KD的临床治疗中似乎无效[489]。据报道,局部应用MMC可将头颈部KD的术后复发率降至10%(十分之一的患者)[444]。局部咪喹莫特也被用于预防手术切除后KD的复发。剃过胡子的KDs每晚用5%咪喹莫特乳膏或载体乳膏治疗两周,在闭塞状态下每周治疗三次,持续一个月。6个月时,咪喹莫特组的KD复发率为37.5%(3/8),赋形剂组为75%(3/4)(p=0.54)[490]。研究了猪明胶-葡聚糖水凝胶支架的注射对预防或减少耳KDs手术切除后KD疤痕复发的作用。术后1年复发率为51.2%。相反,与水凝胶支架相关的复发率为19.2%,在统计学上优于文献中给出的历史复发率(50-100%)[26]。每个受试者切除一个KD,每个伤口被半随机化,每月间隔(四次)接受TAC(10 mg/mL)或VER(2.5 mg/mL)的病灶内注射。数据分析显示,术后12个月,与TAC相比,VER的KD复发率明显更高[409]。局部MMC组KD手术切除后的复发率为16.5%,5%咪喹莫特乳膏组为24.7%,表明局部MMC和咪喹莫特都是预防KD复发的有效替代品[491]。在患有KD疤痕的孕妇中,评估手术切除旧的剖腹产KD疤痕后立即注射TAC和TAC对疤痕复发的影响。接收的患者
笔记在婴儿分娩后伤口闭合时进行外科切除和皮下注射TAC。结论是,当用于剖腹产KD疤痕的治疗时,这种联合治疗将是安全、持久和成本效益高的[348]。评估复发性耳廓KDs患者手术切除并围手术期注射TAC后的复发率。在13个月(平均)随访期间,复发率为9.6%[492]。与其他组(单独病灶内TAC注射、术中/术后TAC注射联合手术切除)相比,联合用药(术中/手术后TAC+术中PRP注射联合手术摘除)的5年复发率显著降低。结论是,就低复发和不良反应而言,这种联合治疗(手术切除+TAC+PRP)对耳KDs患者是一种非常成功的多模式治疗[493]。关于用病灶内TAC和5-FU治疗KDs和HTSs的瘢痕复发率,当随访期约为11个月(1-24个月)时,报告的复发率为7.5-23.3%。然而,相比之下,六项使用不同病变内联合方案的研究报告称,在随访期内复发率为0%(TAC+5FU、TAC+BTX-A、TAC+BLM、TAC+冷冻治疗)。研究中缺乏一致的复发率报告方法,需要长期随访(18-24个月)来确定使用各种病变内药物治疗病理性瘢痕的复发特征[494]。为了防止KDs复发,手术切除、压迫治疗、硅敷料、皮质类固醇注射、放射治疗、冷冻治疗、INF治疗和激光治疗均单独或联合使用。尽管有广泛的可用治疗方法,但复发率通常保持在50-70%的范围内[444]。评估了硅胶和局部维甲酸乳膏预防手术切除后HTSs和KDs的有效性。这两种治疗方法都有效地防止了HTS/KD的复发,并改善了手术后的疤痕[495]。评估了含有洋葱提取物和芦荟的硅胶与硅胶片相比预防术后HTSs和KDs的能力的功效。经过12周的随访,两组的瘢痕形成发生率没有统计学上的显著差异,这表明两种治疗方法在术后瘢痕预防方面与硅胶片一样有效[262]。评估了手术切除结合病灶内PRP和术后办公室浅表放射治疗预防KD瘢痕患者复发的疗效。这种联合治疗在1-3个月的随访中实现了95.5%的无复发率[496]。总复发率在手术切除后以15Gy照射治疗时为29.3%,2003年后以10、15或20Gy的总剂量电子束照射治疗时的总复发率为14.0%,具体取决于部位。有人建议,复发风险高的KDs和顽固性HTSs应在4天内分四次接受20 Gy治疗,耳垂应在2天内分两次接受10 Gy治疗[497]。在接受正中胸骨切开术的患者中,从手术后2周开始,将硅胶片直接放在手术切口上24小时,然后每4周用新的硅胶片重复一次,持续24周。在24周的研究中,甚至在24周后,没有一名患者出现任何主观症状加重[498]。采用手术切除、PRP和冷冻手术三重联合治疗耳廓KD。这种联合疗法治疗耳廓KD有效,复发率低,美容效果良好[499]。
首选
4.讨论
在这篇文章中,首先,我们试图评估使用单一药物的单一药物治疗KD/HTS的临床疗效或有效性的排序。然而,整理每种单一疗法并不容易,或者几乎不可能,因为每种单一治疗的临床疗效并不一致,而是根据不同的研究人员而有所不同。与体外研究的情况不同,患者体内的临床条件差异很大。一般来说,药物的药理作用至少在体外条件下是剂量依赖性的,这表明它们只有在适当的浓度下才能表现出适当的药理作用。在较低的浓度下,每种药物都不会发挥有效的药理作用,在较高的浓度下会引起不必要的副作用。在体内临床情况下,很难确定在KD/HTS疤痕组织中应用的每种药物的适当浓度。此外,许多其他因素,如患者之间症状的变化、药物治疗的开始时间、药物的剂量和给药配方、治疗频率、治疗周期、治疗技术,如病灶内注射和/或局部应用、药物疗效评估的时间和疗效评估(症状)的方法(例如,疤痕的大小、疼痛/瘙痒、患者的满意度),也极大地影响临床疗效的评估。在本节中,将讨论一些因素。
4.1. 药物治疗开始时间的影响
比较术后注射TAC和使用INF-α2b治疗的切除KDs的复发率。术后在KD切除部位注射INF-α2b提供了比KD切除更高的治疗优势,尽管术后TAC注射并没有减少KD复发的次数[411]。比较局部硅胶和甲基强的松龙乳膏在Pfannenstiel切口后第3个月和第6个月预防HTS和KD形成的效果。在术后早期(第3个月)新鲜伤口局部使用甲基强的松龙乳膏似乎是有希望的。两种治疗的患者均未出现副作用,甲基强的松龙组的患者满意度更高[488]。比较早期(损伤后≤6个月)和静止期(损伤后>6个月的)病灶内TAC注射的疗效。TAC治疗改善了高温超导/KD瘢痕的颜色、厚度、柔软度、血管分布和硬度。TAC治疗的疗效在病理性瘢痕形成的静态阶段比在早期阶段更好[500]。在一项系统综述中,据报道,TAC可能有益于HTS和KD的短期治疗;然而,5-FU、TAC+5-FU和VER在中长期治疗中可能产生优越的结果[501]。在评估包括联合药物治疗在内的每种药物治疗的临床疗效时,药物治疗的开始时间和评估时间非常重要。4.2. 剂量和剂型的影响
评价TAC病灶内注射治疗KD的临床疗效。病灶内TAC注射产生了良好的效果,7.5 mg/cm2的TAC剂量比15 mg/cm2的剂量显示出更好的疗效[104]。在兔耳HTS模型中,在创伤后第15、20和25天用低、中或高剂量的病灶内辛伐他汀、洛伐他汀或普伐他汀进行治疗。低剂量(40μM)辛伐他汀、洛伐他汀和普伐他汀分别显著降低疤痕升高21.9%、25.8%和22.8%,低剂量辛伐他汀也促进了CTGF表达的显著降低。相反,中剂量(120μM)和高剂量(400μM)他汀类药物组没有显著改变瘢痕升高[331]。使用三种不同的TAC软膏(TA-A,一种品牌制剂,以及TA-B和TA-C,两种仿制药),比较了一些物理化学性质,如内聚性、铺展性、TAC结晶的产生、油/水含量和粘弹性。据报道,添加剂类型和含量的差异导致了单个软膏理化性质的差异[502]。可以推测,三种不同TAC软膏的理化性质的差异也导致了它们之间临床疗效的差异。使用来自兔耳的HTS瘢痕组织在体外检测TAC脂质纳米颗粒(尺寸为232.2±8.2nm的TAC-LNP)在瘢痕组织中的经皮渗透性。TAA-LNPs对瘢痕组织的渗透性分别是普通脂质体和商业悬浮液的2倍和40倍[503]。疤痕组织中每种药物的浓度可能因不同的临床情况而异,尽管每种药物都有发挥适当药理作用的最佳浓度。
4.3. 临床疗效评价方法的效果
在治疗KD瘢痕方面,将病变内TAC(4mg/cm2或0.1mL/cm2的TAC 40mg/mL,3周间隔)与5-FU(10mg/cm2或0.2mL/cm2的5-FU 50mg/mL,三周间隔)的临床疗效进行比较。5-FU治疗KD瘢痕更为有效。TAC组的患者满意度评分较高,但5-FU组的VSS评分和VAS评分较好[504]。当比较BTX-A和5-FU在KD治疗中的临床疗效时,BTX-A实现了极好的病变平坦化,远优于5-FU。在BTX-A组中,与中型和大型病变相比,小型病变的临床反应没有统计学上的显著差异,尽管在5-FU治疗中,小型和中型病变的反应明显好于大型病变[219]。比较TAC单用、VER单用及TAC与VER联合治疗KD的临床疗效。与VER相比,TAC产生了更显著和更快的改善,但与更高的不良反应率有关。两种药物的组合可以增强每种药物的作用机制,而不会产生不必要的副作用[431]。不同药物的主要药理作用不同。
4.4. 临床疗效评估时机的影响
比较了病变内TAC和VER治疗HTSs和KDs的临床疗效。两种药物在随访3周和1年后都减少了疤痕的血管性、柔韧性、高度和宽度,但没有减少疤痕的色素沉着和长度。TAC的药物不良反应比VER更常见[93]。评估病灶内BLM治疗KDs的临床疗效。完全扁平化的发生率为70.8%,高度显著扁平化发生率为8.3%,其中局部副作用包括疼痛(100%)、水泡(78.3%)、溃疡(5.8%)和色素沉着过度(56.7%)。最后一次治疗后6、12、15和18个月,KDs的复发率分别为3.8、15.4、45.5和50%[104]。在一篇综述文章中,据报道,在治疗KDs和HTSs时,TAC在9周内改善血管系统方面比VER更有效。此外,TAC在18周内产生了与改善柔韧性相关的优越结果,而VER在治疗的18至24周内产生优越结果[92]。据报道,各研究缺乏一致的复发率报告模式,需要长期随访(18-24个月)来确定使用各种病变内药物治疗病理性瘢痕的复发特征[494]。据报道,临床疗效的评估因评估时间的不同而有很大差异。理想情况下,需要完全治愈KD/HTS疤痕。
4.5. 处理技术的效果
使用注射器在病灶内多次注射治疗药物是KDs和HTSs最广泛使用和最有效的治疗方法之一,因为它能够以指定的剂量/浓度将治疗药物递送到靶位点。然而,使用针头进行病灶内注射的疗效在很大程度上取决于注射的医疗专业人员的技能[505]。病灶内注射给病人带来疼痛。已经开发了各种治疗药物的给药方法,包括增强透皮给药,以实现减少疼痛的靶向给药,如下所示:使用电动注射器共同注射利多卡因[506],局部施用利多卡因[507508],使用冷冻麻醉[509],使用无针气动喷射注射[120],微针贴片[510]等。药物的透皮离子电渗给药不会引起任何疼痛,皮质类固醇等难溶性化合物的剂量配方可以修改如下:使用有机溶剂和水的混合物[511],使用纳米结构脂质载体作为载体[512],使用固体脂质纳米颗粒水凝胶[513]。此外,凝胶制剂中皮质类固醇的透皮给药也被报道用于声传导和超声给药[514]。另外,通过将患者分为两组:边缘内切除组和边缘外切除组,研究了手术切缘对HTSs复发的影响。所有接受边缘内切除治疗的患者(15/15)在6个月内出现HTS复发。9名患者中有3名(33.3%)在切除3–5 mm的HTSs时出现复发[514]。有效的裕度对于防止HTSs的再次发生是必要的。
5.结论
我们综述了药物治疗在治疗和/或预防KDs/HTSs术后复发方面的应用。KDs和HTSs都是血管化和细胞化增加的隆起和色素性疤痕,这些疤痕是由于过度产生纤维化增强细胞因子(如TGF-β1/β2)和ECM(如胶原蛋白)而形成的。这些疤痕会引起疼痛、瘙痒、挛缩、不适等,大大降低患者的生活质量。因此,临床上有用的药物可以抑制成纤维细胞的增殖、TGF-β和ECMs(主要是胶原蛋白)的产生和/或功能、血管形成和/或疼痛和瘙痒(表2)。为了提高药物治疗KDs/HTSs的临床疗效,根据患者的症状(如疤痕的大小和部位)、给药因素(如剂量、给药频率和周期、配方、伤口给药时间以及局部和/或病灶内注射的给药技术)以及症状评估方法(包括时间)适当选择药物将非常重要。一般来说,与单一药物治疗相比,联合药物治疗在治疗和/或预防KDs/HTSs复发方面要有效得多。联合治疗的更大疗效是由于其同时对受影响部位进行多个靶向治疗。通过使用组合药物治疗,包括适当的物理治疗,可以预期具有较少副作用的附加和/或协同药物作用。目前,KDs和HTSs仍然是棘手的疾病。然而,在开发更安全、更有效的KDs和HTSs药物疗法时,有关各种药物、其在患者中的使用方法、临床结果以及评估方法的信息将是有价值的。
本信息并非旨在或暗示作为专业医疗建议的替代;不应在任何医疗紧急情况下使用,也不应用于
任何医疗状况的诊断或治疗。所有医疗紧急情况请拨打120。




