
作者:Chin-An Chen,1,2,# Yi-Chen Huang,3,# Jing-Jou Lo,4 Shih-Hung Wang,3 Shu-Hung Huang,5,6,7 and Sheng-Hua Wu1,2,8,
1Department of Anesthesiology, Kaohsiung Municipal Ta-Tung Hospital, Kaohsiung, Taiwan.
2Department of Anesthesiology, Kaohsiung Medical University Hospital, Kaohsiung, Kaohsiung Medical University, Taiwan.
3School of Medicine, College of Medicine, Kaohsiung Medical University, Kaohsiung, Taiwan.
4Department of General Medicine, Kaohsiung Medical University Hospital, Kaohsiung Medical University, Kaohsiung, Taiwan.
5Division of Plastic Surgery, Department of Surgery, Kaohsiung Medical University Hospital, Kaohsiung Medical University, Kaohsiung, Taiwan.
6Department of Surgery, School of Medicine, College of Medicine, Kaohsiung Medical University, Kaohsiung, Taiwan.
7Hyperbaric Oxygen Therapy Center, Kaohsiung Medical University Hospital, Kaohsiung Medical University, Kaohsiung, Taiwan.
8Department of Anesthesiology, School of Medicine, College of Medicine, Kaohsiung Medical University, Kaohsiung, Taiwan.
摘要
背景:脊髓腹角神经元凋亡和炎症导致烧伤后失神经肌肉萎缩。高压氧疗法(HBOT)具有抗炎和神经保护作用。此外,缺氧诱导因子(HIF)-1α已被报道可促进炎症和细胞凋亡。我们研究了HBOT的治疗潜力和HIF-1α在烧伤后的作用。
方法:将Sprague-Dawley大鼠分为三组:对照组、未经治疗的烧伤组接受烧伤和假治疗,以及接受烧伤和HBOT治疗的HBOT组。右后爪在75℃±5℃下烧伤。在烧伤后第28天开始HBOT(2.5大气压下100%氧气,90分钟/天)和假HBOT(1大气压下21%氧气,90分/天),并持续14次治疗(第28-41天)。在烧伤前和烧伤后每周进行丧失能力(后肢负重)测试。在烧伤后第42天,分析腓肠肌和脊髓腹角。
结果:HBOT改善了烧伤引起的负重失衡。在烧伤后第42天,HBOT组的腓肠肌萎缩和纤维化程度低于未治疗的烧伤组。在腹角,HBOT减轻了烧伤后的神经元凋亡和胶质细胞活化。HBOT后,烧伤后磷酸化AKT/mTOR的增加减少。如免疫荧光和蛋白质印迹所示,HBOT还抑制了HIF-1α信号传导。
结论:HBOT可能通过HIF-1α信号传导减少烧伤诱导的腹角神经元凋亡。
关键词:烧伤、高压氧治疗、神经元凋亡、失能性肌肉萎缩、缺氧诱导因子-1α
骨骼肌萎缩是烧伤后的常见特征,可能持续数月至1-5年。它通常与多种并发症和康复受损有关。然而,有限的研究已经调查了潜在的分子机制,并且缺乏减轻烧伤后长期肌肉萎缩的有效策略。烧伤可导致肌肉中蛋白质过度降解,我们之前的研究表明,脊髓腹角中的神经元凋亡导致失神经腓肠肌萎缩。烧伤后的神经炎症也会增加远处肌肉质量的损失。
高压氧治疗(HBOT)涉及患者在1.5至3.0个标准大气压下呼吸100%氧气,平均持续时间为90分钟。它通常用于治疗减压病、一氧化碳中毒和问题伤口等病症。HBOT通过改善实验性诱导的骨骼肌损伤和结肠炎模型中的组织缺氧来减轻炎症和氧化反应。此外,HBOT的神经保护作用可减少认知障碍。Mu等人报道,延迟HBOT(缺血性脑损伤后48小时开始)可增加再生细胞增殖。数据越来越多地支持HBOT的益处,包括神经元凋亡抑制、神经炎症减少和抗氧化能力。Dave等人指出,在运动神经元疾病的小鼠模型中,HBOT可以预防线粒体功能障碍。基于这些证据,我们认为HBOT对减轻烧伤后脊髓腹角神经元凋亡和炎症具有潜在的治疗作用。
先前的研究表明,HBOT通过抑制缺血伤口模型22中缺氧诱导因子-1α(HIF-1α)的过表达来改善伤口愈合。Nakazawa等人报道,烧伤诱导小鼠骨骼肌线粒体功能障碍和HIF-1α通路激活。HIF-1α通路在几种中枢神经系统(CNS)疾病中也起着关键作用;然而,HIF-1α在中枢神经系统损伤中的作用仍然存在争议。上调HIF-1α表达促进了创伤性脑损伤2脑缺血和脊髓损伤大鼠模型中的程序性神经元死亡。此外,在常氧条件下,炎症刺激是HIF的强效激活剂,靶向HIF活性是炎症性疾病组织修复的潜在策略。HIF-1α信号轴也与脑缺血期间异常神经胶质炎症的激活和神经元细胞死亡有关。Guo等人指出,HIF-1α轴的激活增强了创伤性脑损伤中间充质细胞的迁移,减少了神经元的凋亡。上调HIF-1α信号通路的方法以及表达HIF-1α36的重组腺病毒的给药也被提出用于减轻脑缺血损伤中的神经元凋亡。在本研究中,我们调查了HBOT是否通过在烧伤诱导的失神经中靶向HIF-1α信号传导来发挥神经保护作用
材料和方法
动物与实验设计
该实验已获得高雄医科大学机构动物护理和使用委员会的批准(IACUC批准号:109045)。将18只成年雄性Sprague-Dawley大鼠(体重150-175g)(BioLASCO台湾有限公司)随机分为三组,每组6只。根据之前的研究,群体规模通常足以检测动物37、38的显著生物效应。对照组接受假烧伤和假治疗。未经治疗的烧伤组接受烧伤和假HBOT治疗。HBOT组接受烧伤和每日HBOT治疗2周。图1A1A显示了实验设计的时间线。如前7所述,在第0天造成烧伤。伤口每天用磺胺嘧啶银软膏护理,直到伤口愈合,大约在受伤后3-4周。将HBOT组的大鼠置于高压室(Genmall Biotechnology Co.,有限公司,台湾)中,并在烧伤后第28至41天接受HBOT(100%氧气,2.5 ATA,90分钟)39、40。另外两组的大鼠被置于同一室内,接受室内空气(1个大气压下21%的氧气,90分钟/天)作为假治疗。使用丧失能力测量仪(Singa Technology,Taipei,台湾)测量受伤和未受伤的后肢之间的重量分布比例,而正常大鼠的重量分布为50-50。在烧伤前第0天和烧伤后每周进行一次测量,直至处死大鼠。在5秒的时间内进行了3次测量的重量平衡测试,并如前所述计算了后爪重量分布的变化。
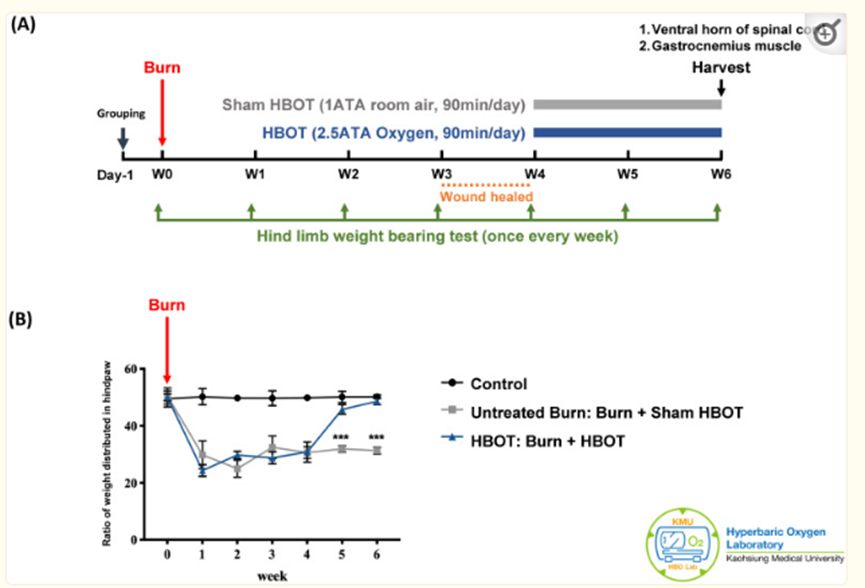
图1实验设计和行为测试结果。(A) 实验设计的时间过程。(B) 每组在指定时间点的丧失能力测试结果。测量受伤后爪和非受伤后爪之间的重量分布比。HBOT在烧伤后第5周和第6周显著改善了右后爪的负重能力。数据显示为平均值±标准偏差***p<0.001(每组n=6只大鼠)。
烧伤后6周,使用舒泰50(50μg/g;澳大利亚Virbac实验室)对大鼠进行麻醉。取腓肠肌和脊髓腹角(L3-5段)。根据制造商的说明,用苏木精和伊红(H&E)、苦杏仁红和Masson三色染色对腓肠肌组织切片进行染色,并通过光学显微镜进行可视化。每组的平均肌肉横截面积是通过尼康Eclipse E600显微镜从每个标本的六个染色切片中获得的,图像是用尼康Digital Sight DS-5M成像系统捕获的。在显微镜下观察后,使用Image Pro Plus 6.0图像分析软件(Media Cybernetics,Bethesda,MD,USA)对Masson的三色染色图像进行纤维化分析。肌肉切片还与肌环指-1(MuRF-1,1:200;Bioss Antibodies,中国北京)和层粘连蛋白(1:200;GeneTex,美国加州尔湾)一起孵育过夜,进行免疫荧光分析。对atrogin-1(1:1000;Affinity Biosciences,Changzhou,China)进行蛋白质印迹以观察肌肉萎缩,并在肌肉切片中评估胱天蛋白酶级联(胱天蛋白酶-3,1:1000;Cell Signaling Technology,Beverly,MA,USA;胱天蛋白酶-9,1:1000;Novus Biologics,Littleton,CO,USA)。使用ECL蛋白质印迹检测试剂盒和Bio-Rad ChemiDoc XRS系统对蛋白质条带进行可视化。Quantity One软件也对谱带强度进行了量化和绘制。
此外,用末端脱氧核苷酸转移酶dUTP缺口末端标记(TUNEL)法研究了脊髓腹角的神经元凋亡,并用倒置显微镜(Leica DMI6000)记录了图像。对腹角中磷酸化的NFκB(p-NFκB,1:200;细胞信号技术)、神经胶质原纤维酸性蛋白(GFAP,1:500;Arigobio,台湾)、裂解的胱天蛋白酶3(1/1000;细胞信号处理技术)、HIF-1α(1:200;Bioss Antibody,北京,中国)和神经元特异性核蛋白(NeuN,1:1000;Millipore,Temecula,CA,美国)进行免疫荧光染色,并通过荧光显微镜(Leica DMI6000)进行分析。此外,Western blot用于研究p-NFκB(1:1000;细胞信号技术)、p-IκB(1/1000;细胞信息技术)、切割的胱天蛋白酶3(1:1000,细胞信号技术mTOR,1:1000;细胞信号,技术),mTOR(1:1000,细胞信号技术),HIF-1α(1:500;Bios抗体)和β-肌动蛋白(1:5000;Novus生物制品)在腹角。
组间差异的显著性通过配对学生t检验或单因素方差分析来确定,然后根据需要进行事后Dunnett多重比较检验。所有数据均以平均值±标准差(SD)和95%置信区间(CI)表示,分别由条形图和误差条表示。实验结果采用SPSS 14.0版软件(SPSS,股份有限公司,美国伊利诺伊州芝加哥)进行分析。p值<0.05被认为具有显著性。
结果
如图1B1B所示,未经治疗的烧伤组右后爪的承重能力显著降低,并在烧伤后持续6周。与未经治疗的烧伤组相比,HBOT组在烧伤后第35天和第42天表现出更大的承重能力(95%置信区间分别为10.67-17.11,p=0.0003;95%置信区间为14.65-19.96,p=0.0001)。这些结果表明,HBOT改善了力分布的均匀性。
腓肠肌切片用H&E和抗层粘连蛋白抗体染色,以研究图2中的肌纤维结构和横截面积;2.烧伤后,与假手术相比,烧伤显著减小了肌肉纤维的直径,但HBOT显著增加了平均纤维横截面积(95%CI:153.0-986.8,p<0.05)。根据picrosirius红染色和Masson三色染色,HBOT减轻了烧伤后纤维化区域的程度(图(图2).2)。此外,腓肠肌中的免疫荧光显示,在肌肉萎缩期间被激活的E3泛素连接酶MuRF-1的表达与腓肠肌的炎症反应有关
图2:通过组织学检查,HBOT改善了烧伤引起的肌肉萎缩和纤维化。(A) 烧伤后42天,每组腓肠肌横截面的苏木精和曙红(H&E)染色和层粘连蛋白(B)免疫荧光。HBOT改善烧伤后肌纤维横截面积的减少。(C) Picrosirius red和(D)Masson三色染色腓肠肌切片,显示总胶原蛋白含量。结果显示为腓肠肌切片中胶原蛋白的百分比面积。与对照组和HBOT组相比,未经治疗的烧伤组腓肠肌胶原沉积显著增加。原始放大倍数×400。比例尺,50µm*与对照组相比,p<0.05,**p<0.01。
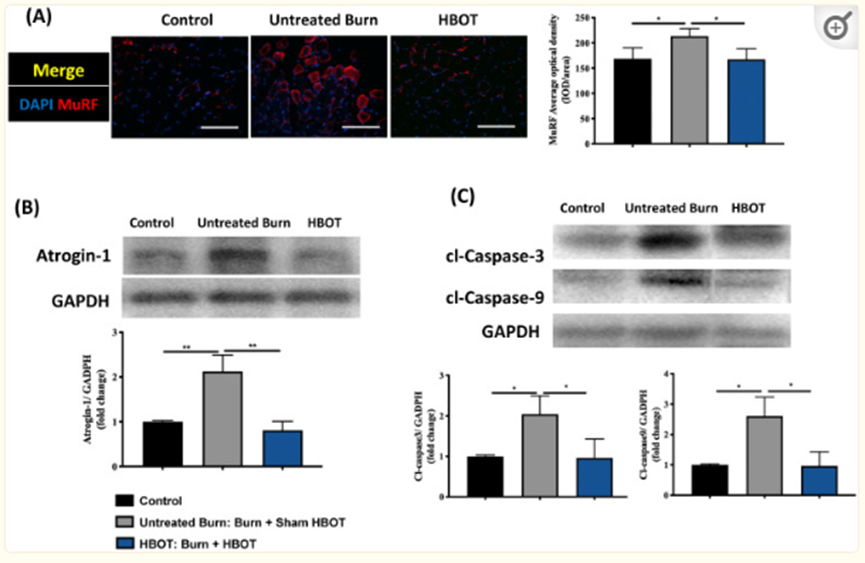
图3HBOT通过免疫荧光和蛋白质印迹减轻烧伤引起的肌肉萎缩。(A) 腓肠肌中肌环指-1(MuF-1)(红色)的免疫荧光。参与骨骼肌萎缩的MuF-1在未经治疗的烧伤组中上调,HBOT减轻了这一现象。肌肉切片中的细胞核用DAPI(蓝色)复染。(B) 泛素介导的骨骼肌蛋白质降解的重要调节因子atrogin-1的蛋白质印迹分析。HBOT减轻了烧伤后atrogin-1的显著下降。(C) cl-capase-3和-9的蛋白质印迹分析。HBOT还可以改善烧伤后胱天蛋白酶级联的上调。比例尺,50µm*与对照组相比,p<0.05,**p<0.01。
在腹角,研究了HBOT的抗炎和抗凋亡作用。HBOT降低了烧伤后NFκB介导的星形胶质细胞活化,如免疫荧光所示(图4A),并减弱了p-NF-κB和p-IκB的过表达,如蛋白质印迹所示(见图4B)。用NeuN进行TUNEL双标记染色,以共定位神经元凋亡;与对照组相比,未经治疗的烧伤组TUNEL和NeuN阳性细胞更丰富,但HBOT组凋亡的神经元细胞更少(图5A)。合并图像显示,在未经治疗的烧伤组中,NeuN阳性细胞中的裂解能力-3免疫染色更多,但HBOT减少了烧伤后胱天蛋白酶-3阳性神经元的数量。此外,通过蛋白质印迹,HBOT降低了烧伤后切割的半胱氨酸天冬氨酸蛋白酶-3、切割的半胱氨酸蛋白酶-9和BAX(凋亡调节因子)/BCL-2(抗凋亡蛋白)的表达(图5B)。5B)。这些结果表明,HBOT可以减少腹角的神经炎症和细胞凋亡。我们之前报道过AKT/mTOR通路参与烧伤诱导的运动神经元凋亡42。HIF-1α是参与组织炎症和细胞凋亡的关键调节因子。Western印迹显示,烧伤后p-AKT/AKT、p-mTOR/mTOR和HIF-1α的表达升高,HBOT后明显降低(图(图6A).6A)。双重免疫荧光还显示,HIF-1α和NeuN阳性标记细胞在未经治疗的烧伤组中增加,在HBOT组中减少(图6B)。
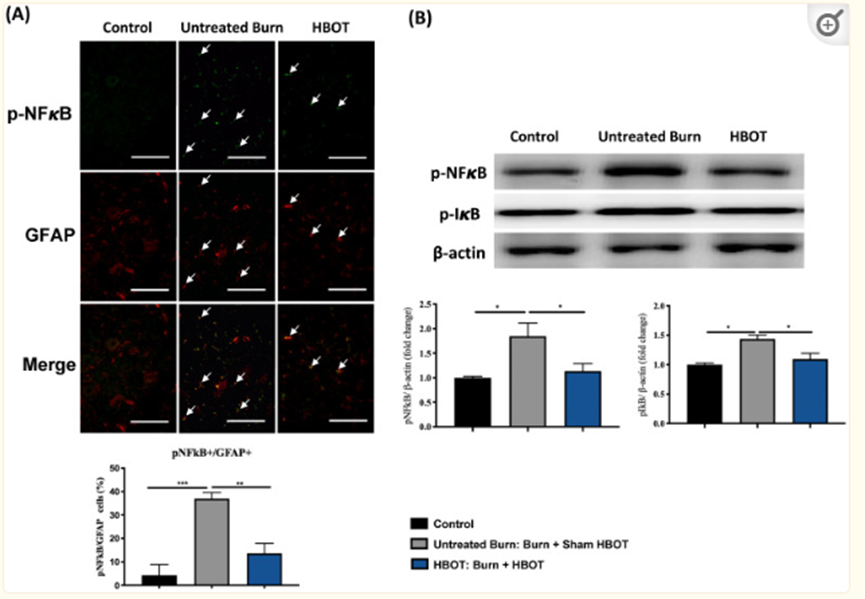
图4 HBOT抑制脊髓腹角烧伤引起的神经炎症。(A) GFAP(红色)和NFkB(绿色)的代表性免疫荧光图像是脊髓腹角。HBOT降低烧伤后NFkB介导的星形胶质细胞活化。(比例尺,50µm)。(B) 脊髓腹角p-NFkB和p-IkB的蛋白质印迹分析。HBOT减轻了烧伤后p-NFkB和p-IkB的增加*与对照组相比,p<0.05,**p<0.01,***p<0.001。
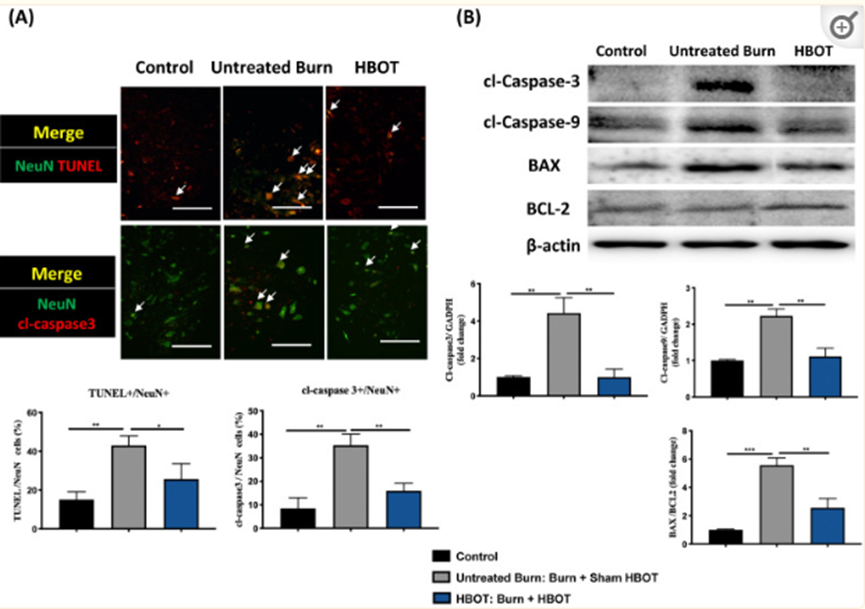
图5 HBOT可减轻烧伤诱导的脊髓腹角神经元凋亡。(A) TUNEL检测(红色)和NeuN(绿色)的合并图像。HBOT组TUNEL阳性细胞减少(双染色,箭头)。(B) 裂解(cl)-半胱氨酸天冬氨酸蛋白酶-3(红色)/NeuN(绿色)双重免疫荧光图像显示,HBOT减少了烧伤后半胱氨酸天冬氨酰蛋白酶-3阳性神经元的数量(双重染色,箭头)(比例尺,100µm)。(C) cl-caspase-3、cl-caspase-9、BAX和BCL-2的蛋白质印迹分析。HBOT组半胱氨酸天冬氨酸蛋白酶级联和BAX/BCL-2比值降低*与对照组相比,p<0.05,**p<0.01,***p<0.001。
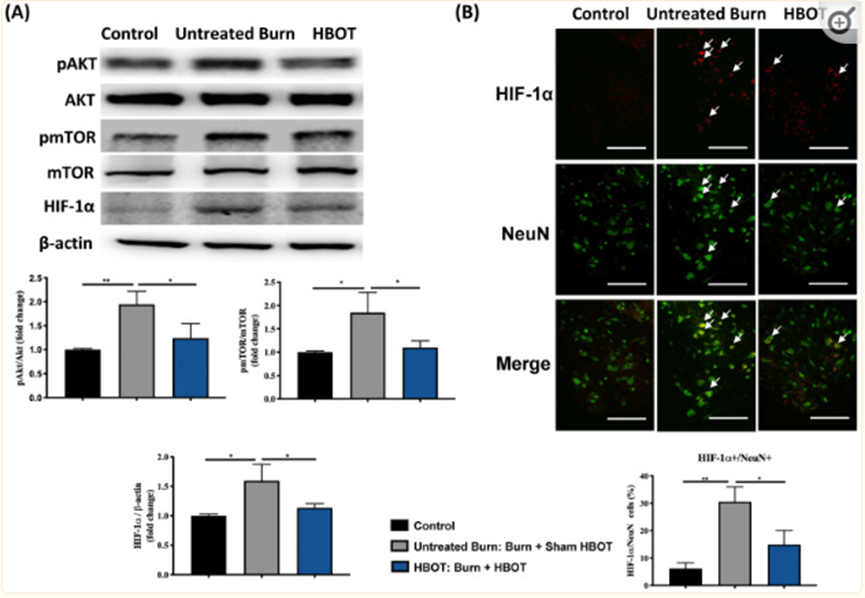
图6 HBOT通过调节AKT/mTOR/HIF-1α来减轻烧伤诱导的神经元凋亡。(A) AKT、mTOR和HIF-1α的蛋白质印迹分析。HBOT降低烧伤后AKT、mTOR和HIF-1α的表达。(B) HIF-1α(红色)和NeuN(绿色)的免疫荧光。HIF-1α(红色)/NeuN(绿色)双重免疫荧光图像显示,HBOT减少了烧伤后HIF-1α阳性神经元的数量(双重染色,箭头)。(比例尺,100µm)*与对照组相比,p<0.05,**p<0.01。
讨论
在本研究中,我们研究了延迟HBOT(2.5 ATA,90分钟/天)的治疗效果,该治疗在烧伤后5周开始,共14次治疗,以及HBOT后烧伤引起的神经肌肉损伤慢性期的治疗机制。HBOT减少了大鼠烧伤后受伤肢体的步态障碍和腓肠肌萎缩。腹角的炎症和凋亡导致失神经肌肉萎缩是烧伤模型中的关键致病过程。HBOT减轻了烧伤引起的脊髓腹角神经炎症和神经元凋亡。我们的研究结果还表明,HBOT的治疗作用涉及HIF-1α通路。
据报道,HBOT可以减少组织缺氧、炎症反应和血管新生。然而,HBOT在烧伤护理中的益处的证据仍然不足43-45。此外,对于烧伤护理,HBOT的最佳剂量和时间尚不确定。实验和临床研究表明,HBOT在烧伤伤口愈合中的应用46,47。辅助HBOT已被建议减少烧伤后细菌移位和败血症48,49。此外,越来越多的数据支持将HBOT作为中风50-52、神经退行性疾病53-55和创伤性脑损伤56的神经保护策略的一部分,以改善功能恢复。在这项研究中,我们发现延迟HBOT(在烧伤后28-41天服用)有助于减少烧伤后的长期神经肌肉并发症。
HBOT的效果取决于剂量、压力、持续时间、频率和累积治疗次数。我们之前对大鼠的烧伤研究表明,2周的HBOT比1周的HBOT38具有更长的保护作用。在本研究中,14次2.5ATA的HBOT(90分钟,每天一次)减轻了腹角的细胞凋亡和炎症反应。几项研究提出,HBOT下调NF-κB信号传导,以减轻脊髓损伤57-59后的炎症反应。在我们的实验性烧伤模型中,HBOT降低了烧伤后腹角p-NF-κB和p-IκB的活化。NF-κB在细胞分裂和凋亡的控制中起着关键作用。小胶质细胞中NF-κB在损伤反应中的激活促进神经元退化60。此外,烧伤后腹角BAX与BCL-2的比值增加,caspase-3和caspase-9的激活也增加。HBOT显著减少了烧伤后凋亡神经元细胞的数量,并降低了BAX/BCL-2、caspase-3和caspase-9的表达。
除了烧伤后失神经肌肉萎缩外,我们的研究结果表明,HBOT还降低了腓肠肌组织中胱天蛋白酶的表达,并减少了E3泛素连接酶的上调。HBOT促进诱导性肌肉损伤的恢复61。据报道,增加肌生成11、调节骨骼肌线粒体62的效率和增强卫星细胞63的分化有助于HBOT损伤肌肉的恢复。在这项研究中,HBOT减弱了腓肠肌中胱天蛋白酶-3和胱天蛋白酶-9的表达,表明HBOT保护肌肉组织免于凋亡。泛素-蛋白酶体蛋白水解途径的激活也通过加速肌原纤维蛋白64-66的分解在烧伤诱导的骨骼肌萎缩中起着重要作用。Atrogin-1和MuRF-1是两种肌肉特异性E3泛素连接酶,是肌肉萎缩的极好标志物67。通过蛋白质印迹分析,HBOT降低了烧伤后腓肠肌组织中atrogin-1的表达。免疫荧光还显示,HBOT显著减少了烧伤后MuRF-1阳性细胞的数量。
HIF-1α在HBOT减轻烧伤诱导的运动神经元死亡中的作用尚不清楚。之前的报告表明,HBOT通过降低HIF-1α68、69的表达来促进神经发生。在大鼠脊髓损伤模型中,损伤后HIF-1α的蛋白产生升高,但HBOT降低了HIF-1α70的表达。HIF在生理和病理条件下起着重要作用,涉及存活、细胞周期和代谢71、72。它们被缺氧应激激活;然而,在常氧条件下也经常发现73、74。Stiehl等人假设HIF-1α在常氧条件下通过磷脂酰肌醇3激酶途径74被胰岛素和白细胞介素-1β等肽激活。一篇综述论文还指出,HIF和NF-κB之间可能存在多种医学状况的分子串扰75,因为HIF与炎症有关并放大NF-κB。我们的结果表明,HBOT抑制腹角NF-κB、IκB和HIF-1α的激活,以防止烧伤后神经元凋亡。此外,AKT/mTOR通路已被认为在细胞周期76-78的调节中起着关键作用,抑制AKT/mTOR信号传导可保护神经元免于凋亡79。此外,AKT通路是HIF-1α激活的主要上游介质,与氧气浓度80、81无关。我们之前的研究表明,烧伤通过AKT/mTOR通路82诱导腹角的程序性细胞死亡。在这项研究中,HBOT降低了烧伤大鼠模型腹角中p-AKT、p-mTOR和HIF-1α的表达。我们认为,HBOT通过调节AKT/mTOR/HIF-1α信号通路和灭活凋亡相关蛋白来减轻运动神经元凋亡。
HBOT在治疗神经元损伤83-85方面具有巨大潜力。然而,我们的研究存在一些局限性。首先,HBOT的最佳时机和总治疗次数需要进一步研究,以阐明HBOT的有效性。其次,我们选择将HBOT推迟到烧伤愈合;然而,该模型中没有评估早期HBOT的疗效。第三,HIF-1α在我们的烧伤模型中HBOT治疗效果中的作用仍有待充分阐明。第四,需要后续研究来调查HBOT的长期有效性。第五,HBOT是否对运动神经元和肌肉修复具有同步作用,需要进一步研究以阐明。
我们的研究表明,HBOT通过调节HIF-1α信号传导来减轻烧伤后腹角烧伤诱导的神经元凋亡。HBOT进一步减轻了烧伤后失神经腓肠肌萎缩和纤维化变化。
首选
致谢
台湾科学技术部(MOST110-314-B-037-092)、高雄市立大东医院(kmtth-109-R011)和中华民国儿童烧伤基金会提供了支持本研究的研究资助。
本信息并非旨在或暗示作为专业医疗建议的替代;不应在任何医疗紧急情况下使用,也不应用于
任何医疗状况的诊断或治疗。所有医疗紧急情况请拨打120。




