
迈克尔·A·弗利尔 1,菲利普·F·斯塔赫尔 1,2,✉巴塞尔 M 图班 1,凯瑟琳·M·博尚普 2,史蒂文·J·摩根 1,韦德·R·史密斯 1,凯罗斯·R·伊帕克奇 1
2科罗拉多大学医学院丹佛健康医疗中心神经外科 USA
摘要
严重的烧伤仍然是患者和医疗系统的重大负担。严重烧伤后,受损组织会发起局部炎症反应,旨在恢复体内平衡。当烧伤负荷过大时,免疫反应变得不成比例,患者可能出现过度的全身性炎症反应,损害肺、肾、肝和大脑的多重生理屏障。如果血脑屏障被突破,系统性炎症分子和吞噬细胞会迅速进入大脑,激活中枢神经系统的固定细胞。这些炎症细胞释放大量活性氧、活性氮、蛋白酶、细胞因子/趋化因子和补体蛋白,导致神经元损伤和危及生命的脑水肿。尽管严重烧伤患者的脑部并发症与死亡率存在相关性,烧伤诱发的神经炎症在重症烧伤患者中仍然被低估。本文阐述了导致血脑屏障破坏的分子事件,重点关注严重烧伤患者随后的神经炎症变化导致脑水肿。
严重烧伤仍然是社会的重要健康问题,也是受害者生命的威胁事件。仅美国每年就有超过120万人遭受烧伤伤害[1];其中约有10万患者住院,累计住院天数达200万天[2]。根据儿童烧伤意识项目,热损伤主要影响50岁以下患者[3],并且仍是儿童死亡的主要原因之一。虽然整体死亡率报告为5%,但随着年龄增长和烧伤规模的增加,死亡率迅速上升,最高可达96%[3]。大多数死亡病例(65%)似乎与烧伤引起的多器官衰竭有关,93%的烧伤患者在因伤去世前出现系统性炎症反应综合征的临床症状[4]。 严重烧伤患者中一个严重受损但常被忽视的器官是大脑,尽管严重烧伤患者的脑部并发症已被证明与死亡率高度相关[5]。在多达10%的严重烧伤患者中,低氧性脑损伤被发现是主要死亡原因,且与年龄相关[6]。本综述重点关注严重烧伤后发生的神经炎症变化及其发病机制。 在生理条件下,血脑屏障(BBB)严格调节进入脑组织的分子。然而,在系统性炎症反应综合征、败血症或严重烧伤期间,这道介于全身循环与脑实质之间的物理屏障可能会受到严重破坏。 当周围组织暴露于严重烧伤时,会释放大量促炎介质、细胞毒性蛋白酶、活性氮和活性氧物质。这些介质随后引发全身反应,如发热[7,8]、低水症[9]、痛觉过敏[10,11]、严重烧伤诱发厌食症(消瘦综合征)[9,12]、下丘脑-垂体-肾上腺轴的激素改变,以及内源性儿茶酚胺水平变化[13,14].所有这些炎症变化都试图恢复身体的平衡。然而,当烧伤负荷过大时,释放的炎症介质系统水平会过高且不成比例,导致不良结局[15]。大脑微血管通透性增加,使先前被阻断的大型全身性分子(如白蛋白(见图1a)、渗出物及众多炎症细胞得以渗入周围脑组织。简介
血脑屏障崩溃及脑水肿的发生
图1。
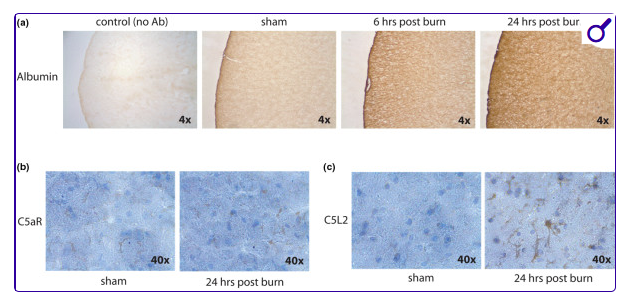
实验性烧伤中血脑屏障的破坏及C5a受体的补充表达。(a)实验性烧伤后随时间变化获得的大鼠大脑冠状切片。切片随后对白蛋白进行免疫组化染色。对照切片中省略了原抗(无抗抗体),以确保白蛋白抗体的特异染色。将假动物(假动物)的脑滑片与烧伤大鼠的大脑进行比较。注意烧伤后6至24小时血脑屏障逐渐崩溃,导致脑内白蛋白积累增加。作为一种大型全身分子,白蛋白只有在血脑屏障被破坏时才能穿过。目前数据表明血脑屏障崩溃加剧,随后脑水肿发展。冠状脑切片分别取自假动物和烧伤后24小时,并对(b)C5a受体(C5aR)和(c)C5a样受体2(C5L2)进行了免疫染色。部分区域随后用快蓝染色。所描绘的区域聚焦于大脑的海马体区域。染色细胞代表小胶质细胞。虽然假大鼠与烧伤大鼠的C5aR表达无差异,但从烧伤动物采集大脑的C5L2表达显著上调,而与假同窝同窝大鼠相比。补体系统可能在烧伤诱发神经炎症的发生中起重要作用。载玻片采用光学显微镜分析,采用四倍(4×)和四十倍(40×)放大。
这些事件会引起随后的神经元损伤[16]和脑水肿[17,18],并可能导致颅内压严重升高[19]。导致这种严重炎症性下行螺旋的病理生理事件如图2所示。严重烧伤后BBB泄漏的程度似乎与严重烧伤患者的死亡率相关[5]。在接下来的章节中,我们将展示导致BBB失效的分子机制。
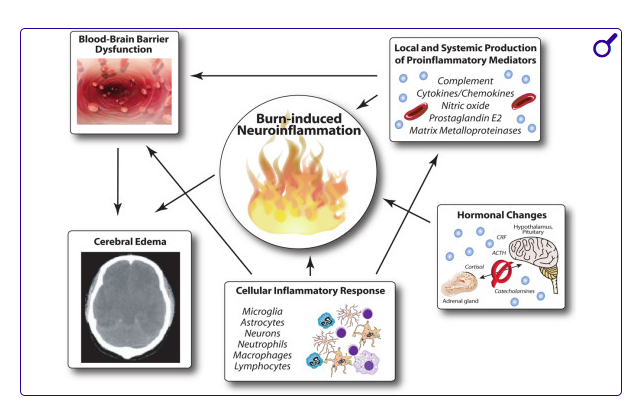
烧伤后导致血脑屏障崩溃及脑水肿的病理生理事件。在严重烧伤后,会触发强烈的全身性炎症反应。促炎介质由各种免疫细胞产生,导致血脑屏障破坏,随后激活驻留的中枢神经系统细胞,如微胶质细胞和星形胶质细胞,这些细胞进一步产生炎症标志物,最终引发大规模神经炎症反应,随后引发危及生命的脑水肿。与此同时,显著的激素变化会被触发,导致严重的代谢亢进状态。促肾上腺皮质激素释放因子(CRF);ACTH,促肾上腺皮质激素。
在实验和患者环境中,严重烧伤后补体系统的激活均已描述[20,21]。虽然适度有益,但补体过度激活可能对宿主有害。事实上,实验性烧伤引起的肺部继发损伤[20]和烧伤诱发的过敏性C5a产生可能与心脏功能障碍有关,表现为左心室压力显著降低和肌节收缩力受损[22]。此外,强健补体激活被描述为创伤性脑损伤和脑膜炎神经病理生理的关键事件[23]。 令人惊讶的是,关于补体系统在烧伤后神经炎症中的作用的文献极为有限。然而,合理推测补体级联反应在烧伤诱导神经炎症的病理生理中起重要作用,因为补体系统的组成部分由多种固着性脑细胞类型表达和释放。 在我们的实验室中,我们发现了两种C5a受体(C5aR和C5L2)在标准化大鼠全层灼伤模型中,烧伤诱导的调节有证据,该模型中30%的全身表面积被烧伤。我们比较了假动物或烧伤动物海马体中C5aR和C5L2的表达(Flierl MA、Stahel PF、Touban BM,未发表观察;图1)。烧伤后海马体C5aR表达似乎无变化,但烧伤后24小时C5L2显著上调(见图1b,c)。与早期的猜测相反,C5L2最近被确认为一种具有明显促炎作用的功能受体[24]。因此,C5L2可能参与烧伤后补体介导的神经炎症。 严重烧伤会促使受影响组织迅速局部产生促炎细胞因子。在人类和动物严重烧伤后,血清TNFα、IL-1β和IL-6水平均被报告升高[25-28]。虽然血清中IL-6、IL-8和IL-1β的浓度与严重烧伤的程度成正相关,但只有血清IL-8水平与死亡率呈正相关[27,29]。TNFα、IL-1β和IL-6均已被证明能直接在体外诱导BBB的破坏[30]。 近期在多种神经炎症动物模型中的研究证实了BBB以细胞因子/趋化因子依赖性的方式分解[31-33]。细胞因子和趋化因子最初仅在烧伤部位产生,但可能成为全身性物质,直接攻击BBB。此外,严重烧伤在损伤后3小时显著上调脑组织中TNFα、IL-1β和细胞间粘连分子1的mRNA水平[26]。因此,必须认识到严重的烧伤会使BBB暴露于来自大脑和全身循环两个不同区室的有害促炎介质。目前尚无数据表明人类中BBB分解需要多严重的烧伤损伤,但大多数动物模型会在60%至70%的身体表面造成严重烧伤以诱发BBB功能障碍[34,35]。 一氧化氮(NO)具有多方面的生物和免疫功能[36,37],并由神经元、内皮细胞或线粒体中定位的不同NO合酶异构体进行生物合成[38]。相比之下,诱导性NO合成酶在所有对免疫刺激产生大量NO爆发的有核细胞中均有表达[39]。诱导性NO合成酶输出NO通常与炎症性疾病相关,如出血、外伤或严重烧伤[39,40]。抑制诱导性NO合酶可减少实验性严重烧伤后的微血管渗漏[41],且在严重烧伤后诱导性NO合酶阻断已报告有益[42]。 关于尿中硝酸盐和亚硝酸盐水平是否对烧伤患者临床决策具有预测价值存在较大争议。虽然一些研究报告烧伤后第5天NO、亚硝酸盐和硝酸盐水平升高,并将NO水平与死亡率相关[43-45],但也有研究描述了血浆亚硝酸盐水平显著下降和硝酸盐水平升高[46]。关于烧伤后尿液中亚硝酸盐和硝酸盐浓度的报告也存在争议[45-48]。严重烧伤后NO的不良反应可能由NO与超氧化物(O2-)相互作用介导,导致高度毒性的氧化剂过氧亚硝酸盐形成[49]。过氧亚硝酸盐随后会造成广泛的组织损伤和水肿形成[50,51]。过氧亚硝酸盐的生成已在严重烧伤部位以外的器官中被描述,使其成为严重烧伤诱发多器官衰竭的重要介质[52,53]。 令人意外的是,热损伤后下丘脑诱导性NO合酶的mRNA表达显著下降[54],严重烧伤后大脑皮层的NO水平迅速下降[55]。关于这种中枢/外周差异的假说包括NO从大脑向烧伤部位招募,和/或因中枢NO的氧化和自由基有害作用而形成的负反馈回路阻断[55]。 外周严重烧伤会诱导中枢神经系统内皮细胞中的环氧酶-2和微粒体型前列腺素E合酶,导致脑脊液中前列腺素E2水平升高[56]。因此,脑脊液中前列腺素E2水平升高可能参与严重烧伤后中枢神经系统介导的系统反应的发病机制。最终,严重烧伤患者可能从环氧合酶-2选择性抑制剂治疗中枢神经系统介导症状中受益。然而,认识到使用环氧加氧酶-2选择性抑制剂后胃肠道出血风险增加非常重要。 基质金属蛋白酶最近被确认是严重烧伤后BBB功能障碍发展的关键因素[34,35]。在严重烧伤后上调时,这些蛋白酶可能促成BBB基底层的降解和破坏。 严重烧伤后,身体会以一般的应激反应[57]。经过初期的退潮期[12,58]后,会发生普遍的超分解代谢[57]。这种高代谢至少部分由儿茶酚胺介导,并与损伤的严重程度相关[14]。严重烧伤后,血浆儿茶酚胺增加多达10倍[59,60],导致超动态循环[61]。此外,去甲肾上腺素和多巴胺在大脑某些区域水平升高[12,58,62],儿茶酚胺水平升高会动员体内脂肪和蛋白质储备中的底物,导致瘦体重流失和肌肉萎缩[12]。严重烧伤后阻断β肾上腺素能受体,可减少产热、心动过速、心脏工作负荷和静息能量消耗[63-65]。在严重烧伤儿童中,使用β肾上腺素受体阻断剂普萘洛尔治疗减轻了高代谢并逆转了肌肉-蛋白质的分解代谢[66,67]。 严重烧伤导致下丘脑功能改变也被描述[68]。最新研究证实严重烧伤患者下丘脑-垂体-肾上腺轴受扰。下丘脑肽和促皮质激素释放因子家族受体被确认为严重烧伤诱导代谢亢进的潜在介质[69,70]。血清催乳素与烧伤严重程度相关[29],进一步在严重烧伤早期阶段报告了暂时性肾上腺功能不全[71],这与更高的死亡率相关[72]。一项研究在儿童热损伤后下丘脑-垂体-肾上腺轴上发现了促肾上腺皮质激素-肾上腺反馈回路的破坏[73]。 迄今为止,尚无直接研究严重烧伤后小胶质细胞和胶质瘢痕激活的报告。在一项最新研究中,实验性严重烧伤后,周围轴突口径和传导速度严重受损[74]。这些形态和功能缺陷在远离烧毁地点的侧面观察到。严重烧伤后轴突口径减小和神经传导速度减弱,不仅可能影响外周神经元,还可能影响中枢神经元,并可能导致神经肌肉传递的改变以及严重烧伤常见的肢体和呼吸肌无力。此外,在烧伤组织中,周围感觉神经元的长期激活会导致脊髓的重组[75]。从组织学角度看,脊髓背角表现出μ-阿片受体表达减少[76]。 最近在伤口边缘新形成的上皮细胞中检测到神经生长因子[77]。这种生长因子不仅有助于伤口重组和愈合,还可能在严重烧伤后引发对热和机械刺激的过敏反应[78,79]。神经生长因子似乎增强了与背角神经元的传入神经连接的强度和分布[80],从而扩展其感受野[81]。这些发现表明,严重烧伤后脊髓会出现中枢可塑性。 严重烧伤会激活中性粒细胞和巨噬细胞[82]。脑内产生的细胞因子和趋化因子通过BBB吸引吞噬细胞[26]。此外,一旦BBB严重受损,系统性吞噬细胞即可自由进入脑血管周围空间[83]。活化的吞噬细胞释放其全部炎症性蛋白酶、活性氧和活性氮[84-86],加剧神经炎症反应。严重烧伤后,吞噬细胞对促炎介质的生产能力显著增强[82]。巨噬细胞在热损伤后表现出增强的氧化代谢[85],严重烧伤患者则显示氧自由基活性增加[87]。因此,与幸存者相比,未幸存的严重烧伤幸存者抗氧化剂摄入量增加[87]。 严重烧伤会引发显著的脑电图异常[88]。在初期心血管稳定、复苏和止痛过程中,较不明显的神经精神后果常常被镇静治疗掩盖。严重烧伤后出现的神经症、认知障碍和行为后果均已在文献中有所描述[89,90]。在热损伤后的初期阶段,可能会出现暂时性失忆[91]。 如上所述,严重烧伤后,一氧化氮水平会在外周上调。此外,NO已被证明是中枢神经系统中重要的生物分子,神经元NO合触广泛存在[92]。NO作为神经精神神经递质的假定作用涉及海马体的长期增强和小脑的长期抑制[93,94]。NO似乎特别参与短期记忆和学习[92,95]。生物行为检测证实了NO在记忆获取和巩固中的重要作用[96,97]。最近发现,大脑NO水平的快速且显著下降解释了大鼠行为变化[55]。是否通过脑内NO代谢的改变缓解严重的烧伤引发的认知障碍,尚待观察。 大约三分之一的烧伤患者表现出身体、精神或酒精相关问题的迹象,使其易受伤害[98]。在烧伤后的关键复苏阶段,患者常表现出极度嗜睡、迷糊、迷糊、谵妄和精神病反应等认知变化[99]。在康复和恢复性护理的急性期,抑郁、焦虑、睡眠障碍和前病精神病理症状很常见[100]。出院后,患者可能会出现抑郁症或创伤后应激障碍的症状,这些症状可能在烧伤后1个月到初次烧伤后2年之间出现[99,101]。超过50%的烧伤患者在住院早期报告中度至重度抑郁症状,且近50%在受伤两年后仍保留这些症状[102,103]。有趣的是,烧伤的程度并不能预测烧伤后的心理问题[102-104]。烧伤一年后,约20%的患者符合创伤后应激障碍的诊断标准[105]。 恐惧回避或神经质等功能失调信念被描述为烧伤后的长期后遗症[106]。睡眠障碍也被描述为烧伤的长期后遗症[107]。多学科团队合作似乎是成功管理和烧伤患者长期重新融入的关键。 烧伤护理的进步在过去50年中显著降低了死亡率[108-110]。特别是,早期且积极切除烧伤伤口对烧伤患者的发病率和死亡率影响最大,通过减少伤口败血症、高分解代谢、手术次数和住院时间的发生率[111-114]。因此,当前治疗指南建议在首家医疗机构对严重烧伤进行常规且积极的清创[115]。即使在严重烧伤后出现感染并发症时,治疗的基石仍是早期、积极且确定的外科清创——而抗生素仅被视为治疗的重要辅助[116]。后续皮肤移植通常通过自体或异源皮肤或生物合成皮肤替代物完成[117]。 可以想象,早期且积极切除烧伤伤口的无可置疑益处与上述病理生理变化密切相关。当烧伤负荷过大时,受伤周围组织引发的局部炎症反应可能溢出至全身循环,形成上述炎症恶性循环。因此,随后的恶性循环可通过积极的初步清创早期被打断,显著减轻全身炎症负担,改善终末器官功能,降低发病率和死亡率。全层烧伤的早期切除也与烧伤引起的代谢亢进减弱相关[118-120]。 目前,几种有前景的免疫调节治疗策略——如免疫营养、重组人活化蛋白C的施用或局部免疫抑制剂——的实验台到床边移植正在研究中,详见其他文献[121]。因此,最近一份报告呼吁将“优秀的动物研究成果进一步转化为人类领域”,以推动严重烧伤患者的护理[122]。 严重的烧伤诱发神经炎症是一个极其复杂和复杂的现象。只有当治疗重症护理人员深入了解严重烧伤后的系统性和大脑病理生理,并据此调整治疗方式时,才能实现严重烧伤患者的最佳管理。虽然肺、肾或肝脏屏障的塌陷通常通过简单的实验室参数识别,并作为严重烧伤管理的一部分治疗,但烧伤诱发的神经炎症会随时间演变,因此在初步计算机断层成像评估中无法检测到。如果治疗医生未能识别烧伤后复杂的脑部炎症事件,患者可能会被提前允许进行手术干预,这可能导致潜在的有害医源性第二次击中。因此,主治医生需要对这一棘手的存在保持高度的怀疑。虽然涉及的一些分子事件已被充分理解,但仍有许多未解之谜,这些问题需要通过实验和临床研究来解决,以推动重症烧伤患者的护理进步。亚细胞免疫变化
补体激活
细胞因子与趋化因子
一氧化氮
前列腺素E2和基质金属蛋白酶
激素应激反应的紊乱
细胞变化
神经元
嗜中性粒细胞和巨噬细胞
神经精神病学影响与认知功能障碍
神经精神病学影响
认知功能障碍
免疫病理生理学对烧伤管理的影响
结论




