烧伤是一种多样且复杂的损伤,不仅有局部影响,还通过严重且持久的炎症反应带来严重的全身性后果。它们由热、电、摩擦、化学物质或辐射引起,通常分为浅层、浅层部分损伤、深度部分损伤和全层损伤。烧伤的严重程度主要取决于伤口的大小和深度,也取决于部位、年龄和潜在的全身性疾病。长期且强烈的免疫反应会使严重烧伤加重,因为它会造成多种系统性影响,包括对心脏、肺部、血管、肾脏及其他器官的损伤。无需手术切除的烧伤,无论是表层还是表层部分厚度,都遵循已知的伤口愈合进程(炎症、增生、重塑),而需要切除和移植的深层部分和全层损伤则无需。对于这些烧伤,需要进行干预以实现最佳覆盖、功能和美容效果。每年全球有数百万人因烧伤而受高发病率和高死亡率的困扰。幸运的是,过去几十年来,烧伤护理有了显著改善。对烧伤损伤及其病理机制及其进展的理解进步,推动了皮肤移植、液体复苏、感染控制和营养领域的进步。本文重点关注烧伤后的免疫和再生反应。在引言中,我们描述了烧伤的流行病学及其病理生理学。下一章重点关注烧伤的系统性应对。接下来,我们定义了免疫对烧伤的反应,引入了所有涉及的不同细胞类型。随后,我们讨论了烧伤的再生细胞反应以及一些新兴的烧伤治疗方法。
关键词:烧伤、免疫反应、炎症、组织再生
1. 引言
根据世界卫生组织(WHO)的说法,烧伤是全球性健康问题[1]。这些伤害痛苦且毁灭性强,且伴随高发病率和死亡率。全球每年有数百万人遭受烧伤,许多人需要住院治疗,近20万人因此死亡。在美国,每年有50万例烧伤需要医疗救助,约有4万人住院治疗。这些患者死亡率也较高,使烧伤成为美国意外死亡的主要原因(烧伤发生率事实表)。在中低收入国家,烧伤负担更为严重,超过90%的烧伤死亡发生[2,3]。幸运的是,过去几十年来,烧伤护理有了显著改善。对烧伤损伤及烧伤伤口进展病理生理学的理解进步,推动了皮肤移植、液体复苏、感染控制和营养学的发展[4]。如今,患有90%全身表面积(TBSA)烧伤的患者仍可存活[5]。然而,烧伤幸存者常常遭受长期的身体残疾、情绪困扰和生活质量下降[6]。
烧伤是由热、电、摩擦、化学物质或辐射引起的组织损伤。烧伤的分类通常取决于损伤的深度,因此它们被分为浅层、浅层、部分性、深度部分性和全层性损伤。表浅烧伤会损伤皮肤的不同层,而深度烧伤则损伤软质(组织脂肪和肌肉)甚至骨骼[4]。烧伤的严重程度主要取决于伤口的大小、深度和位置,以及年龄和潜在的系统性疾病。轻微烧伤影响TBSA低于10%,通常愈合良好;而严重烧伤,TBSA超过20%,通常需要手术治疗才能愈合。这些较大的烧伤也更容易出现并发症,如感染、败血症和皮肤瘢痕形成(见图1A)[7]。
图1。
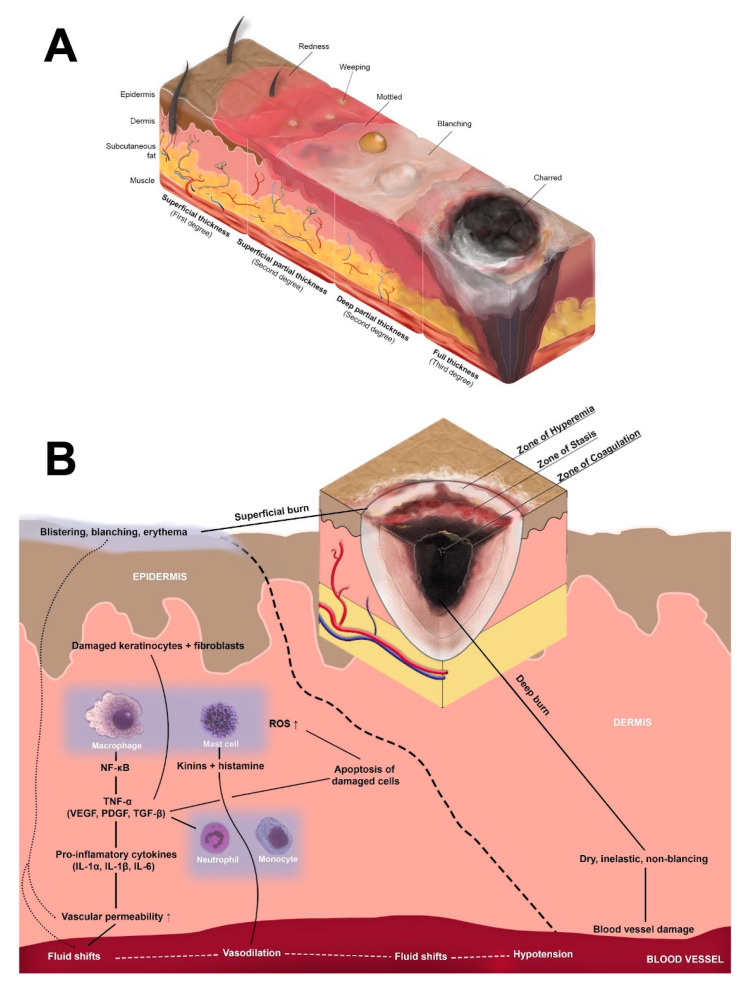
(A)燃烧深度。烧伤分为浅层、局部厚度、浅层或深层或全厚。浅层烧伤会损伤皮肤的不同层,而深层烧伤则损伤软质皮肤(组织、脂肪和肌肉)甚至骨骼。(B)杰克逊区。烧伤分为三个明显的凝血区、静止区和充血区。凝固区是最内侧的区域,也是损伤的主要部位,一旦烧伤发生,其细胞将迅速发生坏死。周围的休眠区表现为组织损伤和缺血,但仍可能有挽救的潜力。充血的最外层区域通常会恢复,但其特征是局部明显肿胀和红肿,主要由损伤引起的即时炎症反应引起。先天免疫系统及其细胞是身体在烧伤后抵御入侵病原体的第一道防线。其特征是防御病原体并处理坏死组织,先天免疫反应为烧伤后伤口愈合的增殖和重塑阶段奠定了基础。图片显示了对真皮表面灼烧的局部炎症反应。
烧伤与其他皮肤伤口不同,主要分为三个不同的凝固区、静止区和充血区。凝固区是最内侧的区域,也是损伤的主要部位,一旦烧伤发生,其细胞将迅速发生坏死[8]。周围的休眠区表现为组织损伤和缺血,但仍可能有挽救的潜力。充血的最外层区域通常会恢复,但其特征是局部肿胀和发红,这是由于损伤引起的即时炎症反应[9]。一旦激活,炎症反应会刺激先天免疫反应及其细胞,保护受损区域免受病原体侵害。此外,炎症细胞清除死细胞和碎屑,为角质细胞和成纤维细胞启动组织修复铺平道路(见图1B)[10]。
然而,对于严重的烧伤,免疫反应持续时间较长且强烈,导致损伤加重,导致多种系统性影响,并损害心脏、肺、血管和肾脏等多个器官[11]。严重烧伤时,热损伤会增加毛细血管的渗透性,导致液体流失,使血浆从循环中泄漏。此外,液体可能滞留在体内,导致水肿。液体的快速流失可能导致烧伤性休克,表现为心输出量降低、血管阻力增加、血容量低和灌注不足[12]。长期且严重的炎症反应还可能导致多器官衰竭,原因是系统性炎症反应综合征(SIRS),表现为心率快、低血压、体温低或过高以及白细胞计数过高或偏低[13]。此外,烧伤部位的长期炎症可能导致肉芽组织过度生长和伤口收缩,最终导致瘢痕形成,疤痕可能毁容、功能受限,甚至可能需要修复手术[14]。
本综述旨在描述烧伤时的免疫和细胞反应。因此,第一章描述了烧伤的系统性反应。下一章将重点介绍免疫对烧伤的反应,介绍所有涉及的不同细胞类型。随后,解释了烧伤后的再生细胞反应以及缓解烧伤后严重炎症反应的策略。“最后,讨论将讨论研究和探索新疗法在抗击烧伤中的重要性。
2. 对烧伤的系统性反应
烧伤的影响可能超出直接受伤部位。事实上,严重烧伤无论来源如何,都会引发全身性炎症反应。每个器官系统中表现出的效应既是烧伤的结果,也是该器官系统对其反应的结果。引发系统性反应的阈值估计为严重烧伤TBSA的20%或更多——超出表层深度。涉及多个器官系统,重点是循环系统导致血流动力学变化,呼吸系统导致呼吸频率或呼吸工作增加,内分泌系统产生高代谢和高血糖状态,以及免疫系统频率和功能的改变。烧伤的全身反应范围从TBSA近乎正常的基础代谢率(BMR)<10%开始,随着严重程度增加,直到TBSA达到40%及以上时,基础代谢率几乎翻倍时达到平稳[15]。以下将讨论严重烧伤对这些器官系统的影响及其随之而来的系统性影响。
2.1. 炎症反应
烧伤会引发大规模炎症反应。严重烧伤后,全身炎症会系统性增加,循环细胞因子如肿瘤坏死因子α(TNF-α)和干扰素γ(INF-γ)升高。系统性炎症反应综合征(SIRS)是一种免疫系统在细胞环境中平衡被破坏时上调的状况。SIRS标准——心率升高、体温和呼吸频率升高、循环白细胞激增——是烧伤后常见的表现,尤其是在严重烧伤引发全身反应后。这种对身体的影响与烧伤的大小成正比,存在于一个光谱上。也就是说,损伤深度越大,受影响的表面积越大,系统性反应就越大[16]。
2.2. 多器官系统的参与
全身性炎症增加毛细血管的通透性,使液体渗入间质,加重周围水肿,并因血管和循环系统内剩余容量减少而加重低血压。心率和全身血管阻力被提高以补偿这一现象,试图维持全身灌注。支气管收缩会影响呼吸功能,导致呼吸工作量增加。随之而来的是呼吸过速,这进一步促进了能量利用和代谢需求的增加。尽管严重烧伤带来的持续创伤增加了周围免疫细胞的丰度,但由于细胞介导和体液保护的抑制,免疫反应仍会出现填塞。由损伤相关分子模式(DAMPs)或危险信号发起的信号,如DNA、ATP、高迁移率基团1(HMGB1)或细胞因子及其他从死亡细胞释放的警报剂,可能调节不正常炎症和免疫反应控制,导致炎症信号过度激活或抑制失败[17,18,19,20,21].抑制DAMPs(也称为SAMPs)的活性增加,如前列腺素E2,旨在最终解决炎症激活,也可能使免疫系统变得脆弱[22]。这使得严重烧伤者感染风险更高,而不仅仅是作为一线防御去除皮肤本身就很麻烦[23]。
2.3. 新陈代谢亢进与高血糖
高代谢发生在中度和重度烧伤中,且随着损伤的深度和大小成正比增加。受伤后的超代谢状态表现为激素、循环系统活动和免疫反应的动态上调,尽管保护作用较弱。严重烧伤后基础代谢率升高,甚至可超过正常值的两倍[24]。儿茶酚胺的释放会升高体温、心率和血压。高代谢状态与糖皮质激素升高相关,糖皮质激素会诱导循环蛋白和脂质的分解代谢。因此,代谢构建单位的快速更替会迅速耗尽其供应,加剧分解代谢状态。资源是内源性产生的,以促进这些高代谢通路——蛋白质合成、脂肪生成、糖新生、激素生成等。肌肉萎缩是这一分解代谢现象的后果,氨基酸的稀缺加上过度的需求,促使肌肉中蛋白质分解以提供氨基酸。治疗应重点缓解新陈代谢亢进,因为这种状态可能持续长达一年。高血糖是严重烧伤的已知后果,原因多样,包括因高代谢导致的糖新生和糖原解率升高,以及细胞内胰岛素抵抗增加。由于循环葡萄糖的大量利用减少,胰岛素抵抗会加重高血糖状态。这种利用不足加剧了蛋白质和脂质通过肌肉萎缩分解,这些脂肪因葡萄糖代谢受损而被用作能量来源。高血糖状态通过抑制免疫反应,损害伤口愈合,导致脆弱的免疫抑制状态[25,26]。
2.4. 烧伤休克
当严重烧伤的系统反应及多器官系统受累表现为灌注不良状态时,可能引发烧伤休克。当器官缺乏灌注,导致功能障碍和细胞死亡时,这被称为休克。休克的原因多种多样,例如感染源的败血症,可能导致器官功能障碍。然而,烧伤休克的独特之处在于其特征是心肌活动下降,同时血管通透性增加,导致循环量和灌注量减少了两倍。心肌活动减少会导致血液、氧气和营养物质循环减少。如前所述,液体转移通过血管通透性增加同步发生。间质和结缔组织的癌压上升,导致液体随之增加,导致周围血管塌陷。最终,这些问题可能导致灌注不良和末端器官缺血,这需要积极复苏以维持循环,同时在需要时输送血液、免疫细胞、营养物质、细胞因子和生长因子有助于对损伤的反应[27]。
2.5. 败血症
烧伤伤口感染很常见,且常常导致侵入性感染。表面积越大、烧伤越深,发展为危及生命的侵袭性感染的风险就越大,进而发展为败血症。败血症是身体对感染的最终反应,也是严重烧伤患者的主要死因。它被定义为“宿主对感染反应紊乱导致的严重器官功能障碍”。败血症通常由细菌感染引起,但也可能由真菌和病毒引起。由于皮肤脱落,烧伤患者的败血症与一般败血症不同,因为只要受伤部位未愈合,感染风险就存在[28,29]。在败血症的病理生理中,人体免疫系统释放内源性DAMPs和外源性病原体来源分子模式(PAMPs),激活抗原呈递细胞和单核细胞表面的Toll样受体(TLR)。这会引发广泛的炎症,引发败血症临床综合征,导致持续的组织损伤,最终导致多器官功能障碍。败血性休克是最后一种、最严重的败血症形式,血压会降到令人担忧的低水平。现代烧伤病房中大多数烧伤相关死亡都是由于败血性休克[30,31]。
3. 先天免疫对烧伤的反应
先天免疫系统及其细胞是身体在烧伤后抵御入侵病原体的第一道防线。先天免疫反应以防御病原体和分解坏死组织为特征,为烧伤后伤口愈合的增生和重塑阶段铺平了道路(见图2)。先天免疫系统的细胞包括中性粒细胞、单核细胞和巨噬细胞、自然杀伤细胞、树突状细胞和肥大细胞,这些细胞共同负责热损伤的急性炎症反应。虽然其中一些细胞是靠近损伤部位的常驻真皮细胞,但大多数免疫细胞是从循环系统及周围血管中招募的[32]。在初次损伤数小时内,血小板脱颗粒释放信号,包括细胞因子、趋化因子和微小RNA,这些信号会招募白细胞到受伤部位,然后激活并调节其功能[33]。白细胞到达后,即中性粒细胞、单核细胞和巨噬细胞以及肥大细胞,释放大量额外的生长因子和信号蛋白,负责空间和时间线适切的增殖和分化调节,以促进伤口愈合过程从止血和炎症阶段进入增殖和重塑阶段(见表1)[34].这些细胞和过程代表了先天免疫反应中细胞介导的部分。相比之下,先天免疫系统通过补体激活发挥体液免疫,目标是针对性病原体的消灭,其实现途径包括经典途径、凝集素途径和替代途径。经典途径使用抗原-抗体复合物,凝集素途径通过甘露糖靶向病原体,替代途径则用于靶向受损组织中的病原体。值得注意的是,这三条通路均在C3复合物处相交,最终形成具有靶向病原体溶解能力的膜攻击复合体。在烧伤中,补体过度激活会导致炎症反应延长。动物烧伤模型显示补体水平增加,即复合物C3、C3a和C5a,这些复合物是三条通路的产物。C3a和C5a均被证明具有止血、抗菌和促炎作用,这些作用对伤口愈合很重要,但当过度激活时则违反直觉(见图1B)[35]。
图2。
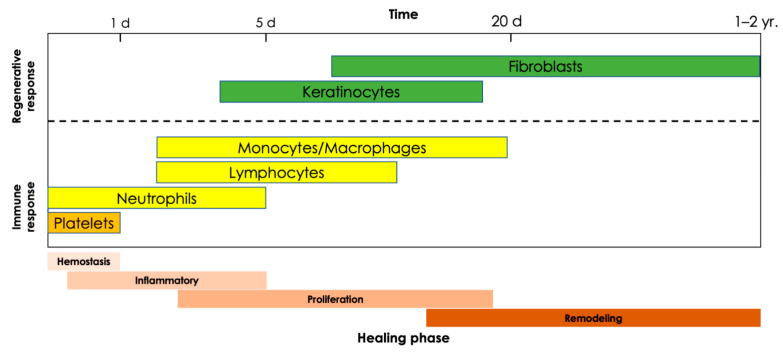
总结了烧伤伤口愈合不同阶段主要的免疫和再生细胞。缩写:d,日;年,年。
表1。
免疫细胞和再生细胞及其在烧伤期间的作用和特性。缩写:GM-CSF,粒细胞-巨噬细胞集落刺激因子;EGF,表皮生长因子;FGF,成纤维细胞生长因子;IFN,干扰素;IL,白细胞介素;KGF,角蛋白细胞生长因子;MHC,主要组织相容性复合体;MMP,基质金属蛋白酶;MSH,黑色素细胞刺激因子;PDGF,血小板衍生生长因子;RNS,活性氮物种;活性氧(ROS);TLR,toll样受体;肿瘤坏死因子TNF;TGF,变革增长因子;VEGF,血管内皮生长因子。
3.1. 中性粒细胞
中性粒细胞是最早响应组织损伤的白细胞,通过上调血管内皮细胞表面的P-选择蛋白和循环血小板,从周围微血管中招募。P-选择蛋白结合中性粒细胞表面,使其在血管内皮上系绳和滚动,然后经过透水进入炎症组织[36]。中性粒细胞到达后具有三个功能:消灭微生物、清除细胞外基质(ECM)以及招募更多炎症细胞(见表1)[37,38]。
中性粒细胞利用吞噬溶酶体,即由吞噬体与溶酶体融合形成的消化囊泡,来中和细菌,进而释放自由基,如活性氧(ROS),并倾向于损伤部位附近的健康细胞[13,38]。中性粒细胞还被证明能通过将入侵微生物困在挤出的组蛋白和DNA细胞外网中来杀死它们[39]。这一程序化过程称为NETosis,常导致细胞死亡,可被微生物或其成分激活,也可被细胞因子和趋化因子激活。有趣的是,细胞外陷阱的形成并非中性粒细胞独有,嗜碱性粒细胞、嗜酸性粒细胞、肥大细胞以及单核细胞和巨噬细胞也可能经历类似的程序性反应[40,41,42,43]。中性粒细胞还负责通过产生基质金属蛋白酶(MMP)、弹性蛋白酶和胶原酶等酶来清除受损的ECM,为未来新ECM的形成铺平道路[38]。最后,中性粒细胞释放多种细胞因子,包括TNF-α、白介素(IL)-1β(IL-1β)和IL-6,这些物质进一步促进炎症,并招募更多中性粒细胞、单核细胞和巨噬细胞到受伤部位,从而延续先天免疫系统的反应[38]。烧伤对中性粒细胞部分伤口愈合的影响包括受伤后前5天迁移速度受阻、中性粒细胞(及巨噬细胞)在受伤后数周的长时间浸润,以及趋化性、吞噬功能和杀菌能力受损[44,45,46]。然而,1970年代对豚鼠的一系列实验表明,去除中性粒细胞并未显著干扰组织修复[47]。最近,糖尿病小鼠中中性粒细胞敲除实验支持了这些发现,并报告称在缺乏中性粒细胞的情况下,伤口愈合的进展实际上更快[48]。这些研究表明,中性粒细胞的作用可能并非先天免疫系统对损伤的炎症反应的关键,因此中性粒细胞所承担的功能可能已被其他白细胞对损伤的反应充分完成,而不会对整体伤口愈合过程造成不利影响。虽然这些发现旨在强调中性粒细胞的具体作用以及不同白细胞之间职能的重叠,但值得注意的是,该理论可能被忽视,即快速愈合并不一定等同于有效或最佳的伤口愈合(见图2和表1)。
3.2. 单核细胞与巨噬细胞
单核细胞是巨噬细胞的前体,这两个吞噬细胞群体在免疫功能调控、清除细胞残骸和组织修复中都扮演着重要角色[49,50]。活化后,这些白细胞暂时保持单核细胞形态,同时分泌促炎和促血管生成因子(如IL-8、IL-1β和TNF-α),随后分化为巨噬细胞[51,52]。这一分化过程部分由微小RNA(如miR-146a)调控,该RNA调节M1和M2表型间巨噬细胞的极化,以平衡促炎和抗炎操作(见图2和表1)[53]。
分化后,巨噬细胞作为吞噬细胞清除烧伤伤口中的受损基质和细胞碎片,包括用过的中性粒细胞和血小板[13,52]。巨噬细胞最初表现出促炎或M1表型,最终转变为抗炎或M2表型[50]。M1细胞被描述为促炎介质的来源,如前列腺素E2、活性氧和氮中间体、TNF-α、IL-1、IL-6和IL-8[38,49]。相比之下,M2表型旨在解决炎症,同时促进愈合级联中的血管生成和缓解,通过产生IL-1受体拮抗剂、PDGF、TGF-β1和FGF等促进ECM产生和血管生成的因子[34,38,49](见表1)。多种信号控制或促成巨噬细胞极化状态。这些重要线索包括细胞的微环境因素(氧气浓度、pH值等)以及代谢底物的可用性[54,55]。鉴于巨噬细胞作为守门人的重要调控角色,为组织愈合提供支持或破坏环境,随着关于巨噬细胞反应性动态调控的更多信息的出现,巨噬细胞谱上更细分的亚型很可能被识别出来[55,56]。
3.3. 肥大细胞
肥大细胞是存在于皮肤真皮层的免疫细胞,促进急性炎症,刺激再上皮化和血管生成,且已被证明在皮肤瘢痕形成中起重要作用[57]。热损伤会导致常驻肥大细胞脱颗粒,进而释放组胺、TNFα、前列腺素、IL-1和IL-6[21,58]。这些细胞因子促进血管通透性增加,从而促进并帮助中性粒细胞和单核细胞招募到受伤部位[59,60]。组胺的释放最终导致活性氧(ROS)的产生增加,并触发P-selectin的快速胞吐作用,P-selectin是一种由活化血小板和内皮细胞产生的蛋白质[61]。同样,肥大细胞释放的TNF-α会上调E-Selectin的表达,E-选择蛋白是一种由内皮细胞产生的受体。P-和E-选择蛋白均有助于改善白细胞在血管内皮细胞腔表面的粘附,从而促进向损伤部位迁移[36]。对这些选择蛋白的敲低实验报告称,伤口闭合显著受损,角蛋白细胞迁移、血管生成、肉芽组织形成、白细胞浸润以及转化生长因子β(TGF-β)和伊尔-6的表达受抑制[62]。这表明肥大细胞信号在有效招募和迁移额外免疫细胞到受伤部位中的重要性。
值得注意的是,肥大细胞不仅存在于免疫系统对烧伤反应的早期阶段,还会在伤口愈合后期被招募到伤口部位,通过产生组织纤溶酶原激活剂和纤溶酶原激活剂抑制剂-1,帮助ECM重塑[63]。肥大细胞还被证明能释放IL-10以抑制过度的免疫反应,以及蛋白酶(如chymase),通过将TGF-β1和MMP-9转化为活性形式,促使成纤维细胞招募[63,64]。沿此,肥大细胞释放血管内皮生长因子(VEGF)、成纤维细胞生长因子(FGFs)和板状衍生生长因子(PDGF),这些因子有助于为伤口愈合修复阶段的损伤部位做准备(见表1)[63]。
3.4. 自然杀手(NK)与树突细胞
自然杀手(NK)细胞是真皮上的先天淋巴细胞,对病原体的破坏和早期免疫反应至关重要。NK细胞与树突状细胞之间存在互惠调控关系,产生独特且强效的激活交叉,负责抗菌防御[65]。NK细胞被I型和III型干扰素(IFN)激活,并在激活后促进II型IFN、IFN-γ和TNF-α的合成[66]。抵达受伤部位后,NK细胞通过细胞溶解活性诱导受感染细胞的程序性细胞死亡,其特征是释放细胞毒性颗粒[67]。一项针对小鼠烧伤模型的研究发现,全层烧伤后NK细胞IL-12和CCL3的产生水平下降,且部分厚度烧伤中这些细胞因子水平较健康对照组更高[68]。CCL3是调节单核细胞和中性粒细胞招募的重要因子,而IL-12则促使树突状细胞释放IFNγ并激活额外的NK细胞[69,70]。这似乎表明从NK细胞的角度来看,全层烧伤会导致白细胞招募功能失调(见表1)。
树突状细胞是吞噬细胞和抗原呈递的真皮白细胞,作为T细胞的“免疫哨兵”,同时增强早期免疫反应并清除细胞残骸[71]。有观点认为树突状细胞通过托尔样受体7和9通过宿主来源的核酸感知皮肤损伤,并通过此过程被招募到受伤部位[72]。与巨噬细胞类似,树突状细胞负责损伤部位受损组织的吞噬作用。研究还显示它们在伤口修复中起作用[73]。如前所述,树突状细胞和NK细胞之间存在互惠激活关系,这种关系通过树突状细胞产生I型干扰素实现,从而激活NK细胞[66,72]。一项小鼠研究强调了树突状细胞在伤口愈合过程中的重要性,该研究发现树突状细胞缺乏的小鼠烧伤伤口闭合延迟。这种伤口愈合受损与早期细胞增殖、肉芽组织形成、TGF-β1水平的显著抑制以及血管生成相关(见表1)[73]。
4. 对烧伤的适应性免疫反应
适应性免疫系统或获得性免疫系统由白细胞组成,称为淋巴细胞,这些细胞又可分为T细胞和B细胞。适应性免疫系统负责识别和消除外来入侵者,即抗原,其对烧伤的反应主要致力于感染控制。适应性免疫系统对这些抗原的反应有两种方式:分别由T细胞和B细胞进行的细胞介导免疫和体液免疫反应。细胞介导的免疫反应涉及通过直接与宿主细胞相互作用激活T细胞,这些T细胞会直接与已感染抗原的宿主细胞相互作用,然后激活巨噬细胞以摧毁入侵的微生物。而体液反应则使用B细胞,B细胞分泌抗体,也称为免疫球蛋白,这些抗体随后结合外来抗原,从而阻断其结合宿主细胞受体并感染其的能力。这些抗体还作为先天免疫系统吞噬细胞的标记,标记这些抗原以致破坏。在全层烧伤破坏真皮层作为保护屏障完整性后,适应性免疫反应通过消除入侵的病原体帮助伤口愈合,同时调节先天免疫对损伤的反应(见图1B)[74]。
4.1. T细胞
T细胞是细胞介导免疫反应的主要淋巴细胞;它们负责增强先天免疫系统并直接防御外来抗原。与大多数其他组织相比,健康的皮肤和上皮具有独特之处,因为它们主要由伽马-德尔塔(γδ)T细胞亚群组成,已被证明具有促进再生能力,并在调节浸润、炎症和烧伤愈合中起关键作用[75,76,77,78]。小鼠烧伤模型的数据发现,受伤初期循环中γδ T细胞水平升高,同时强调其作为趋化因子来源的重要性[79]。该T细胞亚群的重要性再次被观察到缺乏γδ T细胞的小鼠在受伤后头48小时内的高死亡率所凸显[80]。此外,研究表明,这组T细胞在伤口愈合的急性阶段调控髓系细胞和Alpha-Beta(αß)T细胞向伤口部位的浸润,帮助从炎症期过渡到增生期[81]。另一项针对小鼠烧伤模型的研究支持了这些发现,数据显示热损伤后伤口部位有较高水平的αβ T细胞浸润。同一研究指出,该T细胞表型抑制淋巴细胞增殖,同时产生促炎细胞因子,如IL-17,这是一种将T细胞激活与中性粒细胞动员和激活联系起来的关键细胞因子[24]。因此,尽管健康的真皮组织主要含有γδ T细胞,但正是它们在热损伤后招募αβ T细胞,使其成为受伤部位的主导亚群体,从而在伤口愈合早期阶段有利于炎症而非增殖(见表1)。还有其他非常规T细胞亚组,称为黏膜相关不变T(MAIT)细胞和不变自然杀伤T(iNKT)细胞,这些细胞近年来成为许多研究的主题。无论主要组织相容性复合体(MHC)表达如何,它们都会触发快速的免疫反应,最新研究表明这两种细胞类型都可能有能力参与组织修复[82,83,84]。
幼稚的T细胞可以分化为T辅助细胞1(Th1)或T辅助细胞2(Th2)。Th1细胞通常与促炎状态相关,激活和分化后分泌IL-2和IFNγ。而Th2表型则分泌促进细胞凋亡的细胞因子,并产生包括IL-4、IL-5和IL-10在内的抗炎反应,进而促使B细胞产生抗体。此外,还发现了若干额外的T细胞亚群。它们在损害修复和烧伤中的作用正受到深入研究[24,85]。
4.2. B细胞
除了上述细胞因子IL-4和IL-5外,B细胞还能对由树突细胞、单核细胞和巨噬细胞以及内皮细胞分泌的IL-15反应,启动免疫球蛋白或抗体的产生[86]。然而,在烧伤情境下,局部和全身免疫球蛋白或抗体水平在烧伤后48小时内显著下降,部分患者血清水平持续数周保持低水平[87,88]。这表明热损伤后B细胞的作用可能被下调,进一步证明烧伤后感染控制的困难(见表1)。
5. 烧伤的再生反应
对于全层烧伤,表皮和真皮均被破坏,则需要手术治疗,因为烧伤伤口无法自行再生。标准治疗是切除烧伤组织并用自体移植物替代[89]。浅层和部分厚度烧伤可根据正常伤口愈合步骤无需手术愈合。受损组织的修复与炎症期末期重叠,角质细胞和成纤维细胞是主要负责烧伤组织恢复的细胞类型。如其名,增殖阶段的特点是细胞增殖,目标是实现伤口闭合。伤口闭合的特征是受影响皮肤完全重新上皮化,这对恢复皮肤最重要的功能至关重要,包括调节体液以及防止感染和紫外线损伤[90]。在伤口部位形成肉芽组织后,成纤维细胞分泌胶原蛋白,形成新的细胞外基质,而覆盖的角质细胞则迁移覆盖伤口部位。部分厚度烧伤的增生阶段可能在受伤数小时内开始。这最终进入重塑阶段[91](见图2)。
5.1. 角蛋白细胞
角蛋白细胞是表皮中的主要细胞类型,负责新上皮的形成以及烧伤后皮肤屏障功能的恢复。健康未受伤的皮肤由角质细胞维持,这些角质细胞在基底层增殖,随着颗粒层迁移而分化,最终成为角膜层中扁平的死细胞残余[92]。针对烧伤后的表皮损伤,免疫细胞分泌的大量细胞因子和生长因子会招募并激活未受损的角质细胞,促使它们在热损伤造成的表皮缺损处的伤口间隙中迁移[92,93]。角膜细胞通过先松开彼此间的地膜体附着以及半岛体附着于局部基底层,从而实现迁移,从而获得迁移所需的灵活性[94]。生长因子(EGF、KGF、TGF-β、VEGF和成纤维细胞生长因子)、细胞因子(IL-1、IL-6、IL-8和TNF-α)、整合素、角蛋白和基质金属蛋白酶(MMPs)在下方肉芽组织中由成纤维细胞释放,促进角质细胞的增殖和伤口迁移[95,96](见表1)。角蛋白细胞还被证明与成纤维细胞和内皮细胞协同作用,通过释放MSF、NGF、VEGF和GM-CSF等生长因子促进血管生成,并协助卵泡和汗腺再生[97]。角蛋白细胞还通过细胞因子信号传导释放IL-8、IFN-β和TNF-α等因子,参与免疫调控(见表1)[98,99]。
5.2. 表皮干细胞
表皮干细胞存在于表皮附肢(皮脂腺、白皮汗腺和毛囊)。这些包括基底上皮细胞、血皮腺、毛囊细胞、真皮乳头细胞和膨出细胞[97]。在伤口愈合的背景下,这些干细胞超越了其基础自我更新功能,分化并迁移到伤口腔,以帮助急性再上皮化,以应对IL-1和TNF-α信号[99]。抵达伤口部位后,这些细胞释放细胞角蛋白、基底膜蛋白和生长因子,如表皮生长因子(EGF)、TGF-β、VEGF和胰岛素样生长因子(IGF),目的是再生烧伤后受损或坏死的角质细胞、黑色素细胞、毛囊和汗腺(见表1)[97]。
5.3. 黑色素细胞
黑色素细胞根植于表皮基底层,树突延伸至表皮的棘层,负责皮肤色素沉着,进而防止紫外线对皮肤的损伤[97]。烧伤患者常见色素脱落。Carney等(2021)提出,色素脱落是由黑色素细胞低活性或过度活跃引起的,而非烧伤后愈合皮肤中该细胞的缺失或丰盛。除了上述作用外,角质细胞还通过传播损伤相关信号,这些信号被黑色素细胞接收,黑色素细胞再从酪氨酸合成黑色素。黑色素随后被转移回角质细胞,以保护其免受核损伤[100]。然而,烧伤会导致该过程失调,可能通过黑色素细胞的“失活”。Carney等人(2021)提出,这些烧伤后黑色素细胞可以通过α黑色素细胞刺激激素(α-MSH)重新激活,从而恢复色素沉着并增强保护新角质细胞免受紫外线损伤的能力(见表1)[100]。
5.4. 成纤维细胞
成纤维细胞促进伤口愈合和真皮重塑过程中结缔组织的形成,同时也有助于上皮细胞再形成。在伤口愈合的炎症阶段后,成纤维细胞迁移到伤口部位,并开始通过胶原沉积重组细胞外基质。在愈合早期阶段,III型与I型胶原蛋白的生成比例高于成熟疤痕或正常皮肤[101]。随着伤口进展,平衡得以恢复,I型胶原蛋白最为丰富。这些成纤维细胞大多最终分化为肌原纤维母细胞,最显著的是其收缩性表型和α平滑肌肌动蛋白(α-SMA)的表达,后者负责重塑阶段的伤口收缩[102]。在理想的伤口愈合环境中,成纤维细胞和肌原纤维母细胞在细胞凋亡前就已完成其职责。然而,该过程的失调会导致激活时间延长,进而导致挛缩和肥厚性烧伤疤痕的形成[103]。研究表明,长非编码RNA对这一过程至关重要,影响烧伤后真皮成纤维细胞的增殖和凋亡[104,105]。成纤维细胞中这28条长非编码RNA的表达增加促进了自分泌的TGF-β2,进而导致肥厚瘢痕(HTS)和瘢痕疙瘩的形成[106]。尽管如此,已有多种疗法被引入并测试以减轻因成纤维细胞活动引起的HTS相关发病率(见表1)[107]。
6. 烧伤后慢性炎症
如果急性炎症反应对烧伤的反应持续时间延长,可能导致过度愈合。因此,烧伤通过修复而非再生愈合,导致肉芽组织过度生长和伤口收缩,最终形成瘢痕组织[108]。虽然肥厚性瘢痕形成可能发生在任何病因上,但烧伤后尤为关注和关注,因为它加剧功能障碍和美容风险。具体来说,是挛缩、慢性疼痛、瘙痒和不可接受的瘢痕外观。慢性炎症是肥厚性瘢痕的最重要风险因素。炎症反应受损会导致伤口愈合级联反应停滞,间隔不定,但通常发生在炎症期。在持续炎症存在时,形成中的ECM受损,血管生成减少,再上皮化受阻[109]。这导致慢性愈合,随后出现病理性瘢痕,称为肥厚瘢痕或瘢痕疙瘩形成。
肥厚性瘢痕
肥厚型瘢痕(HTS)是指在伤口愈合过程中胶原蛋白沉积过多,导致其相对于邻近正常皮肤呈现凸起的外观,但其边界仅限于受伤区域,且没有过度伸展——这是这类病理性疤痕形成的关键特征。这些伤口通常在约2年后成熟,切除后不再复发。烧伤后挛缩的发生率很常见,有些数据显示其发生率高达30%。这一范围很可能是由于伤势严重时发生率增加,深层和较大的烧伤发生率更高[110]。
从组织学角度看,从最初愈合到最终重塑,HTS所含胶原蛋白密度、肌纤维母细胞和糖胺聚糖(GAGs)密度高于正常瘢痕[111]。有趣的是,HTS这些部分的组成也有所不同。例如,III型胶原蛋白与I型胶原蛋白最初过度生成,尽管两者均产生。随着愈合进展,这一比例趋于正常,成熟时稳定为正常瘢痕水平——分别为I型和III型,约为6:1,[112]。尽管HTS中的胶原蛋白比正常皮肤多,但HTS内的束比正常皮肤更薄,且排列平行于基底膜,没有正常皮肤中存在的网状方向[113]。ECM中其他受破坏的局部因素包括恢复伤口完整性的蛋白质,如弹性蛋白,已证明在严重烧伤且愈合时间延长后数年内缺失,可能促成病理性瘢痕形成[14]。
肥厚瘢痕中的成纤维细胞反映了完整正常皮肤深层网状真皮中的成纤维细胞活性。其特征是前胶原mRNA表达上调,以及与纤维化相关的已知细胞因子(如TGF-ß)水平升高。除了胶原合成和ECM生成相关活性增加外,ECM重塑、胶原蛋白分解和吸收相关因素的表达也有所减少。肥厚瘢痕中的成纤维细胞降低了基质金属蛋白酶-1(MMP-1)活性,从而减少胶原蛋白的分解发生。已知的血管扩张因子一氧化氮水平也较低[114]。这可能导致局部细胞招募减少,因为血流不足。参与恢复和生成正常胶原纤维的蛋白聚糖活性被抑制。这一现象通过减少Decorin的产生被发现,decorin是一种蛋白聚糖,也结合TGF-β——其已知的前纤维化活性因此增强[115]。
损伤位置也与病理性瘢痕形成相关,因为在承受较高张力的伤口中,肌纤维细胞分化被上调,这与肥厚瘢痕形成的发生率增加有关。TGF-β还与纤维细胞生成、迁移及分化至肌纤维母细胞的增加相关,巩固了其在通过基质沉积、纤维化及组织收缩形成的肥厚瘢痕形成中的作用。肌原纤维母细胞在通过微丝束增加和α平滑肌肌动蛋白活性增加的肥厚瘢痕导致的伤口收缩病症中起到很大作用[116]。
炎症细胞的招募也受到影响,尤其关注辅助T细胞(CD4+)。CD4+亚型细胞浸润,与辅助T细胞的1–3型不同,已被证明会导致促纤维化或抗纤维化的创伤环境。1型辅助T细胞产生IL-2、干扰素γ(IFN-γ)和IL-12,这些与抗纤维化和胶原酶活性增加相关。在微环境中推算这一变化表明,辅助T细胞1型亚群的增加有助于重塑和胶原蛋白降解,从而可能抑制肥厚瘢痕的形成。相反,2型和3型辅助T细胞与IL-4、IL-5、IL-10和TGF-β的产生有关。其中亚组与胶原酶活性下降的前纤维化表型相关——这种环境会导致伤口重塑缺乏努力、胶原蛋白退化,并可能形成肥厚型瘢痕[108,116]。旨在用IFN-α拮抗TGF-β活性的治疗方法在局部烧伤和肥厚瘢痕中表现不一。IFN的系统性施药,而非局部注射,也在探索中。IFN-α尚未被持续证明有助于改善结果,其使用仍处于进化阶段,需要进一步研究[117,118]。
7. 缓解烧伤后炎症反应
深层和大面积烧伤是毁灭性的伤害,不仅有局部影响,还会通过严重且持久的炎症反应带来严重的全身性后果。炎症对于烧伤伤口的成功愈合至关重要,但找到合适的平衡至关重要。随着烧伤复苏和护理的发展,炎症的作用不容忽视。本节旨在将一些提出的治疗和复苏方案融入讨论中,特别是与烧伤后炎症相关的内容。
7.1. 烧伤复苏计划
如前所述,对烧伤发生大规模全身性炎症反应的一个后果是血管渗漏的发生。显著水肿由多种因素引发,包括血管扩张、液体渗出以及微血管通透性增加,这些通常伴随炎症[119]。因此,炎症会影响所需的液体复苏需求,但反之亦然。所采用的液体复苏方法有可能减轻或加重烧伤后炎症过程。Gurney等人(2019)主张恢复二战时期使用血浆进行烧伤后液体复苏的标准,理由是可能在烧伤后内皮病中保护糖萼,从而避免炎症性细胞因子进一步渗出和组织水肿加重[120]。同样,研究表明,在复苏阶段给予晶体与促进炎症细胞因子浓度升高相关,进而促进白细胞浸润的粘附分子表达更高[121]。除了所用液体类型外,复苏量在管理炎症和烧伤后水肿时尤为重要,尤其是液体渗出问题。近期研究重点在于优化初始所需液体量以及最适合烧伤患者的解决方案。研究表明,前24小时内的输液量应略高于帕克兰公式的预测值。包括胶体和晶体在内的多种溶液被测试为初始复苏液,研究表明平衡的晶体是最优选择。如今,帕克兰配方仍是烧伤患者首次液体复苏最广泛使用的治疗方法[122]。
7.2. 减少炎症的策略
此外,凝血级联反应与烧伤的炎症反应高度整合,具有相互激活的加剧性潜力。反过来,针对凝血功能障碍可能缓解过度的炎症反应。其中一种提出的机制是抗凝血酶(AT),该药物已在重度败血症患者中被研究[123]。值得注意的是,烧伤患者在烧伤后护理的前24小时内AT水平显著下降,且这种短缺已被证明与多器官衰竭相关,使得替代AT成为烧伤患者的潜在治疗方法[124]。
烧伤通常会持续加重,无法挽救的凝固区不断扩大[125]。因此,表层部分厚度烧伤可能变得更严重。深层部分或全层烧伤会增加烧伤的表面积和深度,进一步导致更严重的全身性和局部症状[126]。多种因素会导致烧伤转化,如组织灌注减少、周围微血管凝固、严重炎症、游离氧自由基和细胞死亡。多项研究表明,通过增加局部灌注、减少炎症或具有抗凝和抗凋亡特性的治疗方法,可以减少烧伤伤口的进展[127]。为增强区域静止的灌注,Battal等人研究了TAK-044(一种内皮素A和-B拮抗剂)对大鼠烧伤进展的影响。结果显示,烧伤后立即静脉注射该分子可增加局部灌注,减少水肿和炎症,显著改善组织存活率[128]。多项研究探讨了抗炎试剂对烧伤治疗的影响。Eski等人(2012)使用局部硝酸铰(CE)在大鼠烧伤后立即减少局部炎症。他们的研究显示,局部使用CE相比对照烧伤能减少炎症并减缓烧伤进展[129]。为了减少凝血和烧伤伤口进展,Yuhua等人(2012)研究了具有抗凝作用的表面活性剂Poloxamer-188(P-188)在大鼠烧伤模型中的效果。每24小时静脉注射P-188的结果显示,该治疗相比未治疗对照组显著降低了二次烧伤转化[130]。Taiara等人(2009)研究了罗格列酮(一种噻唑烷二酮)作为大鼠烧伤模型中凋亡抑制剂的作用。结果显示,口服PPAR-γ-配体(核激素受体)显著降低了继发烧伤转化率[131]。
还有许多针对炎症的治疗方法也被探索过,包括干细胞、类固醇和阿片类药物。尽管其作用机制尚未被完全探索或确立,但骨髓来源的干细胞已被证明能有效调节烧伤后炎症[132]。使用类固醇,如甲泼尼松龙,以及非甾体抗炎药,如酮托拉酸,已被提出并证明能减轻烧伤患者的炎症、疼痛和住院时间[133,134]。同样,局部吗啡已被证明能延缓早期炎症期的起始,同时加速增殖期[135,136]。这些发现得到了早期体外研究的支持,这些研究显示阿片类药物可以刺激角蛋白细胞迁移[137]。尚未开展大规模临床试验评估阿片类药物对伤口愈合的疗效,但其主要作为止痛剂的用途使其成为烧伤患者疼痛管理的主要药物,促使进一步研究的必要性[138,139]。
8. 讨论
以往研究表明,研究已促成了烧伤护理中新颖治疗策略的发展[133]。通过新型治疗方法、替代传统分层皮肤移植(STSG)以覆盖伤口,以及感染控制、液体复苏和营养支持的进步,预防烧伤伤口进展,提高了严重烧伤后的生存率和愈合效果(见表2)[5]。
表2。
烧伤研究推动了烧伤护理中新型治疗策略的发展。通过新型治疗方法预防烧伤伤口进展,采用替代传统分层皮肤移植(STSG)的方法来覆盖伤口,以及感染控制、液体复苏、疼痛管理和营养支持的进步,提高了严重烧伤后的生存率和愈合效果。
烧伤最常见的并发症是感染,感染可能进展为系统性败血症,最终导致发病率和死亡率增加[140,141]。目前的烧伤感染预防和治疗包括多种外用抗菌产品,包括银、碘和蜂蜜,这些通常浸渍在敷料中,如薄膜、泡沫、水凝胶、水胶体和海藻酸盐。局部抗菌剂给药是首选方法,因为它能预防烧伤感染,使得无论血管损伤如何都能直接施药于伤口,这有可能避免全身性不良反应,同时在目标部位保持高浓度[142]。由于微循环紊乱导致组织穿透不良及肾病、神经病变和胃肠障碍等不良副作用,系统性抗生素治疗受限,因此应仅短期使用[143,144,145]。常见的短期使用包括手术前、手术中和手术后,尤其是在重度烧伤患者[146]。作为避免抗菌素耐药性和不良反应的又一尝试,抗菌肽的纳米配方已被评估用于伤口愈合。抗菌肽由皮肤和免疫系统细胞内源性产生,用于对抗病原体,基于其作用机制的治疗方法,主要引入孔洞和破坏细菌膜,已显示出令人印象深刻的效果[147]。未来还需开展研究,以评估高浓度抗菌肽纳米制剂作为控制释放治疗大面积烧伤感染控制的疗效。此外,研究表明内源性气态小分子介质一氧化氮(NO)具有抗菌活性,参与止血、炎症、血管和表皮通透性调控,以及细胞增殖和组织重塑的调控[148,149,150,151].NO由内皮细胞和炎症细胞在生理条件下和多种病理生理状态下产生。在伤口补充NO以控制感染、促进血管生成以及促进伤口修复和再生,已显示出令人鼓舞的效果[151]。然而,在设计和针对NO释放伤口愈合治疗药物时,必须考虑NO高度依赖的Janus面部行为[152]。
如前所述,烧伤不仅会造成局部伤害,还会在身体各处造成严重的系统性损伤。因此,烧伤研究也关注改善系统性反应的治疗方式。对重大烧伤进行的长期且严重的全身性炎症反应可能导致血容量低和灌注不足,称为烧伤休克。毛细血管通透性增加会导致大量血管内容积不足,因此需要立即进行液体复苏和密切监测静脉输液量,确保足够但不过量,以防止死亡。液体复苏主要在患者深度低血容量和心脏功能障碍的前24小时内提供支持[153]。心脏抑制是多因素的,机制上与带有β-肾上腺素能受体的儿茶酚胺过度刺激有关,并引发多种下游效应,同时也涉及促炎细胞因子TNF-α。长期增加儿茶酚胺已被证明会破坏细胞内钙止血,抑制最佳心脏功能[154]。TNF-α效应已被充分研究,已被证明能引起负向肌萎缩并诱导心肌细胞凋亡,这既与一氧化氮无关,也与一氧化氮相关[155]。低血压可能因心脏活动抑制以及前述的多种同时因素引起。然而,另一个重要的血管压介质是NO。NO合酶2活性使NO水平升高会诱导血管扩张,可能导致随后的低血压[155]。
此外,严重烧伤后可能持续一年以上,会出现显著的高代谢反应。该状态表现为循环量异常增加,严重代谢、生理、分解代谢和免疫系统紊乱[15]。在严重烧伤期间及之后需要营养支持以满足代谢需求,因为未能满足增加的能量和蛋白质需求可能导致多器官功能障碍、感染易感性增强甚至死亡[156]。挑战在于,对于严重烧伤患者,由于精神状态改变、吸入损伤导致肺功能或胃肠功能障碍以及进食不耐受,口服所需的营养量通常难以承受[157]。烧伤护理的进步推动了针对高代谢反应的药物治疗方式的发展。例如,每日服用合成代谢类固醇,如奥桑德龙(一种睾酮类似物),已被证明能改善烧伤患者的肌肉蛋白降解并减少减重[158]。最有效的抗分解代谢治疗是普萘洛尔,一种β受体阻滞剂。长期使用已被证明能降低心率、肝脏脂肪浸润以及烧伤后降低血糖所需的胰岛素量[159]。然而,高代谢反应的生理结构复杂,营养支持的最佳路径、体积和成分尚未完全明了。因此,营养治疗应在恢复过程中个性化、监测和调整[24]。
9. 结论
烧伤是由于能量向身体快速传递不同大小,导致皮肤和皮下组织细胞破坏的结果。烧伤的影响可能超出局部受伤区域。严重烧伤中长期且强烈的免疫反应会引起多种系统性影响,损伤血管、心脏、肺、肾及其他器官。此外,烧伤部位的持续炎症可能导致肉芽组织过度生长和伤口收缩,最终导致瘢痕形成,疤痕可能造成毁容、功能受限,甚至可能需要修复手术。轻微的浅表烧伤通常按照正常伤口愈合步骤愈合良好。深层、严重的烧伤需要手术治疗才能愈合。对烧伤病理生理学及身体对严重烧伤的系统反应的深入理解,促使烧伤护理取得了进步。





