
作者:Craig G. Crandall, 1 Matthew N. Cramer, 1 and Karen J. Kowalske 2
1University of Texas Southwestern Medical Center and Institute for Exercise and Environmental Medicine, Texas Health Presbyterian Hospital, Dallas, Texas
2Department of Physical Medicine and Rehabilitation, University of Texas Southwestern Medical Center, Dallas, Texas
Corresponding author.
摘要
在美国,每年都有数以万计的人因烧伤而住院治疗。深度烧伤的治疗通常包括皮肤移植,以加速愈合并降低感染风险。移植程序导致受伤和随后被清除的宿主部位与放置在该部位顶部的皮肤移植物之间的物理破坏。神经和血管连接必须发生在宿主部位和移植物之间,才能对皮肤血流进行神经调节。此外,这种烧伤损伤区域的排汗冷却实际上是不存在的,导致体表大部分烧伤的个体的体温调节反应严重受损。烧伤后的住院治疗可能持续数周至数月,此类损伤的心血管和代谢后果可能会对烧伤幸存者出院后数年产生不利影响。在这种背景下,本文的目的是讨论1)我们目前对皮肤移植的生理学和相关后果的理解,2)皮肤移植对传出体温调节反应的影响以及与全身体温调节有关的相关后果,3)可以降低烧伤幸存者过度高温风险的方法,4)烧伤的长期心血管后果,以及5)烧伤幸存者可以在多大程度上“正常化”其他受损的心血管反应。我们的主要目标是引导读者理解严重烧伤会导致严重的生理后果,这种后果可能在受伤后持续数年。
关键词:有氧能力、烧伤、体温调节
严重烧伤的流行病学
在美国,每年约有150000名烧伤患者在急诊室接受治疗,其中40000至70000人住院治疗(1-3)。美国烧伤协会报告称,这些住院患者中约有16%的烧伤覆盖了20%或更多的体表面积(BSA;4)。军事冲突也是烧伤相关伤害的重要来源,因为5%-20%的战场伤害与烧伤有关(5-7)。25年前,50%BSA烧伤患者中有一半以上没有存活,而目前90%BSA烧伤的患者仍在存活(8)。因此,目前有更多的人(即数十万人)生活在比以往任何时候都更大比例的BSA烧伤中。
转到:
植皮
严重的皮肤烧伤(定义为深度2度或3度烧伤)通常需要切除大部分或全部真皮,因为切除过程的目的是切除所有无法存活的皮肤。因此,烧伤越严重,皮肤会逐渐脱落。由于体温调节所需的附件(即皮肤血管和汗腺/导管)包含在真皮内,这些附件通常在严重烧伤的皮肤中受损,因此在切除过程中被切除。如果有足够的未受伤皮肤可用,则将采集这种皮肤,通常将其网状以增加表面积,然后用于覆盖新切除的烧伤损伤区域。这种自体皮肤移植物通常分为中厚或全厚,中厚移植物是烧伤最常见的移植物。对于分层移植物,将所有表皮和真皮上部从供体部位移走,然后移植物到切除的受体部位。这与全厚自体移植物形成对比,全厚自体移植将整个真皮和表皮从供体部位移走,并附着在烧伤部位。由于真皮附属物,如汗腺的分泌线圈,位于真皮层深处,如组织学评估所示,分层移植物通常不包含这些附属物。
供体皮肤的生存能力取决于来自清创受体部位的血液供应,以及在整个恢复期内尽量减少感染和适当的营养摄入。血管重建和血管生成发生在移植组织中的血管发芽和出芽(。根据移植物的厚度,通常在移植后的第4至第7天恢复一定程度的循环。在愈合良好的移植皮肤中,清晰的脉冲同步血流反应证明了这种血运重建(图1)。
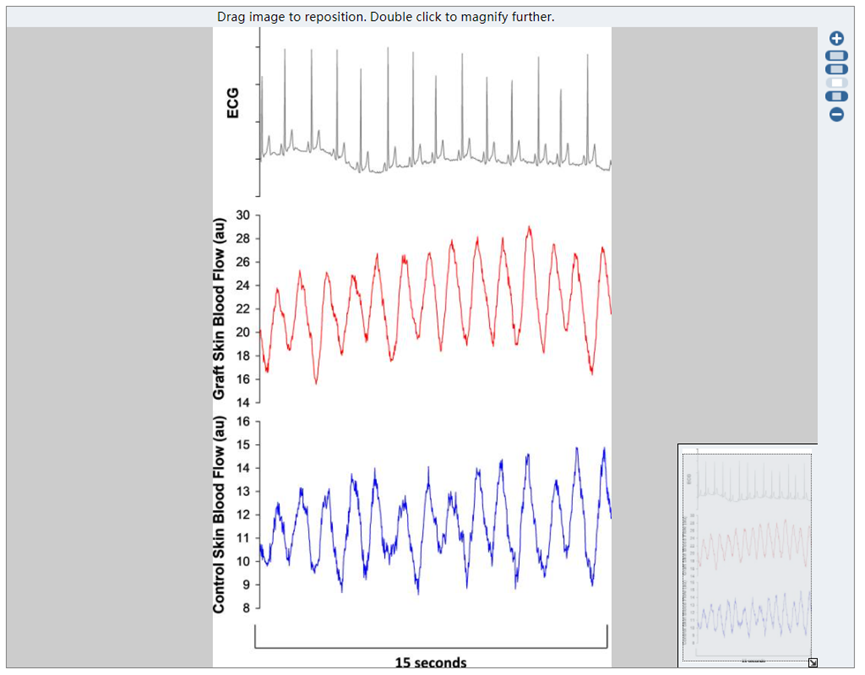
图1。覆盖有中厚移植物的全层烧伤和邻近未受伤“对照”部位的心电图(ECG)和皮肤血流反应。注意两个部位的皮肤血流与心电图之间的同步性。在上下肢和躯干区域,无论男女,早在烧伤后5个月以及烧伤后数年,都观察到了类似的反应。Crandall实验室未发表的观察结果。
移植皮肤的神经再支配
尽管收获的和随后移植的皮肤显然是血运重建的,如图所示。移植皮肤中的血管在多大程度上重新神经化,这是神经介导的皮肤血流控制所必需的,但仍不清楚。由于它与温度调节有关,皮肤血流的神经控制通过两种不同的交感神经途径进行。一种途径,通过交感血管收缩神经,与大多数区域循环中发现的途径相似。在寒冷暴露期间,皮肤交感血管收缩神经活动增加,导致皮肤血管传导率下降(阻力的倒数),其次是去甲肾上腺素和协同递质的释放。皮肤血管传导率降低会导致皮肤血流量减少,减少血液与环境的热交换。这种皮肤血管收缩系统是中性和凉爽环境中体温调节的重要机制。控制皮肤血流的第二个系统是非肾上腺素能交感神经活性血管舒张系统,它只存在于少数物种中,包括人类。负责皮肤主动血管舒张的神经递质仍然未知,尽管这种神经递质可能是一种与交感胆碱能神经中的乙酰胆碱共释放的肽。尽管在常温期间处于静止状态,但在核心体温升高期间,皮肤活性血管舒张系统介导了85%-95%的无光泽(即多毛)皮肤的皮肤血流量增加。这种由神经介导的皮肤血流量的大幅度升高是将热量从个体核心转移到环境中所必需的。重要的是,在失神经的皮肤中没有主动的皮肤血管舒张;因此,一个功能正常的皮肤交感神经系统对热暴露期间的适当体温调节反应至关重要。
Freund等人最初研究了烧伤和随后的移植对移植区域神经再支配和血运重建的影响。他们确定了烧伤幸存者,他们的手臂周围烧伤,并用中厚移植物进行了移植。使用静脉闭塞体积描记术,他们评估了受伤皮肤通过水灌注服方法对全身热应激进行扩张(需要如上所述的功能性神经支配)的能力。需要强调的是,评估的前臂区域没有与热源接触,因此移植皮肤中皮肤血流的任何变化都需要进行功能性神经再支配和血运重建。这些研究人员报告了6名受试者中的3名受试对象的适当反射诱导的皮肤血管舒张。作者没有推测这些异质反应的原因。Auklick等人在烧伤后9-107天对烧伤幸存者提出了类似的问题,其中一些受试者因受伤接受了皮肤移植,而其他受试者则没有。当直肠温度升高0.4–0.5°C时,“大面积腿部烧伤”(超过腿部烧伤的35%)的患者腿部血流量没有增加,而“小面积腿部烧伤(小于腿部烧伤的5%)的患者的腿部血流量增加与未烧伤的对照组参与者相似。
鉴于这些混杂的发现,我们试图更好地理解移植皮肤的皮肤血管系统的神经控制。这些研究的主要方法是招募烧伤患者,这些患者需要随后进行皮肤移植,理想的候选者是在非烧伤部位附近移植烧伤,这样在热激发过程中可以同时评估两个区域的反应。测试了三个相互关联的假设:1)烧伤和随后的皮肤移植会减弱移植皮肤中的皮肤血管舒张和出汗反应,2)移植的皮肤对局部刺激(如连接后反应)和神经介导的皮肤血管舒张(如连接前和连接后反应的组合)的血管舒张和出汗反应受损以及3)移植的“成熟度”将有利地影响皮肤血管舒张和汗液反应。
皮肤移植与体温调节反应
根据Freund等人(30)的上述研究,我们使用水灌注服方法将烧伤幸存者暴露在全身热应激下。简单地说,46–50°C的水通过参与者穿的西装灌注,这显著提高了水灌注西装下的皮肤温度,并最终提高了体内温度。与Freund等人的研究一样,接受评估的移植和非移植皮肤区域没有与水灌注服接触,因此只有在皮肤血管系统的交感神经支配完整的情况下,皮肤血流量才会增加。一名受试者的皮肤血流反应如图所示。注意,在热应激之前,移植区域的皮肤血流略高于相邻的未受伤皮肤,这一发现在评估的队列中是一致的。随后的全身加热使未受伤部位的皮肤血管传导率(CVC)增加了约三倍(例如,ΔCVC 1.28 ± 0.16AU/mmHg),而移植皮肤的CVC与预热水平保持相对可比性(例如,ΔCVC,0.24 ± 0.11 AU/mmHg)(图3,左)。与这些皮肤血管反应一致,与邻近的未受伤皮肤相比,在这种热应力期间,移植皮肤基本上没有出汗的增加(图3,右)。
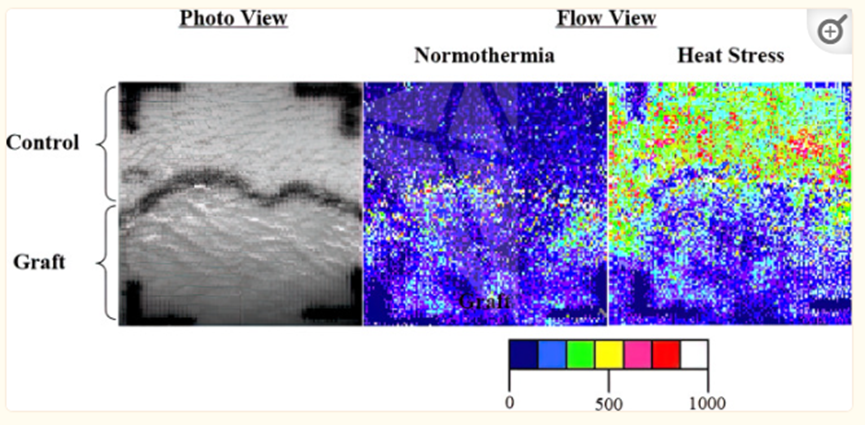
图2:来自烧伤幸存者的激光多普勒图像,在常温和全身热应激期间,来自未受伤(对照)皮肤和相邻皮肤移植区域(全层烧伤,覆盖有中厚移植物)。照片中的黑线描绘了未受伤区域和移植区域之间的边界。在常温下,与未受伤部位相比,移植部位的皮肤血流量通常升高。然而,在热应激过程中,移植部位的皮肤血流量没有明显变化,而未受伤部位的皮肤血流则大幅增加。参考标尺描绘了与从0到1000的灌注单位相关联的颜色。早在受伤后5个月和受伤后数年,两性都观察到了类似的反应。图经许可从Crandall和Davis处重新发布。
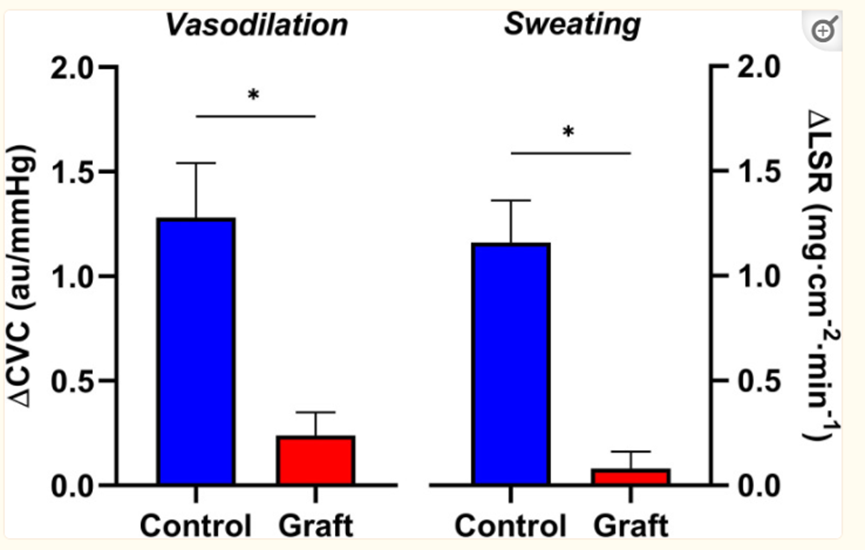
图3由于全身加热,对照(蓝柱)和移植(红柱)部位皮肤血管传导率(ΔCVC)和局部出汗率(ΔLSR)的变化。注意到在接枝位点ΔCVC和ΔLSR的高度显著衰减*P<0.05。该图中的数据来自Davis等人。(34)经牛津大学出版社许可,代表了烧伤后5-9个月,男性和女性手臂和腿部用中厚移植物覆盖的全层烧伤的反应。随后在损伤后数年的移植皮肤中观察到类似的反应。
评估皮肤血管收缩剂对间接全身冷却(例如,冷却皮肤,但不是评估皮肤血流的区域)和直接局部冷却的反应性的随访研究显示,移植皮肤对这两种冷却刺激的血管收缩功能都得到了保留。综合来看,这些数据表明,移植的皮肤大大减弱了散热反应,同时保持了保温反应。这些观察结果令人感兴趣,因为它们表明皮肤血管收缩肢体具有适当的神经再支配和连接后反应性,而对皮肤活性血管舒张肢体的相关神经递质的再支配和/或反应性受损。
移植皮肤对局部刺激的皮肤血管扩张和出汗反应,例如连接后反应
在完成上述研究
中的全身加热方案后,将移植和非移植部位局部加热至42°C,并在该温度下保持30分钟,这可以评估皮肤的最大扩张能力。尽管移植皮肤对这种局部加热刺激的平均CVC反应比未受伤部位低约25%,但这种差异在统计学上并不显著。Aulick等人也没有观察到烧伤和未受伤腿部在局部加热过程中血流量增加(通过静脉闭塞体积描记术测量)的任何差异。一个显著的区别是,这些参与者在受伤后仅6–21天,尚未接受皮肤移植,这与我们的工作形成了对比,在我们的工作中,参与者在受伤5个多月后接受了完全愈合的皮肤移植。
为了评估移植皮肤降低连接后反应性的程度,这可能有助于降低皮肤对热应激的血管舒张和出汗反应,我们采用皮内微透析将药物局部输送到皮肤中,同时评估皮肤对这些药物的血流量和出汗反应(见图4;。在该方案中,输送了两种药物:乙酰胆碱,主要通过内皮依赖性机制引起皮肤血管舒张,硝普钠,主要通过非内皮依赖性机理引起皮肤血管扩张。此外,当功能性汗腺存在时,乙酰胆碱通过汗腺上的毒蕈碱受体刺激出汗。虽然乙酰胆碱的给药增加了两个部位的CVC,但这种增加在移植部位明显减弱,因此在最高剂量的乙酰胆碱下,移植部位的CVC比相邻的未损伤部位低约60%(图5,左)。有趣的是,CVC对逐渐增加剂量的硝普钠的反应显示出非常不同的模式,因为在移植部位和未损伤部位之间没有观察到“统计学上显著”的差异。然而,在最高剂量的硝普钠下,移植部位的CVC增加降低了约30%(图5,右)。对这些发现的解释是,移植皮肤减弱了内皮依赖性血管舒张反应,而通常保留了内皮非依赖性血管扩张反应。关于出汗,无论乙酰胆碱的剂量如何,在移植部位都没有观察到出汗的迹象,而在未受伤部位,在更高剂量的乙酰胆碱下观察到剧烈的出汗。这些观察结果与分层移植皮肤中缺乏功能性汗腺的组织学结果一致。
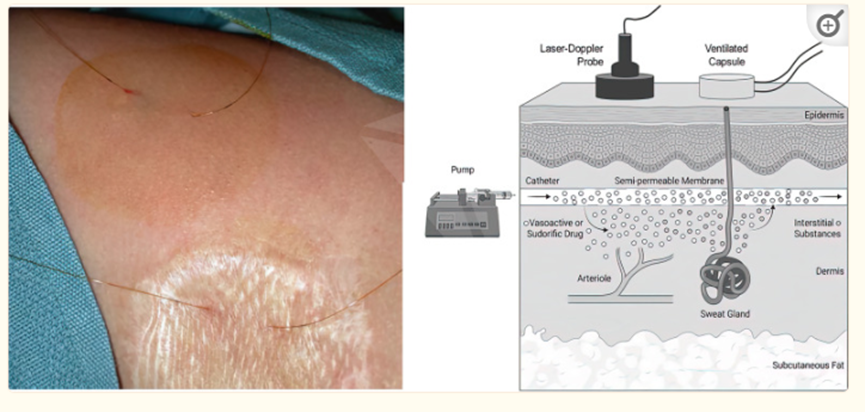
图4。左图:微透析探针插入未受伤皮肤和植皮片的照片。右图:真皮空间内微透析探针的示意图。通过泵给药的药物从半透膜处的微透析探针中移出,对从皮肤表面测量的皮肤血流和出汗反应产生影响。使用http://BioRender.com制作并经许可发布的图像。
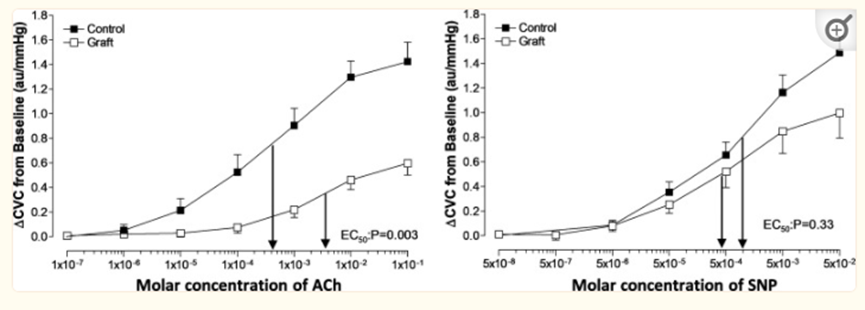
图5。通过皮内微透析在未受伤(对照)和移植部位给药的乙酰胆碱(ACh)和硝普钠(SNP)剂量增加引起的皮肤血管电导(ΔCVC)变化。注意嫁接部位对Ach反应的深刻差异,但对SNP反应的差异较小。我们对这些数据的解释表明,移植皮肤减少了内皮依赖性皮肤血管舒张。经牛津大学出版社许可,修改自Davis等人(33)的图。
移植皮肤成熟度对皮肤血管扩张或出汗反应的评估
在上述关于移植皮肤连接前/连接后反应性的研究中,这些数据是在评估前6-9个月在烧伤和随后移植的个体中获得的(。这一系列研究中调查的最后一个问题是,在烧伤和随后的移植后的几年里,皮肤血管舒张和出汗反应性是否有所改善。为了研究这个问题,我们比较了在评估前6–9个月、2–3年和4–7年遭受烧伤和随后移植的个体对被动热应激(通过水灌注服)和局部乙酰胆碱和硝普钠给药(通过皮内微透析)的皮肤血管舒张和出汗反应。尽管数据明显更具异质性,但总体反应与之前的观察结果相比没有变化;也就是说,无论损伤的持续时间如何,移植的皮肤在损伤后7年内都会减弱皮肤血管舒张反应,并且没有大减弱出汗反应(图6)。我们实验室随后对数十年烧伤患者进行的大量研究强烈表明,这些受损的皮肤血管舒张和出汗反应将在患者的一生中持续存在。
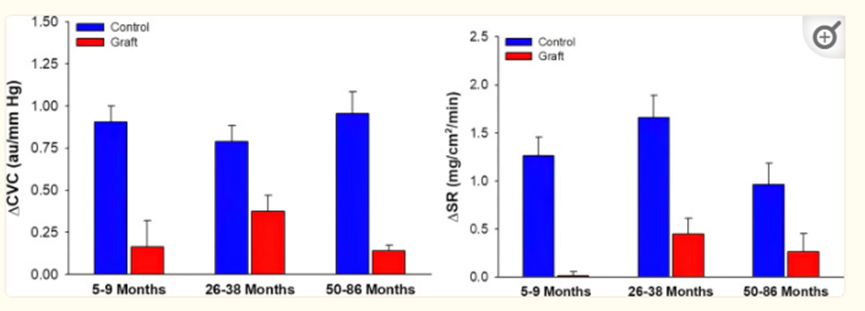
图6。皮肤血管传导率(ΔCVC)和出汗率(ΔSR)在未受伤(蓝色柱)和移植(红色柱)后5-9个月、26-38个月和50-86个月对全身热应力的变化。注意损伤后数年ΔCVC和ΔSR反应的持续衰减。经牛津大学出版社许可,转载自Davis等人(35)。
烧伤和随后的皮肤移植对全身体温调节的影响
在我们的实验证明移植皮肤的血管舒张和出汗反应受损之前,一些实验室试图确定这种烧伤对中等至高温环境条件下运动的内部体温反应的影响。这些研究的结果通常喜忧参半,一些研究发现烧伤幸存者的核心体温过度升高,而另一些研究则没有观察到这种反应。夏皮罗和他的同事们对这个问题进行了最全面的研究。他们评估了两组烧伤幸存者,其中一组(n=4)有48.6的深度二级和三级烧伤 ± 3.6%的BSA和另一个(n=6)具有覆盖23.7的烧伤 ± 3.1%的BSA。烧伤在植皮或“自发上皮化”后完全愈合。还包括一个未受伤的对照组(n=10)。受试者在40°C和50%相对湿度的环境中,在工作台上/下进行有节奏的踩踏。感兴趣的主要变量是衰竭时间、直肠温度和心率。高烧伤组受试者在97分钟结束运动 ± 28分钟,而低烧伤组的受试者在163分结束运动 ± 10分钟,非烧伤对照组的所有受试者完成了整整3小时的运动。值得注意的是,高烧伤组运动1小时后的直肠温度和心率更高(38.4 ± 0.03°C和158 ± 7次/分)与其他两组相比,低烧伤组(37.95 ± 0.07°C和105 ± 6次/分)和未烧伤(37.76 ± 0.05°C和110 ± 5次/分)组。在我们的实验室中,在更大的烧伤幸存者队列中观察到了类似的反应(n=34),他们的皮肤移植覆盖了他们体表面积的17%-75%,愈合良好;也就是说,与未烧伤的对照受试者相比,移植>40%BSA的烧伤幸存者的胃肠道温度升高到生理上不可恢复的运动热应激的90分钟大约高出两倍。该研究还评估了表达烧伤损伤的各种方法(例如,以平方米为单位的移植或非移植皮肤面积或占总BSA的百分比)与随后胃肠道温度升高之间的关系。我们发现,非移植皮肤(即可用于蒸发散热的皮肤)的绝对表面积(m2)与运动结束时胃肠道温度升高的幅度最为密切(r2=0.41;P<0.001)(43)。这并不奇怪,因为蒸发热损失的绝对容量(以瓦特为单位)与具有完整汗液功能的皮肤的表面积成比例。
值得注意的是,在我们小组进行的这些和随后的研究中,轻度/中等强度运动期间,即使在炎热的环境条件下(例如39°C),核心温度的升高在前30分钟的运动中也没有什么不同,无论烧伤的程度如何。鉴于目前的体育活动指南建议成年人每周至少进行150分钟的中等强度运动,这些发现很重要,可以分为每天30分钟。因此,烧伤幸存者,无论损伤大小和热环境如何(在合理范围内),如果他们每次坚持30分钟或更短时间,都可以实现中等强度体力活动对心血管和代谢的益处,而不会有过度高温的风险。
在与渥太华大学的Glen Kenny博士及其同事的合作下,我们探索了烧伤幸存者在高温运动期间身体核心温度指数升高加剧的相关机制。该方案使用直接量热法比较了一名烧伤幸存者和两名未烧伤女性之间的全身蒸发热损失,前者接受了覆盖75%BSA的愈合良好的中厚移植物,后者的年龄、身高、体重和最大有氧能力与烧伤幸存者相似。每个参与者在35°C和25%相对湿度的量热计中以约400 W的代谢热产生率锻炼60分钟。烧伤幸存者的总蒸发热损失率仅达到热平衡所需的59%,而未烧伤的对照受试者达到了92 ± 热平衡所需的3%(图7);即,烧伤幸存者的蒸发热损失率降低了~47%。有趣的是,烧伤幸存者表现出对环境的干热损失,可能是由于平均皮肤温度过高(比环境温度高约1.5°C)和蒸发冷却率较低,而对照受试者表现出从环境中获得的干热。然而,由于蒸发热损失在这种环境中的重要性,在60分钟的运动结束时,烧伤幸存者的核心体温升高是未烧伤个体的两倍多。尽管样本量很小,但这些令人信服的数据有力地表明,移植皮肤中汗液的减少/缺失是烧伤幸存者体温调节受损的主要机制。
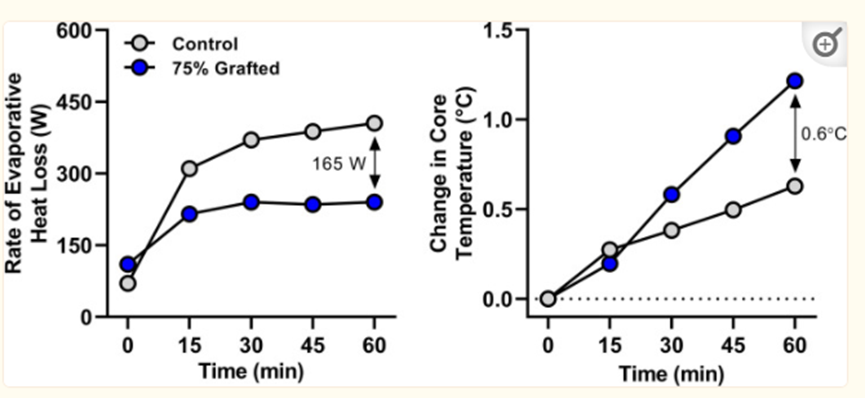
图7。在35°C和25%相对湿度的环境中,一名体表面积为75%的烧伤幸存者(蓝色数据点)和两名性别、年龄、身高、体重和最大有氧能力(灰色数据点)匹配的未烧伤个体在60分钟的运动中的蒸发热损失率(左)和核心温度变化率(右)。我们提出,烧伤幸存者蒸发热损失的衰减率是运动结束时核心温度过度升高的主要机制。通过遥测药丸从胃肠道测量核心温度。经牛津大学出版社许可,Ganio等人重新绘制的数据。
供体部位与体温调节功能
尽管先前的切片清楚地表明移植皮肤的体温调节功能受损,但尚不清楚供体部位是否会表现出类似的受损反应。将表皮和真皮部分切除,然后放置在烧伤部位。这些供体部位最终愈合,甚至可以多次采集同一供体部位用于皮肤移植。
我们的实验室首先通过评估全身被动热应激期间的局部出汗率(电容湿度计)和皮肤血管舒张(激光多普勒技术)来检查供体部位的体温调节反应。与邻近的未受伤皮肤相比,供体皮肤的基线CVC、被动加热期间的ΔCVC和局部加热期间的最大CVC没有差异。此外在供体之间观察到局部出汗率的类似增加(1.04 ± 0.15 mg·cm−2·min−1)和未受伤部位(0.84 ± 0.17 mg·cm−2·min−1)。当随后在移植物成熟期对这些反应进行比较时,在术后2-3年和4-8年,供体和相邻未受伤皮肤之间没有观察到局部出汗率和CVC的差异,这表明热损失效应器反应在移植物收获后几年仍能得到适当的维持。
在最近的一项研究中,我们进一步研究了在非胶囊化运动热应激过程中供体部位的体温调节功能。这项工作的动机是2017年美国陆军的《医疗健康标准》,其中包括在考虑烧伤对入伍或继续服役的影响时捐赠场地的大小。具体而言,这些指南指出:“之前的烧伤(包括供体部位)涉及40%或以上的体表总面积不符合标准”,这假设供体部位的体温调节功能受损。然而,鉴于没有证据支持这些指南,我们试图确定供体部位在与军事训练和行动更相关的热应激条件下是否表现出受损的体温调节功能。与我们被动加热研究的结果一致(,在高温环境(-40°C,21%RH)下运动时,供体和未受伤皮肤部位的局部出汗率或皮肤血流量(通过激光多普勒成像评估)没有明显差异。这些发现表明,在评估烧伤对全身体温调节反应的影响时,不应将供体部位包括在内,因为这些皮肤区域具有适当的散热反应。
环境温度和运动强度对烧伤幸存者全身体温调节的个体和交互影响
提供烧伤幸存者体温调节反应受损证据的大部分数据是在35°C或更高的环境温度下获得的。出于这个原因,我们开始了一项方案,以评估中等强度运动期间烧伤大小和环境温度对核心体温反应的交互影响。我们假设,在相对温和的环境条件下,烧伤较大的人能够在身体核心温度没有过度升高的情况下进行体育活动。为了实现这一目标,我们模拟了未烧伤个体的烧伤,方法是用吸收性、不透气的材料覆盖他们的皮肤,防止覆盖区域的任何蒸发冷却。使用这种方法,我们能够模拟在温和(25°C,20%RH)和炎热(40°C,20%RH)环境中运动时,精确覆盖20%、40%和60%BSA的烧伤损伤的影响,并比较对未受伤对照条件(即0%BSA)的生理反应。这种实验方法的优势在于,它最大限度地减少了受试者之间的可变性,因为每个参与者都进行了全部八次运动(在两种环境中的每种环境中都有四次模拟烧伤情况)。在所有试验中,受试者以固定的代谢热产生率运动60分钟[6 W/kg体重;6.1 ± 0.7代谢当量(METS)]。与在实际烧伤幸存者中观察到的情况一样,在40°C的环境条件下,40和60%BSA模拟烧伤试验的核心体温升高明显高于未烧伤(0%BSA覆盖率)试验。相反,当在温和的环境条件下锻炼时,模拟烧伤试验之间的核心体温升高没有差异(图8)。我们得出的结论是,在中等强度的运动中,只有在环境温度升高的条件下进行运动时,覆盖超过20%BSA的烧伤才会导致核心体温过度升高。作为心血管压力的标志,心率反应与核心温度反应一致,因此在高温下运动期间,与0%BSA烧伤试验相比,40%和60%BSA模拟烧伤试验的心率高出25+次/分。在温和条件下运动期间,只有在60%BSA模拟烧伤试验中,心率的升高才高出~10次/分。这些发现对烧伤幸存者的康复具有重要意义,因为无论烧伤的大小,他们都可以在温和的环境条件下(例如,在空调空间中)进行中等强度的运动,而不必担心核心温度过高。
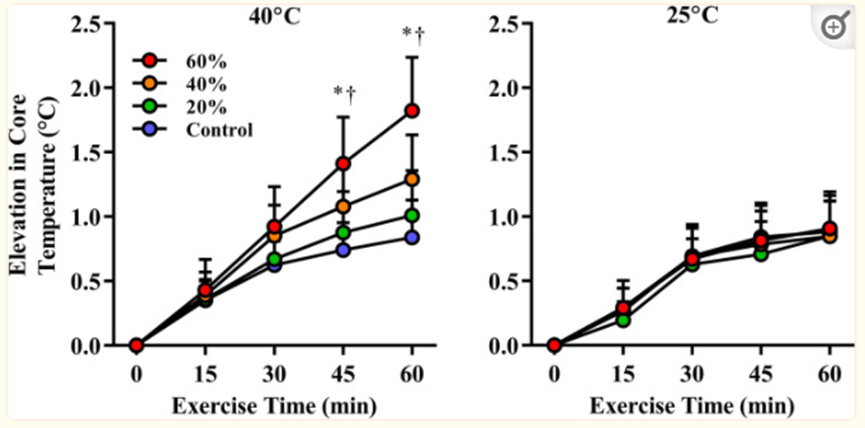
图8。在40°C(左)和25°C(右)的环境中进行60分钟的运动,模拟烧伤覆盖了每个人体表面积的0%(对照组)、20%、40%和60%,核心温度升高。请注意,当在25°C环境中进行运动时,在40°C环境下以相同的代谢热生成速率进行的核心温度过度升高会被消除。通过遥测药丸从胃肠道测量核心温度。经Wolters Kluwer Health,股份有限公司许可,由Cramer等人(47)修改的图。本信息并非旨在或暗示作为专业医疗建议的替代;不应在任何医疗紧急情况下使用,也不应用于任何医疗状况的诊断或治疗。所有医疗紧急情况请拨打120。
本信息并非旨在或暗示作为专业医疗建议的替代;不应在任何医疗紧急情况下使用,也不应用于
任何医疗状况的诊断或治疗。所有医疗紧急情况请拨打120。
烧烫伤康复一站式解决平台,烧烫伤压力衣定制,硅酮支具定制,3D面罩定制,烧烫伤残疾康复整形重建咨询。24小时求助定制微信电话 18116590229 24小时求助定制电话 18116590229




