摘要
在大部分历史时期,严重烧伤占据身体表面大部分面积几乎是必然的死刑,因为随后的感染。多种因素如皮肤屏障的破坏、烧伤环境中细菌营养素的易得性、烧伤皮肤的血管供应破坏以及全身性疾病,导致免疫抑制作用共同作用,使烧伤特别易感染。20世纪,抗生素和抗真菌药物的引入、可用于烧伤的局部抗菌剂的使用,以及早期切除和移植的广泛应用,都极大地提高了生存率。然而,微生物对抗生素及其他抗菌药物耐药性的持续增加,促使人们重新寻找预防和对抗烧伤感染的替代方法。本综述将涵盖已获批或申请的专利策略,涉及新型外用药剂、制剂及对抗烧伤感染的方法。讨论了用于临床前研究的动物模型。各种银制剂(纳米晶和缓释)是许多方法的主流,但抗菌肽、局部光动力疗法、壳虫制剂、新型碘递送配方、噬菌体疗法以及蜂蜜和精油等天然产品都已经过测试。这一活跃的研究领域将继续提供用于烧伤的新型局部抗菌剂,以对抗日益增长的多重耐药性。
关键词:烧伤感染、多重药物耐药性、动物模型、生物发光成像、纳米晶银、抗菌肽、皮肤替代品、千万岁、光动力疗法
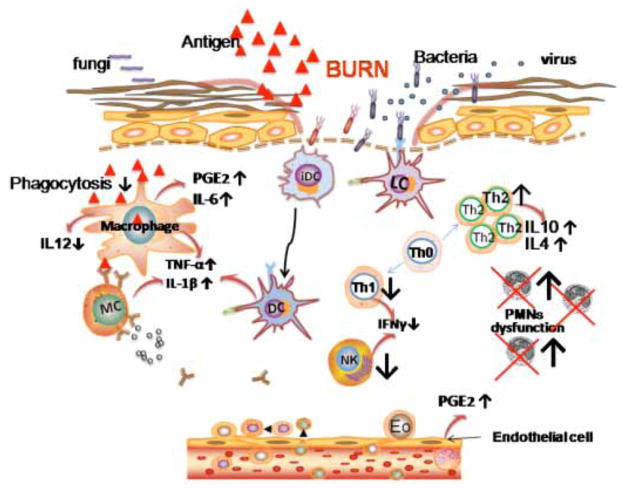
尽管目前已有多种局部治疗方案旨在消除烧伤伤口中的细菌负荷,败血症仍是全球烧伤病房死亡的主要原因[1]。复苏、手术管理、感染控制、超代谢反应控制和康复技术的进步,使烧伤死亡率和发病率在过去60年中取得了显著改善[2]。感染是烧伤的主要并发症。感染与皮肤机械完整性受损以及全身免疫抑制相关的抗性受损有关。皮肤屏障被焦痂取代。这种潮湿、富含蛋白质的无血管环境促进微生物生长。免疫细胞的迁移受阻,中间体释放阻碍免疫反应。由于缺乏活性,肠痂也限制了系统性抗生素的分销。 烧伤按深度和严重程度分为1度、2度、3度和4度,见图(1))。一级烧伤通常仅限于红肿(红斑)、白色斑块和受伤部位轻微疼痛。这些烧伤仅涉及表皮。二度烧伤表现为红斑,伴有皮肤浅层水疱,涉及浅层(乳头状)真皮层,也可能波及深层(网状)真皮层。三度烧伤是指表皮因皮下组织受损而丧失。烧伤患者会表现出焦化和表皮严重损伤,有时还会出现硬痂。四度烧伤会损伤肌肉、肌腱和韧带组织,从而导致焦化和皮下组织的灾难性损伤。 脚上1度、2度、3度和4度烧伤的相对深度。 烧伤还可以以全身表面积(%TBSA)来评估,即部分厚度或全层烧伤的影响百分比。九法则被用作快速且实用的估算受影响TBSA的方法。更准确的估计可利用Lund与Browder图表,考虑成人和儿童身体部位比例的不同[3]图。(2)儿童烧伤超过10%或成人超过15%的烧伤,因存在低血容量性休克风险,应在烧伤病房接受正式的液体复苏和监测。 这些数据用于计算烧伤影响的身体表面积百分比,并评估其预后和感染易感性。 严重烧伤的皮肤失去了其自然的保护和屏障功能,导致水分流失剧烈增加,并可能成为细菌入侵的门户。烧伤后促炎级联反应的激活似乎对后续免疫功能障碍、肠道细菌易位、败血症易感性和多器官衰竭的发展至关重要。局部烧伤反应不仅涉及直接组织凝固,还包括烧伤组织转化,即受损细胞非恢复而是进入细胞死亡,延长了原始损伤的深度和严重程度[4]。全身性烧伤反应由皮肤屏障的丧失和伤口血管活性介质的释放以及随后的感染驱动。当烧伤面积超过约25%的身体表面时,间质性水肿会在远处器官和软组织中出现,主要由伤口释放介质和低蛋白血症的结合继发[5]。热损伤会导致促炎细胞因子大量释放,这些化学介质包括组胺、补体、花生四烯酸、凝血级联产物和氧自由基,这些物质会增加血管通透性,导致低血容量和急性肾衰竭[5]。这可能因系统性炎症反应综合征和明显的免疫抑制而复杂化。随后的伤口感染和胃肠道细菌易位会促进败血症[6]。这又增加了最后一条通向多器官衰竭和死亡的常见路径(Fig)。(3)。 白介素-1(IL-1)和肿瘤坏死因子α(TNFα)由多种细胞产生。前列腺素E2(PGE2)和IL6的产生受到内皮细胞和巨噬细胞的上调,而巨噬细胞分泌的IL-12量减少。T辅助细胞开始优先分化为Th-2细胞,产生抗炎细胞因子IL-4和IL-10。尽管中性粒细胞数量较高,但严重热损伤后中性粒细胞功能障碍仍会发生,而巨噬细胞吞噬作用较低。 表1[7–15]列出了导致侵入性烧伤伤感染的微生物种类[16]。还指出了这些物种中抗生素耐药性的发生率。 导致烧伤感染和耐药性发生的病原体微生物学 美国烧伤协会的一次共识会议制定了关于烧伤中定植(几乎所有烧伤)与感染(可能致病)之间的区别的指导方针[17]。最严重的微生物感染被归类为“侵袭性”。这一特性取决于烧伤的严重程度以及微生物种类或菌株的毒力。毒力是多种因素的综合作用,包括对烧伤的定殖能力(包括与宿主细胞和组织的粘附)、蛋白水解酶的表达、从宿主获取营养的能力以及逃避宿主免疫反应的能力。 侵蚀或感染烧伤的微生物物种有一个相当可预测的时间历程[18]。在热刺激下存活的革兰氏阳性菌,如位于汗腺和毛囊深处的葡萄球菌,会在最初48小时内大量定殖伤口表面。最终(平均5–7天后),烧伤会被宿主正常胃肠道和上呼吸道菌群或医院环境中的其他微生物定殖。这些病原体包括革兰氏阴性菌,而酵母和真菌则是最新的定殖者。这三类致病微生物的细胞壁结构如图所示。(4)。结构差异在很大程度上决定了许多抗微生物药物的相对有效性,这些药物会破坏细胞壁的完整性,进而破坏细胞膜。 革兰氏阳性菌、革兰氏阴性菌和真菌具有不同的细胞壁结构,这些结构决定了它们对不同抗菌剂的敏感性。 烧伤环境的许多生理特征易感染,并抑制传统系统性抗生素的治疗效果。热损伤导致微血管的破坏,使得烧伤被视为非血管组织。烧伤中蛋白水解和脂解上调[19]。基质金属蛋白酶的显著增加(抑制剂减少)会导致蛋白质分解,从而为微生物提供更多营养,使微生物更容易进入组织。 免疫抑制在烧伤感染易感性方面起着重要作用。先天免疫和适应性免疫系统都参与免疫抑制。先天免疫是在微生物入侵后立即触发,响应大量微生物中高度保守的结构;而适应性免疫则是T细胞和B细胞的功能,其中少量被特定抗原选择性激活以克隆式扩散,这一过程至少需要三到五天才能显现。热损伤后先天免疫系统的改变包括中性粒细胞、巨噬细胞、单核细胞、嗜碱性粒细胞、NK细胞和补体。相比之下,热损伤与源自细胞因子网络、内分泌系统以及介导免疫抑制的花生四烯酸级联反应有关。最初,严重烧伤的免疫反应是促炎反应,但后来主要转向抗炎反应,以维持体内平衡和恢复正常生理功能。烧伤后抗炎反应及随后的免疫抑制表现为一组相反的细胞类型和细胞因子。许多细胞因子水平的变化反映了烧伤后适应性免疫系统的改变,更具体地说,发生在T淋巴细胞群体中。 细菌易位是另一种由烧伤与微生物损伤结合引起的生理反应,易发生败血症[18]。“细菌易位”一词用来描述可存活的常驻细菌从胃肠道进入通常无菌组织,如肠系膜淋巴结及其他内脏器官。许多全身性压力可能破坏肠道黏膜屏障,如择期腹部手术、器官捐献者及肠梗阻患者、结直肠癌、缺血再灌注损伤、休克和胰腺炎。[20]在大鼠模型中显示,烧伤和肠球菌感染的两次损伤会增加肠道通透性和革兰氏阴性败血症。 全球范围内日益增长的抗生素耐药性问题没有缓解迹象,当前被称为“抗生素时代的终结”[21]。评论者认为,如果不采取措施,过去只需简单抗生素治疗即可轻松治疗的轻微感染,未来可能会变得几乎无法治疗,就像抗生素被发现之前那样[22]。耐药性被归因于抗生素的广泛非处方供应、错误的处方操作(例如对呼吸道病毒感染开抗生素)、患者依从性低导致过早停止治疗以及牲畜饲料中抗生素的过度使用[23]。如表1所示,抗性在烧伤病原体中也变得普遍。 鉴于上述因素,外用抗菌制剂被特别用于预防和治疗烧伤感染,相较于其他可能易感染的创伤性、外科和医学适应症。糖尿病、血管性和压疮等慢性伤口等不愈合伤口也是类似的症状[24]。许多药物设计用于预防性使用,以防止感染发展,而另一些则旨在杀死感染发生时烧伤部位内正在增殖的微生物细胞。表2[25–80]列出了用于烧伤的局部抗菌治疗剂,构成本综述的主要内容。由于许多外用剂涂抹在烧伤表面,如果设计为主动杀微生物,必须考虑这些剂能穿透到烧伤感染组织以到达入侵的微生物细胞的程度。Stephanides等人[81]测量了多种药物(硫酸根大霉素、醋酸马非奈德、硝基呋喃酮、波维酮碘、硝酸银和磺苲嗪)穿透烧伤残痂的程度。已有研究探讨“增强穿透性增强剂”(甘油、生理盐水、十二烷硫酸钠、乙醇、己烷乙醇、乙酸乙醇二甲基硫氧化物、甘氨酸和萜烯)增强多种抗菌剂进入三级焦痂的能力程度灼烧。在局部抗菌药物领域,另一个重要的考虑因素是对微生物细胞的选择性与对宿主细胞和组织的细胞毒性之间的区别。许多抗菌剂,如局部抗生素[84]、防腐剂[85]、银制剂[86, 87]、抗菌肽[88]、抗菌光动力疗法[4, 89],都被研究是否可能对皮肤及其他人体细胞产生毒性。 本综述涵盖的用于烧伤的局部抗菌治疗剂总结 几十年来,动物作为烧伤感染模型一直是烧伤感染研究的核心部分。通过建立类似人类的烧伤感染,可以研究感染发生的原因,最终目标是寻找预防感染的方法。用于烧伤模型的动物种类包括老鼠、老鼠、兔子以及猪,烧伤的手段包括开水、乙醇浴、加热黄铜块等多种方法。 动物烧伤感染的严重程度以及动物是否发展为败血症并死亡,主要由以下因素决定(除其他因素外):施加在伤口上的细菌数量、特定细菌菌株的毒力、伤口面积占总表面积百分比(TBSA)、细菌是否被涂抹在表面或注射在烧伤部位内或下方, 以及加热物体或液体与皮肤接触的时间长度(决定了全层还是部分厚度的烧伤)。 大约40年前的1968年,梅森和沃克开发了一个用沸水造成热伤害老鼠烧伤模型[90]。这是首个用于研究的动物模型烧伤,并被美国陆军外科研究中心(位于德克萨斯州圣安东尼奥)作为标准烫伤模型用于多项研究[90]。燃烧装置由一个薄金属半圆柱体制成,半圆柱体中央部分切割出一个计算出的孔径。孔径尺寸的选择是为了满足已知体重动物所需的燃烧规模(该方法允许的燃烧上限约为TBSA的30%)。麻醉动物背部被剃毛,然后仰卧放置于燃烧装置中。暴露的区域浸泡在沸水中。据报道,10秒暴露产生全层燃烧,3秒钟产生部分厚度燃烧。烧伤本身并未严重影响行动能力,动物们吃喝都很轻松。该模型被广泛应用于烧伤感染的研究,包括烧伤感染中的细菌易位[91]、用于消除烧伤中多重耐药细菌的抗菌肽开发[92]、预防烧伤感染的创口敷料开发[93]等。 Stieritz 和 Holder 报告了小鼠乙醇浴烧伤模型[94]。该型号使用了体重22–24克的雌性CF1小鼠。老鼠背部被麻醉并剃毛。一块石棉板,窗户约占TBSA的30%,被牢牢压在老鼠背部。乙醇均匀涂抹在窗边的区域,点燃后燃烧10秒。感染由烧伤部位立即皮下注射100 CFU铜绿假单胞菌引发。感染迅速致命,动物在感染20小时后显得奄奄一息。 Stevens等人[95]通过在剃毛小鼠背部一个抬高的皮肤夹片两侧施加两块预热黄铜块(92–95°C)对面,持续5秒,开发了一种全层烧伤的小鼠模型。该程序如图所示。(5)。使用体重25–30克的六周大雄性CD1小鼠。黄铜块面积为1.8厘米×1.8厘米,相当于TBSA的5%。烧伤后,焦痂立即被皮内注射10–106 CFU的P. aeruginosa。单纯烧伤存活率为100%,感染性烧伤为60%。未烧伤肌肉中24小时内均检测出P. aeruginosa(稳定为108 CFU/g组织),涵盖所有不同细菌接种。 将两块预热的黄铜块压在剃毛小鼠背部高起皮肤褶皱的对侧,随后局部涂抹盐水中悬浮细菌。 Bahar等人[96]用体重250–300 克的雄性Wistar鼠开发了部分厚度烧伤模型。麻醉后,将一块2.5厘米×2.5厘米、5毫米厚的吸绒布浸入沸水中(100°C)覆盖背部。热布会在不同时间间隔上铺设。该方法产生了可靠的表浅和深层皮肤烧伤,这一点从组织学特征中得到了证实。 Suzuki等人[97]描述了一种基于皮肤接触玻璃腔体的烧伤模型,玻璃室中水以预定温度循环。这使得在恒定压力10 g/cm2下施用。该模型的最大优势在于可以根据研究人员的需求调节温度和暴露时间,并且可以施加更高或更低的接触压力。 Contag等人[98]开发了一种方法,利用发光的基因工程细菌配合灵敏的低光成像相机,实时监测活体动物感染伤口中的细菌数量和存活能力。在底物存在下,荧光素酶的周转速率使得实时测量成为可能,该酶在哺乳动物体温下具有活性。该方法相比传统的存活或体液采样及随后的装甲和群体计数有了显著改进。第一种方法缺点是浪费动物,且未能真正解决细菌在动物体内的位置;而第二种方法的缺点是组织采样会引入另一个实验误差源,且过程繁琐且无法获得实时结果。 想象系统 图。(6a)我们实验室使用的设备[99]包括一台ICCD光子计数相机(Hamamatsu Photonics,新泽西州布里奇沃特),安装在一个密闭样品室中,配备发光二极管,该装置可捕捉到整只小鼠的背景灰度图像。通过积累包含二元光子信息的多张图像(积分时间为2分钟),生成了伪色发光图像。将该图像叠加到灰度背景图像上,可以获得光子数位置和强度的信息,图。(6b)。相机还通过图像处理器(Argus-50,滨松光子学)连接到计算机系统。使用Argus-50控制程序(滨松光子学)获取图像并处理所收集的图像数据。整个伤口光子计数被量化为相对发光单位(RLU),并以假色标显示,范围从粉色(最强)到蓝色(最弱)。另一款流行的生物发光相机是由Caliper Life Sciences(马萨诸塞州霍普金顿)制造的体内成像系统(IVIS)[100]。 (A)适合对小动物进行体内生物发光成像的低光照相机图像。(B)感染生物发光金黄色假孔杆菌小鼠背部三度烧伤示例,显示光子强度的颜色查找表。连续拍摄了感染(C)P. aeruginosa、(D)Acinetobacter baumannii、(E)金黄色葡萄球菌(E)和(F)白毛念珠菌(Candida albicans)生物发光菌株的代表性小鼠烧伤的连续生物发光图像。 图(6C)展示了代表性小鼠烧伤的连续生物发光图像,分别感染了P. aeruginosa、Acinetobacter baumannii、Staphylococcus aureus和Candida albicans菌株。对于P. aeruginosa感染,该感染为急性且致命,小鼠在感染后第3天死亡。对于慢性的鲍曼酵母、金黄色葡萄球菌和白锥菌感染,感染时间分别为20天、17天和14天。 20世纪80年代,针对F73患者大规模烧伤早期覆盖且自身皮肤资源不足的迫切需求,促使皮肤替代疗法主要作为实验疗法出现[101]。大量研究和试验表明,使用皮肤替代品有助于烧伤愈合,并降低感染风险。需要强调的是,这些产品并非活性抗菌剂,而是作为生物相容性屏障,防止感染[102]。尽管如此,它们常被拿来与标准抗菌剂AgSD比较。使用后,烧伤愈合部位的弹性和柔韧性得到了显著改善,疤痕挛缩减少,减少了疤痕挛缩手术的数量,并减少了长期所需的整形外科重建 大多数儿童烧伤为中等深度的小烧伤,仅需局部治疗。使用皮肤替代品消除了更换敷料和反复前往医院诊所的需求。这有助于避免疼痛和情感创伤,并促进一种成本效益高的管理方式,使得无需进一步治疗,孩子也能不受限制地恢复日常生活。 合成皮肤替代品包括Duoderm(聚氨酯和水胶体)、Opsite(聚氨酯薄膜)、Omiderm(丙烯酰胺薄膜和含聚氨酯的羟基甲基丙烯酸酯)。生物合成皮肤替代品(如胶原蛋白与合成材料结合)包括Biobane(硅胶膜、尼龙、胶原蛋白衍生肽)和Transcyte(含成纤维细胞的聚合物)。生物皮肤替代品包括同源皮肤、猪皮、胶原蛋白衍生物、人类羊膜和培养异体移植。 Duoderm是一种水胶体制剂,提供湿润环境,促进伤口愈合,并防止感染,该部位于1985年获得专利[25]。Martin等人[103]研究了Duoderm对儿科部分厚度烫伤的影响。分析了248例儿童烧伤,采用Duoderm管理的患者移植物率显著降低。 Omniderm(ITG实验室,加利福尼亚红木城)由一种水汽渗透的聚氨酯薄膜组成[27]。Eldad等人[104]研究了Omniderm作为需要皮肤移植的烧伤伤口接口的应用,特别是在细菌污染严重的区域和伤口上。他们得出结论,与类似条件下的其他敷料相比,改善率约为75%。 Suprathel®(PolyMedics Innovations Gmbh,德国斯图加特)是一种可吸收的合成伤口敷料,具有天然上皮特性[28]。它由聚乳酸酯、碳酸三甲二酯和ε-caprolactone的共聚物组成。涂抹后会变得透明,便于近距离监测伤口。Schwarze等人[105]评估了Suprathel对部分厚度烧伤伤口愈合的影响。研究纳入了30名二度烧伤患者,平均年龄为40.4岁。烧伤伤由随机选择,部分用Omiderm治疗,部分用Suprathel治疗。他们得出结论,Suprathel对部分厚度烧伤伤的伤口愈合和疼痛减轻有良好效果,同时显著提升了患者的舒适度。 Epigard是一种两层非药物伤口敷料,功能近似人类皮肤[29]。合成皮肤替代品SYSpur-derm是一种双氨酯聚氨酯泡沫物质[30]。Mahnke等人[106]通过检查23只实验性三度烧伤猪的85份皮肤活检,评估了SYSpur-derm和Epigard的疗效。结论是,这两种材料均表现出卓越的伤口愈合,对伤口表面的附着性良好,且无毒性或抗原效应。 Biobrane(Smith and Nephew 和 UDL Laboratories Inc.)于1989年获得专利[31],由硅胶薄膜与交联尼龙织物结合而成。两层均覆盖亲水胶原肽层,使敷料亲水且与组织兼容。尼龙基质中的血液/血清凝固,从而使敷料能牢固附着于伤口,直到上皮化。Barret 等人[107]假设用Biobrane治疗二度烧伤优于局部治疗。他们得出结论,Biobrane治疗部分厚度烧伤优于使用1%银磺胺嗪的局部治疗。它还显著减少了疼痛、止痛药需求、伤口愈合时间和住院时间。Hassan和Shaw报告[108]使用多孔Biobane导致点状瘢痕,这使得该产品的使用受到质疑。 TransCyte(史密斯与侄子与高级组织科学)是一种源自人类成纤维细胞的临时皮肤替代品,由聚合物膜和新生儿人类成纤维细胞组成,在体外无菌条件下培养于尼龙网上。尼龙网表面覆盖猪皮胶原蛋白,并粘结于聚合物膜(硅胶),涂抹时可获得透明的合成表皮。当成纤维细胞在尼龙网中增殖时,它们分泌人类真皮胶原蛋白、基质蛋白和生长因子。冷冻后,细胞代谢活动不复存在;但组织基质和结合的生长因子依然保持完整。它提供临时保护屏障,且透明,便于直接目视监测伤口床面。Amani等人[26]开展了一项研究,以确定任何大小或病因的部分厚度烧伤是否能缩短住院时间。与接受标准治疗的患者相比,发现了通过皮肤磨皮和换血细胞治疗的患者存在显著差异。作者认为,这种治疗方式比传统治疗更有效,且显著缩短住院时间。 Dermagraft(高级生物愈合)是一种冷冻保存的人类纤维细胞衍生的皮肤替代品;它由成纤维细胞、细胞外基质和1990年获得专利的生物可吸收支架组成[109]。皮肤移植由新生儿包皮组织中的人类成纤维细胞制成,并植入可生物吸收的多格内蛋白网状支架上。成纤维细胞增殖以填补该支架的缝隙,分泌人类真皮胶原蛋白、基质蛋白、生长因子和细胞因子,形成包含代谢活跃活细胞的三维人类皮肤替代品。 Xenoderm和Alloderm(LifeCell, Inc)是从猪皮(Xenoderm)或人类(Alloderm)皮肤中提取的无细胞基质。组织在保留重要的生化和结构成分的同时,经历细胞切除过程[32]。Hosseini等人[110]研究了Xenoderm敷料与1%银磺胺茬(SSD)在部分厚度烧伤中的效果,考虑了伤口感染、住院时间、敷料数量及止痛剂剂量。共考虑了78名患者,其中37人采用每日清洗并使用外用SSD敷料治疗,39人使用Xenoderm。研究结论是,Xenoderm的疗效显著更高。 Apligraf(Organogenesis Inc)作为活体、双层皮肤替代品供应:表皮层由人类角质细胞形成,角质层分化明显;真皮层由人类成纤维细胞组成,形成牛I型胶原晶格[111]。Epicel(基因酶生物外科)是一层厚度从2到8层细胞不等的皮肤细胞片。这些移植物是从患者自身健康皮肤中采集或培养出的邮票大小样本,样本送往GenzymeBiosurgery进行处理。皮肤样本表皮内的细胞通过组织培养分离并生长。在此过程中,使用照射小鼠3T3细胞促进细胞生长,并确保尽快获得足够数量的移植物进行治疗[112]。OrCel(Ortec International Inc)是一种双层细胞基质,其中正常的人类异体皮肤细胞(表皮角化蛋白细胞和真皮成细胞)被分两层培养到I型牛胶原海绵中。供体真皮纤维细胞在胶原基质的多孔海绵侧及内部培养,而同一供体的角质细胞则在胶原基质的涂层非多孔侧培养[113]。 广泛使用有效的局部抗菌剂减少了烧伤表面的微生物负荷,降低了感染风险[33, 114]。选择局部抗菌药物应基于该剂抑制烧伤监测培养中微生物的能力。图中展示了专门用于烧伤局部应用的抗生素的化学结构。(7)。现有专利描述了这些药物在伤口敷料、生物膜和伤口涂层材料、术后粘附剂及美容材料的潜在应用。烧伤病房可轮换使用多种局部抗菌制剂,以减少抗生素耐药性的发展[115, 116]。 醋酸甲苯胺、巴西曲辛、穆匹罗星、新霉素、多米克辛B、硝基呋喃酮、制霉素。 醋酸马非尼德(磺霉菌)乳膏对革兰氏阴性菌,特别是铜绿假单胞菌具有广泛活性,但对革兰氏阳性需氧菌如金黄色葡萄球菌的活性较小[33]。醋酸甲苯酸酯0.5%乳膏(马非奈德)是一种甲基化的局部磺胺化合物。由于外用醋酸麦非奈德膏可以不使用敷料,因此它支持开放性烧伤治疗和定期检查烧伤表面[117]。马芬奈德在银磺胺肼出现之前被引入,并广泛用于烧伤治疗。必须涂抹5%溶液以浸透纱布敷料。以这种方式使用时,溶液的效果似乎与奶油制剂相当[118]。该药应与制霉素联合使用,因其抗真菌活性有限,以防止并发症[119]。在伴有呼吸性酸中毒的烧伤患者中,使用醋酸马非尼德在大面积该化合物上可能致命[120],因为它被转化为对硫氨基万甲酸,导致烧伤患者代谢性酸中毒[33]。 杆菌素是由特雷西芽孢杆菌(Bacillus subtilis var Tracy)地衣目类群生物产生的相关环状多肽混合物,该菌的分离最早于1945年报道[34]。它是磺胺酸盐过敏烧伤患者的良好替代品。当杆菌素锌以约5%至8%浓度局部涂抹于伤口时,能有效促进再生愈合。杆菌素锌可以应用于亲水或疏水载体中,并且有利地浸渍在吸收垫中[121]。 Mupirocin是荧光假单胞菌的发酵产物[35],曾是革兰氏阳性皮肤菌群(如凝血酶阴性葡萄球菌和金黄色葡萄球菌)的强效抑制剂[122, 123]。含有莫匹洛星和氯己定的药物组合物可用于治疗局部细菌感染,特别是感染性烧伤[124]。在北美,莫匹罗星也越来越多地作为烧伤外用剂使用,而MRSA已成为一个问题[125, 126]。最近比较了多种外用抗生素制剂,包括1%银磺胺二嗪、2%穆匹罗辛和2%富西地酸,在MRSA感染大鼠烧伤模型中的抗菌效果[125]。因此,MRSA存在问题的医院可能会轮换使用局部莫匹洛星与其他药物,以减少耐药的发生。 新霉素是一种广谱抗生素软膏,含有三种不同的抗生素:巴西曲素、新霉素和多粘菌素B,采用凡士林基底。一项共计1053名浅表性烧伤患者的研究,定性分析显示金黄色葡萄球菌和铜绿杆菌属是最常见的感染病原。定量上,聚维酮碘加新斯波林组(PVP + N)在治疗后第7天和第18天出现感染的患者数量低于银硫二氮汀组(SSD)。同样,PVP + N的愈合时间也更好,最多患者在15天内愈合。然而,两组的死亡率差异不大[36]。 Polymyxin B是一种简单、碱性的肽类抗生素,通常以软膏基底(白色凡士林)形式获得。多粘蛋白B与磷脂的相互作用使细菌细胞壁能够穿透和破坏,从而影响膜的通透性[37]。据报道,Polymyxin B抑制了PMNs破坏摄入微生物的能力,这可能抑制伤口抑制细菌增殖的能力[127]。考虑到副作用,局部涂抹的多粘蛋白B吸收微乎其微,系统性毒性较为罕见,且通常与长时间在大面积使用有关。如果含有巴奇曲辛,多粘菌素B通过含有表面细菌促进愈合。 硝呋喃是一种对革兰氏阴性菌和革兰氏阳性菌有效的局部抗感染剂。针对侵入性硝基细菌泄殖腔烧伤伤败血症患者的硝基呋喃酮软膏治疗,整体生存率为66%,而文献报告的死亡率为86%[38]。专门用于烧伤患者引入了含硝呋酮的导管[128]。含硝呋酮的导管有效降低了区域烧伤中心导尿管相关尿路感染的发生率。使用这些导管可能在降低烧伤患者尿路感染风险方面发挥重要作用。在对多种抗菌药物耐药性日益关注的时代,硝化呋喃类对已产生抗菌耐药性的生物仍然有效[129]。 尼他丁是对念珠菌的有效杀菌剂。奈抑素由挪威链霉菌产生,通过结合真菌细胞膜中的甾醇具有强效的抗真菌作用[35]。该剂浓度较低时可抑制白色念珠菌,但抑制其他真菌则需更高浓度[130]。霉菌素可以被包裹在脂质体中,最好是稳定的多层囊泡,该囊泡大致包含一个或多个脂质,包括一个或多个磷单甘油、磷脂酸和鞘脂[131]。然而,由于制糖素对细菌无活性,应与具有对多种致病细菌活性的局部药物联合使用,这些细菌会导致烧伤伤口定殖和感染[33]。此外,一项新专利中描述了一种制剂的制剂具有降低毒性[132]。 银的医疗用途至少可以追溯到希波克拉底(被誉为“现代医学之父”[133])时期,他在著作中讨论了银在伤口护理中的作用。到了19世纪末和20世纪初,外科医生通常使用银缝线以降低术后炎症和感染的风险[134]。第一次世界大战期间,士兵们使用银箔来限制和治疗战斗伤口感染[135]。由于抗生素的出现,银在二战期间逐渐废弃。直到1965年,莫耶发表了一篇关于硝酸银抗菌作用的论文,才重新激发了对银抗菌特性的兴趣[39]。如今,银作为预防和治疗伤口、溃疡和烧伤感染的临床治疗重新出现[136]。 市场上有许多不同的含银抗菌剂,包括外用乳膏、软膏和溶液:硝酸银、磺胺医银(SSD)、含硝酸铈的固氨酸,以及更新的缓释银产品[136]。银需要电离才能充分展现其抗菌效果;带正电的银离子容易与伤口液中的带负电的蛋白质结合,从而抑制银离子输送到伤口床。事实上,局部银剂的一个主要问题在于其无法深入组织,且目标区域释放的银含量极低。近年来,为了解决这些问题,市场上推出了多种银制品[137]。无花果。(7)生动地展示了银作为烧伤局部抗菌剂的使用。 胶体银溶液由亚显微的带正电银颗粒悬浮在液态碱中组成。这些溶液一直被广泛使用,直到20世纪60年代莫耶的文章发表[39],之后银盐在临床应用中取代了胶体银溶液。银盐由带正电的银离子与带负电的离子(AgNO3)耦合组成,这种结构比胶体溶液稳定得多。硝酸银是最常用的银盐,在0.5%浓度下具有体外和体内抗菌作用,超过1%时具有显著毒性[138]。硝酸银最常见的方法是通过浸泡纱布外用,然后用于严重烧伤。已有专利用于硝酸银凝胶,声称其更易管理[139–141]。 在烧伤患者中使用硝酸银仍存在争议[40]。硝酸盐对组织和伤口有毒,且会减缓伤口愈合。硝酸盐减少会损害伤口再上皮化,从而部分抵消银的益处。(有趣的是,曾有一项专利用于利用硝酸银作为宫内烧灼剂的毒性[142])。 除了烧伤外,硝酸银还有其他临床用途。传统上,新生儿会滴用1%硝酸银滴剂以预防新生儿结膜炎(ophthalmia neonatorum)。然而,许多医院因担心硝酸银给药后出现化学刺激(及相关的化学结膜炎)而选择使用抗生素(如红霉素滴剂)。尽管有这一合理担忧,Zanoni等人仍然在[143] 发现硝酸银滴剂在预防新生性眼炎方面更有效。 如上所述,随着抗生素的出现,银的使用逐渐废弃。对银的重新关注源于细菌耐药性的快速发展。1970年代,福克斯[144]认为无需在银和抗生素之间做选择;他将硝酸银与抗生素硫二二肼钠结合使用。这种制剂称为银磺胺茬(FlammazineR Silvadene R),受益于银的抑制作用和硫二肼的抗菌作用[136]。银磺胺二氮素(SSD)最初作为软膏制成,后来被掺入亲水性乳膏中[40]。尽管SSD仍是局部烧伤治疗的金标准,但最新研究表明(类似于硝酸银)SSD可能延缓伤口愈合。李秋等人。[145]发现表皮生长因子(EGF)能显著抵消SSD对伤口愈合的有害影响,并认为未来SSD的制备可能与EGF结合使用。SSD相关的另一个问题是细菌对硫二氮素成分的耐药性[146]。已有报道发现抗SSD的假单胞菌属;一项专利获得了专利,用于对抗这些物种,即SSD和钠吡拉西林的结合(后者对铜绿单胞菌非常有效)[147]。其他专利已颁发,涵盖多种SSD递送系统,包括动物组织敷料[148]、水分散型亲水载体[149]和局部喷雾制剂[150]。 1976年,Monafo等人。在SSD中添加硝酸铈用于烧伤伤口治疗,并得出两者具有协同效应[42]。自那时起,硝酸铈-SSD(Flammacerium)被常规用于伤口护理。然而,这种联合配方的有效性存在争议[40]。2005年,Garner等人对相关文献进行了综述,结论是当无法立即切除和缝合时,硝酸铈-SSD可降低严重烧伤的死亡率和发病率[151]。然而,与Monafo提出的假说相反,Garner等人。结论认为硝酸铈抗菌作用极低,其益处主要来自于对烧伤焦痂的作用。烧伤皮肤会产生脂质蛋白复合物,导致烧伤患者的免疫抑制,从而增加感染易感性(以及随之而来的发病率和死亡率)。硝酸铈结合并变性该脂质蛋白复合物,从而阻止免疫抑制[151]。硝酸铈-SSD的多种递送系统已获得专利,包括一种奶油状可分散的亲水性成分[152]。 硝酸银、SSD和硝酸铈-SSD被认为是银产品中的老牌产品。这些是必须涂抹纱布的溶液、盐或化合物。银基沙拉酱是较新的产品,在沙拉酱本身中加入了银[43]。近年来,这类产品激增,制造商也展开了积极的营销活动。多种银质敷料已获得专利,包括Acticoat™、Aquacel-Ag™、Silvercel™和Contreet™等产品。 Acticoat-7(英国赫尔的Smith & Nephew)敷料采用纳米技术:敷料释放出纳米晶体(直径<20纳米)银晶体至烧伤伤口[43]。银晶体以初始大颗粒形式释放,随后持续释放。Fong 等人。[43] 谨慎地得出结论,纳米晶(NC)银不仅减少伤口感染并促进伤口愈合,还能减少换药频率、减轻疼痛程度并降低成本。Gravante等人的荟萃分析。[153] 证实了这些发现,并发现NC银治疗患者感染发生率显著低于使用旧银产品(硝酸银和SSD)的患者。基于此,结论是NC银具有显著更强的抗菌作用,优于旧式银配方。Nucryst Pharmaceuticals Corp.开发的各种NC银敷料和局部制剂已获得大量专利[154–157],该公司后来被Smith and Nephew收购。尽管NC银产品效果令人鼓舞,但纳米晶产物的毒性总体仍令人担忧,这已在体外(但体内未被证明)[43]。 还有其他几种持续释放银的产品,如Aquacel Ag®(ConvaTec,普林斯顿,美国)。离子银被掺入水钢伤口敷料中,接触伤口组织后会变成凝胶状。Barnea 等人。[44] 综述文献,确定Aquacel Ag在急性和慢性伤口中既有效又安全,具有广泛的抗菌特性且无伤口愈合延迟。 Silvercel®(强生)是另一种缓释产品,结合了银的抗菌作用与海藻酸盐的益处[45]。藻酸盐是一种存在于藻类细胞壁中的多糖,能够吸收其体重200–300倍的水,这一能力使其在伤口渗出物管理中尤为有用。Bell 等人。(2007)[158]将Silvercel与Aquacel Ag进行了比较,发现前者在处理渗出物方面更胜一筹,考虑到海藻酸盐强大的吸收能力,这一发现并不令人意外。Silvercel即使在大量湿润的伤口中也能保持形状和强度,这与Aquacel Ag不同。另一方面,Aquacel Ag治疗的伤口较少因过度敷料附着而产生不良反应。 2003年,银藻酸盐泡沫获得了专利[159]。泡沫已成为持续释放银的另一种传递方式,提供了一种更简单、更便捷的施用方式。Jorgensen 等人。[42] 发现Contreet泡沫(持续银释放泡沫,Coloplast)优于Allevyn(无加银的水胞泡沫敷料,Smith and Nephew),使溃疡面积减少幅度比Allevyn的25%高出45%。 已有大量持续释放银释放剂的专利[160–163],此类配方仍处于活跃的研发领域。 在20世纪70年代,人类羊膜作为烧伤患者的可用敷料出现。Sawhney[46]得出结论,这种生物敷料优于传统敷料,因为它促进了快速的再上皮化和伤口愈合。自1978年以来,银被掺入羊膜中,效果显著优于单独使用[164, 165]。一项专利授予了一种由动物组织(包括羊膜)掺入银磺胺嗪的伤口敷料;据称,这些组织上所注入的银比其他含银敷料更多的银[166]。银被摻入羊膜为含银产物增生增加了另一个维度。EZ Derm(Brennen Medical, Inc)是一种改良的猪皮,浸渍了可溶性银化合物,用于治疗烧伤。最初由遗传实验室开发。一项专利描述了EZ-Derm所使用的银[167]。 碘及其抗菌特性已被用于预防或管理伤口感染已有150多年[168]。然而,碘的溶液(酊剂)已被广泛使用的波维酮碘取代,这是一种水溶性化合物,由分子碘和聚乙烯基吡咯里酮结合而成[169]。聚维酮——碘的抗菌作用源于复合物中存在的碘。该溶液对多种细菌、真菌、原生动物和病毒具有活性[170]。一项关于含有聚维酮碘的伤口愈合剂专利描述了抗真菌/抗菌剂(如聚维酮碘)、糖和合适载体的混合物,其基本不致敏,在烧伤或开放性伤口上具有优异的愈合性能,并且在纱布或类似敷料中有效阻碍愈合组织生长[47]。最近一项专利[171]描述了一种装置,用于原位制备由聚维酮碘和类固醇或非甾体抗炎药组成的药物混合物。 聚维酮碘(PVP-I)与脂质体的结合,将防腐物质的微生物杀灭活性与脂质体的耐受性和免疫原性低结合起来;此外,脂质体为伤口环境提供湿润分子膜。一项关于不同含PVP-I脂质体水凝胶配方在深层皮烧伤伤口中疗效和耐受性的动物研究显示,伤口愈合质量良好,肉芽组织平滑,炎症减少,伤口收缩减少,且无角化反应性过高,尤其是3%PVP-I脂质体配方[49].Repithel(Mundipharma Research GmbH & Co. KG,德国林堡/拉恩)是一种新型脂质体水凝胶PVP-I配方,旨在提供湿润的伤口愈合环境,具备抗感染和清创特性。Repithel在吸烟者烧伤中显著的积极作用(因为吸烟和过度炎症对伤口愈合有类似阻碍作用)[172]。有一项专利[173]描述了一种干脂质体PVP-I组分,旨在实现存储稳定封装。 甲德克聚体碘(Iodosorb, Smith and Nephew)是一种含碘的亲水淀粉,适合用于静脉溃疡等颗粒性伤口。然而,碘素或“碘载体”的制剂在较长时间内释放的碘含量较低。卡德克聚体碘是一种缓释抗菌剂,能够吸收多余的伤口分泌物,同时在伤床中提供持续的碘含量。甲胺聚体碘在体内对金黄色葡萄球菌和耐甲氧西林金黄色葡萄球菌(MRSA)也已证明有效。碘需要水分才能活化,类似于含银离子产品。共有61名慢性静脉溃疡门诊患者参加了一项随机选择性交叉试验,使用甲来南聚体碘或标准敷料治疗溃疡。两种治疗效果均显著,但用甲氧酶包扎的溃疡上皮再次显著加快[174]。一项近期专利描述了一种改进的卡德纳聚体碘制备方法[175]。 一项专利描述了含碘衍生物,包括用于耳科和鼻部感染的游离碘和碘仿[176]。罗多福是一种强效的杀菌剂,其成分还含有一种或多种抗炎剂以及一种或多种天然或合成化合物,这些化合物具有镇痛效果。另一项专利(3M Innovative Properties Company,明尼苏达州圣保罗)[177]描述了含有碘和糖醇和/或糖醇的液体防腐剂,主要用于组织消毒。碘灭™绝(Biomedical Development Corporation,德克萨斯州圣安东尼奥)由单碱性碘盐、含有最多八个碳原子的有机酸(如柠檬酸、抗坏血酸或草酸)、氧化剂(如过碳酸钠或过硼酸钠)以及水性缓冲剂组成[50]。将这些成分混合后,生成一种生物相容的抗菌配方中的碘。另一项专利[178]描述了一种稳定的水性碘基杀菌剂组成,包括碘、一种非离子表面活性剂(如聚氧乙烯、多氧丙烯嵌段共聚物)以及一种可溶于碘的卤化物离子(氯离子或溴化物)。 光动力疗法(PDT)[179]是在100多年前通过观察无害光敏剂(PS)和可见光在体外结合杀死微生物时发现的[180]。正确波长的光会激发PS到其激发单重态,进而通过系统间穿越到长寿命激发三重态。在氧气存在下,三重态PS将能量传递给基态分子氧(三重态),产生能够杀死微生物细胞的活性氧(如单重态氧)[181]。无花果。(9)。生动地展示了抗菌PDT的作用机制,并强调其广谱活性,因为能够有效杀死或灭活所有已知的微生物病原体类别。自发现以来,PDT主要被开发用于癌症、眼科疾病和皮肤病学[179]。然而,近年来由于多种病原体类别药物耐药性的不可避免地增加,PDT的抗菌作用兴趣重新燃起[182]。已有大量研究[183]开发和完善具有特定分子特性的PS,能够选择性地使目标微生物细胞失活,且对宿主细胞的损害最小。本节讨论的几种PS的分子结构见图。(10)。大多数强效抗菌性PS(PS)整体上具有正电或阳离子电荷,这种电荷可能由四元化的氮原子(具有固态阳离子电荷)或具有pKa的碱性氨基提供,使其在细菌或感染组织中占优势的pH值下带正电荷。 光敏剂被正确波长的光激发至三重态,然后将其能量传递给分子氧,形成活性氧物种,这些物质能够杀死所有类型的致病微生物。 这些分子具有固有的阳离子电荷或碱性氨基。甲苯胺蓝O(TBO)、阳离子富勒烯(BF6)、阳离子卟啉(XF73)、间基单苯基三(N-甲基-4-吡啶)-卟啉(Sylsens B)、聚乙烯胺氯(e6)共轭物(PEI-ce6)、阳离子邻苯氰酸(RLP068)、硒苯并(A)苯氧嗪氯化物(EtNBSe)。 Nifantiev等人[184]获得了带有光敏剂(PS)的分子偶联物专利,这些分子能够选择性结合微生物表面,在照射后实现光破坏。这些共轭物的关键是一个特殊的间隔器,将至少一个PS(PS)连接到微生物受体(载体)。具有亲水结构的间隔器,如乙二醇单元和氨基羧基端盖乙二醇单元,用于将载体与PS连接。使用了金黄色葡萄球菌、绿色假珠菌和大肠杆菌等细菌物种来测试轭轭物的有效性。研究发现,这些结合物在真实患者相关环境中,血液、血清及其他体液始终存在,能够有效抑制这些细菌。 Hasan等人为抗微生物PDT申请了另一组PS偶联物的专利[185]。这些方法涉及将PS共价连接到“非配对成员”(NPM)部分。该NPM可以是线性、分支或环状多肽,包含一个小的抗菌肽(AMP)(见本综述后文部分)。组蛋白、防御素、天井素、母菌素、革兰氏阳性细菌素和肽类抗生素可以结合在PS上。此外,该多肽也可以是聚L-赖氨酸、聚鸟氨酸或多精氨酸分子,其长度和取代比可能有所不同[186, 187]。NPM的另一种变体是碱性但非氨基酸组成的聚合物,如聚乙氨基亚胺(PEI,见图10)。这些偶联物最初被提议用于口服抗菌应用(PDT用于牙周炎[188]),但后续研究表明PEI-ce6在小鼠模型中治疗烧伤感染非常有效[52]。 Hamblin等人[54]已申请基于功能化富勒烯抗菌PDT的PS化合物专利。在这项发明中,富勒烯分子、高富勒烯及其功能化衍生物被改造为具备将PDT应用于微生物细胞所需的多种性质。这通过控制碳纳米材料的疏水性、分子电荷和水溶性,优先针对微生物物种进行PDT测试。正电荷使富勒烯能够结合细胞,克服微生物的通透性障碍。阳离子富勒烯作为抗菌PS,表现优于广泛使用的抗菌PS 甲苯胺蓝O。因此,阳离子富勒烯在多种情况下的PDT中可能有显著应用,例如伤口、烧伤和黏膜的局部感染。 在另一项专利中,Hamblin和Tegos[189]描述了苯硫嗪和微生物多重耐药抑制剂用于使微生物细胞失活的方法。现在已经证明,苯噻嗪是微生物多药耐药泵(“MDR泵”)的底物。抑制剂(“MDR抑制剂”)使微生物MDR泵失活,增加了微生物可保留的苯噻嗪量,从而提高苯噻嗪在照射光激活时的效能。 Biel [190] 申请了一项专利,利用聚苯乙烯(如亚甲蓝或甲苯蓝)与表面活性剂化合物(如多粘菌素B或SDS)结合溶液,用于治疗细菌或真菌感染或癌细胞根除的PDT。表面活性剂用于影响靶细胞膜的通透性。可治疗的病原体包括金黄色葡萄球菌、白色念珠菌、大肠杆菌、肠球菌、链球菌、透珠菌、流感嗜血杆菌和梭菌。 Hamblin和Foley[58]申请了一组苯二氮卓(A)苯甲嗪染料的硫化物类似物,具有有效的抗菌性苯甲酸碱。特别是当铅质为硒(EtNBSe)时,活性最大化(见图10)。 Albrecht等人[191]揭示了一种方法,通过将由红血素B组成的复合物以PS形式加入生物表面的治疗区域,从而在预定时间内与治疗区的细菌结合,从而破坏患者治疗区域的细菌。 并将预选波长的辐射照射到处理区域以激活PS,从而刺激光动力学反应以消灭细菌。 在另一项专利中,Albrecht等人[192]描述了脂质体制剂以提高抗菌PDT疗效的应用。这些制剂包括疏水性卟啉PS、单糖,以及一种或多种合成磷脂,这些磷脂在储存中表现稳定,尤其通过冷冻干燥和重组过程。 Van Der Haas等人[193]申请了一种制备适用于抗菌PDT的四元化卟啉衍生物的方法专利。另一项专利[194]描述了使用这些以Sylsens B为代表的卟啉(见图10)用于进行包括烧伤在内的真菌皮肤感染PDT的应用。 Roncucci等人申请了一系列邻苯二硫素衍生物的专利[57],见图。(10)具有光敏特性和高水溶解性,适用于光动力学治疗细菌感染,特别是革兰氏阴性菌引起的感染。 在另一项专利中,Bommer 和 Jori [195] 提出使用带有多达四个正电荷的外围取代基,且至少有一个疏水尾巴(含6至22个碳),起源于一个或多个带电位点的卟啉。进行了体外测试以评估这些化合物的光敏化效能。观察到在1微米卟啉存在下,照射15分钟后实现了4对格10单位的大肠杆菌灭活。 Love及其同事[53]申请了一种利用含有阳离子基团的卟啉衍生物进行选择性光动力失活目标微生物细胞的方法专利,且对宿主细胞的损伤最小。据称,XF73图中典型的卟啉衍生物。(10).可作为选择性PDT剂使用,即选择性杀死微生物,也可与传统抗生素联合使用。 首篇描述PDT治疗烧伤感染的论文由Orenstein等人[56]提出。这些研究人员使用氘性啧啉-赫明复合物作为感染多药耐药金黄色葡萄球菌株烧伤伤口PDT的药物。通过将上述卟啉联合应用于豚鼠感染的烧伤伤口,是显著减少污染金黄色葡萄球菌的有效方法。在将卟啉混合物滴入焦痂或注射后,观察到超过99%的可存活细菌减少,这种效果可持续长达24小时。 Lambrechts等人[55]使用由中单苯基三(N-甲基-4-吡啶)-卟啉介导的PDT治疗已确立生物发光金黄色葡萄球菌感染的小鼠烧伤伤口。在细菌生长一天后,通过在伤口加入25% DMSO/500微米PS(聚压性物质溶液)进行PDT治疗,随后用红光照射,并用灵敏相机定期拍摄小鼠以检测生物发光。在PTMPP存在下,轻剂量210 J cm²后,超过98%的细菌被消灭。然而,观察到细菌重新生长。 Dai 等人[52]利用小鼠模型评估了PDT对鲍曼氏烧伤感染的疗效。在剃毛小鼠背部制造烧伤效果,方法是使用两块加热的黄铜块(95°C),块块与小鼠皮肤接触时间为10秒。生物发光的鲍曼氏菌接种于烧伤部位,随后加入聚乙烯胺-氯e6共轭物,并在660±15纳米处用非相干红光照射。 图11展示了感染A. baumannii并用PDT治疗的代表性小鼠烧伤在感染后30分钟、仅用PS治疗的小鼠烧伤(暗对照)和仅用光治疗(光照对照)小鼠烧伤的细菌发光PDT剂量-反应。在240 J/cm²红光照射(40分钟照射时间,照射强度为100 mW/cm²)后,PDT使小鼠烧伤引起的细菌发光约减少3对数单位,而同期,暗照和光照对照仅观察到细菌发光适度降低。感染后30分钟进行PDT时,通过发光成像分析量化了超过3-log10的A. baumannii失活。当PDT在感染后24小时(即感染完全建立时)进行时,实现了超过1 log10的灭活。 感染A. baumannii并用PDT治疗的代表性小鼠烧伤在感染后30分钟出现细菌发光(上排)、仅用PS治疗的小鼠烧伤(暗对照,中排)以及仅用光治疗的小鼠烧伤(对照,下排)。在240 J/cm²红光照射(40分钟照射时间,照射强度为100 mW/cm²)后,PDT使小鼠烧伤引起的细菌发光约减少3对数单位,而同期,暗照和光照对照仅观察到细菌发光适度降低。 PDT未延缓包曼病感染烧伤的伤口愈合。 壳豆是一种具有特定结构和性质的多阳离子聚合物。几千聚糖分子含有超过5000个氨基葡萄糖单位,该物质通过碱性脱乙酰化(NaOH,40–50%)从虾和蟹壳几丁质(一种N-乙酰氨基葡萄糖聚合物)中商业化获得,如图所示。(12)。具有不同分子量、脱乙酰化度(DD)及进一步分子衍生模式的千寿豆制剂因其潜在的有益生物学特性而备受关注。千草蛋白的特性使其能够快速凝固血液,最近已获得美国批准用于绷带及其他止血剂。壳聚糖是一种含有多种碱性氨基的高分子,因此在酸性pH下具有整体阳离子电荷。与许多多阳离子聚合物一样,由于外膜不稳定和质膜渗透,它具有显著的抗菌作用[196]。 用热氢氧化钠处理几丁质(聚N-乙酰氨基葡萄糖)部分水解酰胺键,形成甲氨基聚氨基糖(聚氨基葡萄糖)。 已有大量专利申请或颁发,涉及各种千寿司制剂作为抗菌烧伤治疗或敷料的制备和使用。在这篇评论中,我们只能举出其中的几个例子。 最早的专利之一是Sparkes等人[197]提出的,他描述了一种由明胶和几千聚糖混合物组成的伤口敷料。Yura及其同事申请了[198]一种功能性千合聚衍生物专利,该衍生物由千反桑组成,包含光反应官能团、两性基团(例如多氧乙烷烷醚)和糖胺聚糖,且该衍生物可溶于中性介质,具自交联能力,并能作为伤口敷料使用。Baker和Wiesmann [199]为壳桑或壳桑衍生物(如甲醛氨酸精氨酸和壳桑酸胺)申请了专利,这些化合物对细菌病原体(如耐药性金黄色葡萄球菌MRSA)具有杀菌活性。Scherr申请了[200]一种含有千胞散的泡沫凝胶专利,可以叠加在合适的背衬上用作伤口敷料,或者直接涂抹于伤口,通过千寿司的作用产生止血作用。泡沫壳聚糖凝胶的成分可以降低伤口中微生物感染的风险。穆扎雷利申请了专利[201]一种甲基吡咯里冚酮壳反桑衍生物,可用作伤口敷料,形式包括冻干材料、粉末、薄膜、非织造物、绷带、胶带等。 Alsarra [202] 研究了壳脂凝胶的配方以改善大鼠烧伤伤口愈合。测试了高分子量壳豆,容量为2,000,000兆瓦电,密度为92%,中分子量壳农,功率为750,000兆瓦电,密度为75%,密度为75%,低分子量壳农,密度为63%。研究显示,高分子量且高脱乙酰化程度的壳农样本对烧伤愈合效果最佳。 青柳等人[203]描述了一种由千寿膜和盐酸米诺环素组成的千寿三敷料。使用DD为67%的千寿司,分别为83%和96%(mol/mol)。多种配方被应用于大鼠烧伤。DD为83%的千松生搭配2毫克盐酸米诺环素效果显著。 Boucard等人[204]开发了一种双层物理水凝胶,由壳聚糖和水组成。第一层是刚性保护凝胶,确保良好的机械性能和气体交换,第二层柔软柔韧,使材料能顺应伤口的几何形状,确保表面接触良好。使用了DD含量2.6%、分子量540,000 g/mol的壳反桑。这种材料在猪背三度烧伤后进行了皮肤再生测试。结果显示,壳胞材料耐受良好,并促进良好的组织再生。 Cardenas [205] 通过在醋酸千米聚溶液中添加多种添加剂,如:甘油、油酸和亚油酸,按不同比例制成了几种类型的壳聚复合薄膜。他们使用了醋酸千寿片,这些薄膜是用低分子量和高分子量的虾壳千生(MWt = 68,000 g/mol,MWt = 232,000 g/mol)制备的。这些薄膜根据添加剂和/或混合物的不同,表现出不同的物理性质。向复合材料添加甘油可以提升薄膜的弹性。体外测试使用几胞桑复合溶液对金黄色葡萄球菌、绿血单胞菌和鲍曼单胞菌进行检测,显示分子量影响壳菌复合膜的杀菌特性以及对革兰氏阳性和阴性菌的影响。复合膜在烧伤、溃疡和损伤患者中的医学应用被研究,含甘油的胶片相较于无甘油的胶片,附着力较佳。7至10天后,皮肤恢复效果极佳。 Ribeiro等人[59]提出了一种用于烧伤伤口愈合的壳聚糖水凝胶。通过制备该水凝胶,4%的几胞聚溶液(w/w)被分散在2%(v/v)中的乳酸中。体外研究表明,几胞烷水凝胶能够促进细胞的粘附和增殖,并且对细胞无毒性。体内研究利用大鼠烧伤模型显示,甲烷水凝胶能刺激伤口愈合,且基于用几千散-水凝胶治疗烧伤无肉芽肿性炎症反应且器官无病理异常的证据,具有局部和全身的生物相容性。 Sezer等人[206]开发了含有胡科伊丹的壳藻膜,并研究其在兔子烧伤治疗中的有效性。富科丹是一种常见于海藻的硫酸多糖,具有显著的凝胶促进、整合素表达增强和肝素活性。研究发现含有富科伊丹的壳干聚膜可诱导显著的伤口收缩,加速伤口闭合和愈合过程。作者还制备了富科伊丹-几胞聚氢凝胶,并研究其在兔子皮肤烧伤中的治疗效果[60]。与含有褐炭的几百寿胶片得出类似结果。 Damour等人[207]报告了临床使用由胶原蛋白-GAG--壳胞组成的皮底物,在严重烧伤早期切除后立即移植,然后用自身网格状自体移植物或自身培养表皮进行表皮化。真皮基质通过附着于下方组织,替代切除的真皮层,促进纤维血管生长。与同质移植物相比,这种真皮底物始终可用,可储存,且免受微生物传播。 Peh 等人[208]研究了使用两种不同溶剂——醋酸(甲烷-AA)和乳酸(甲烷-LA)制备的甲壳聚胶片的机械、生物粘附强度和水汽渗透率。两部电影的性质与商业片《Omiderm®》的特性进行了比较。此外,还进行了生物学研究,以调查这些薄膜的皮肤刺激和全身毒性。研究发现,这三种制备在机械和生物粘结强度特性上存在显著差异。千千万-LA比千万-AA更柔软、有弹性、有韧性和生物粘性。此外,甲烷-LA无过敏且无毒。因此,作者认为甲烷-LA更适合用于伤口愈合和皮肤烧伤的管理。 Dai等人[61]研究了最初作为止血敷料开发的冻干甲壳虫醋酸酯绷带(HemCon™)的使用。他们将敷料敷用于感染生物发光金黄色杆菌和奇迹红斑小鼠的三度烧伤处, 图(13)。显示了从P. aeruginosa感染后第0天到第3天连续的生物发光图像,分别是未治疗的烧伤、银敷料处理的烧伤和甲壳酸盐处理烧伤。未治疗烧伤中,细菌从第0天到第3天大约增殖了1000倍;而在银敷料和几胞聚乙酸酯绷带处理烧伤中,第1天因敷料立即熄灭光线,生物发光信号均有所下降。银敷料烧伤在第2天和第3天(相较于第1天)信号明显增强,而甲壳烷-醋酸酯烧伤则未见。第3天银处理烧伤的嵌入图是在移除死老鼠银敷料后拍摄的,显示敷料下方细菌繁殖旺盛。 从P. aeruginosa感染后第0天到第3天的连续生物发光图像,分别是未治疗的烧伤(上排)、银敷料处理烧伤(中排)和醋酸氯桑处理烧伤(下排)。 在金银杆菌感染中,使用醋酸千食肠敷料治疗的小鼠存活率为73.3%,而使用纳米晶银敷料治疗的小鼠存活率为27.3%(p = 0.0055),未治疗小鼠为13.3%(p < 0.0002)。奇幻杆菌感染的可比存活率分别为66.7%、62.5%和23.1%。定量生物发光信号显示,醋酸千寿绷带有效控制烧伤中细菌生长,并防止全身性败血症的发展,血液培养显示了这一点。 “抗菌肽”一词指的是存在于所有生命类别中、同时具有抗菌和抗真菌活性的大量肽。研究表明,它们能杀死革兰氏阴性和革兰氏阳性菌(包括对传统抗生素耐药的菌株)、分枝杆菌(包括结核分枝杆菌)、包膜病毒以及真菌。除了作为内源性抗生素外,抗菌肽还参与免疫的多个方面(炎症、伤口修复和适应性免疫系统的调控)。因此,与大多数传统抗生素不同,抗菌肽还能通过作为免疫调节剂增强免疫力。抗菌肽根据其一级和二级结构、抗菌潜能、对宿主细胞的影响以及表达调控被划分为异质性组别。大多数抗菌肽体积较小(12–50个氨基酸),具有由Arg和Lys残基提供的正电荷,具有能够与细菌膜相互作用的两亲性结构[209]。无花果。(14)。展示了抗菌肽对微生物膜的亲和力高于宿主细胞膜,因此优先裂解致病微生物的抗菌肽所获得的选择性。 抗菌肽表现出的选择性示意图,使其能够裂解微生物细胞膜,但无法溶解宿主细胞的膜。 这些天然抗菌剂是人体自然防御机制的一部分,任何这些化合物的流失显然会导致抵抗感染的能力下降,并易患败血症。有许多报告指出抗菌肽与不同皮肤疾病有关。抗菌肽的过度表达会导致对皮肤感染的保护增强,如银屑病和酒渣鼻患者;炎症性皮肤病——但很少导致超级感染。在其他皮肤疾病中,例如寻常性痤疮患者,炎症或感染皮肤区域常发现AMPs水平升高,表明这些肽在保护感染中起作用。此外,抗菌肽水平下降与烧伤相关,导致的败血症往往致命[210]。这一观察暗示抗菌肽在烧伤治疗中可能具有治疗作用。 defensins是一类阳离子抗菌肽,具有杀菌、杀真菌和抗病毒活性[211–213]。它们是由非淋巴细胞分泌的非特异性化学防御系统的一部分[62]。当它们释放到细胞外环境时,直接通过攻击微生物膜发挥抗菌活性,并有助于对被吞噬的微生物进行非氧杀死。此外,防御蛋白在先天免疫与适应性免疫系统之间的相互作用中起到中介作用[214]。已鉴定出两种人类β-defensin。人类B-defensin-1已在泌尿生殖器、胃肠道和肺部上皮中被检测到,最近则在皮肤中被检测到[215–217]。研究表明,烧伤时抗菌肽(AMPs)水平下降,主要是与防御素相关的[210],这有助于感染及随后的败血症。防御素的减少还可能改变T淋巴细胞和B淋巴细胞、中性粒细胞、巨噬细胞和补体的功能,从而促进烧伤相关全身性炎症反应的病理生理[218]。防御素具有广泛的抗菌特性、化学抗性以及缺乏抗原性,表明它们也可能作为感染预防和治疗的局部或全身性药物[62]。它们也可能在防止烧伤伤口感染方面发挥保护作用,因为这些肽的表达改变可能促进微生物局部过度生长。 部分合成抗菌肽相较天然防御素具有更高的效力、更高的特异性和更低的毒性。这些肽对高溶质含量具有较强的抵抗力,且表现出比天然肽更强的抗生素活性。其中一种合成肽是Demegel D2A21(Demegen公司,宾夕法尼亚州匹兹堡),已获得专利[219, 220]。该肽在体外对多种病原体的研究中显示出显著前景[221]。Chalekson等人[63]展示了D2A21在感染烧伤模型中提升生存和恢复的效果。随后,他们比较了该肽在感染伤口模型中与传统创伤治疗——银磺胺茼和磺胺酰胺——对生存的影响,报告D2A21的活性显著优于对照组和标准治疗[222]。 组蛋白是真核细胞中与DNA结合最丰富的蛋白质,也是已知进化上最保守的蛋白质之一。它们是分子量在11至20 kDa之间的小型碱性蛋白,含有较高比例的正带电氨基酸(约20%),如赖氨酸和精氨酸。真核细胞主要包含五种组蛋白类型:组蛋白连接蛋白H1和核心组蛋白H2A、H2B、H3和H4。组蛋白H1.2属于组蛋白H1家族[223],具有潜在的先天抗菌防御作用[224]。研究表明,组蛋白H1.2在体外和体内(感染大鼠烧伤模型)对多种烧伤感染病原体具有良好活性[64]。H1.2的重组生产获得了专利[225]。 Cecropin B及相关肽类已被申请为抗菌剂专利[226]。研究了cecropin B对小鼠伤口P. aeruginosa感染的抗菌作用,观察到施用cecropin B可降低小鼠死亡率[65]。HB-107是一种由cecropin B衍生的全肽段,缺乏抗菌活性,但在无菌全层切除损伤小鼠模型中,与炒化肽或载体对照组相比,第13天的伤口闭合改善率可达64%。这一效应与接受当前接受治疗后的效果相当。对HB-107治疗伤口的组织学评估显示角蛋白细胞增生和白细胞浸润增加,较对照组更明显。在Ghiselli等人使用的两种不同大鼠模型中,[227],β-内酰胺甚至会增加血浆内毒素和TNF-α水平,而与头孢素B联合治疗被证明是最有效的治疗方法,生存率最高(超过90%),抗菌活性最高且最强效。 这种源自人类中性粒细胞序列的重组肽被申请为抗菌剂专利[228]。早期使用rBPI21治疗可能有效减轻因肠源内毒素易位引起的多器官损伤,尤其发生热损伤时。这可能与组织脂多糖结合蛋白和 CD14 基因表达通过 rBPI21 下调效应有关。目前,正在进行一项临床试验,探讨rBPI21在烧伤患者中的治疗效果[66]。 水化素,或称阳离子类固醇抗生素(CSA),是一种合成生产的小分子化合物,由固醇骨架和氨基酸及其他化学基团结合组成。它们在一系列专利中被描述[229–231]。虽然CSA的作用机制也存在于抗微生物肽中,这些肽是人体先天免疫系统的一部分,但它们避免了许多作为药物使用的困难。其中几种衍生物对多种细菌表现出抗菌活性。虽然某些形式的神经菌素对革兰氏阴性菌和革兰氏阳性菌都有效,但它们通常对革兰氏阳性菌更具效力。细胞生具有与磷脂形成复合物的特殊特性。因此,心腺素是一类具有多种特性的药物,使其适合用作抗感染剂[67]。 一项专利[232]描述了家蝇(Musca domic)蛹天然AMP,作为一种具有广谱抗生素活性且对小鼠血红细胞无溶血活性的产品,其特征为高耐高温、耐酸性和耐碱性及良好稳定性。 另一项专利涉及抗菌肽的多聚体形式,例如具有抗菌活性的defensin肽,这些肽可制成用于医疗器械等涂层的抗菌复合物。该发明还涉及利用这些多聚肽形式抑制和/或减少包括烧伤在内的感染中微生物的生长[233]。 抗菌博利辛肽最初从牛胸腺中提取,并已在专利中描述[234]。其他专利也已颁发,涉及来自组蛋白[235]、蚕血淋巴[236]、肝素结合蛋白或人类中性粒细胞弹性蛋白[237–239]的抗菌肽。 外用氯己定已被研究多种配方用于对抗烧伤感染。Macmanus等[68]研究了两种致命烧伤伤口感染大鼠模型(20%被铜绿假单胞菌或神奇的Proteus感染)。它的表现与银磺胺嗪相当。Miller等人[69]在一项临床试验中比较了29名烧伤患者的不同浓度CHP,每人有两个类似的烧伤,可以分别治疗。一个烧伤部位使用了四种不同浓度的CHP治疗,浓度从0.25%到2%,另一个部位则使用AgSD乳膏。CHP浓度与患者在模拟量表上的疼痛评分之间存在直接关系。0.25%的CHP乳膏在疼痛耐受度上最接近AgSD。已有多项专利涉及氯己定作为外用抗菌剂用于烧伤的应用[124, 240–242] 过氧化水基于通过盐水溶液电化学处理获得的次氯酸,并在美国专利中披露了[70]。理想情况下,超氧化水的pH值应在4到7之间,且氧化还原电位为>950毫伏。基于超氧化水的药物可以是液体或凝胶形式,可用于控制伤口或烧伤内的微生物数量,同时促进细胞增殖。 一项抗菌纳米乳剂在另一项美国专利中被披露[243]。它由一种油中水纳米乳剂组成,含有约5%体积的表面活性剂,如多氧乙基硅基单醇酸盐或多氧乙烯基烯酸单烯酸酯,含8%乙醇、64%油、1%乙基吡啶氯化物和蒸馏水。烧伤感染是其他被提出的应用。 FPQC(1-乙基-6-氟-1,4-二氢-4-氧-7-[1-啉傉-羧酸])[72]是一种外用药物,已在感染耐药铜绿假单胞菌株的烧伤小鼠中测试;接受FPQC局部治疗组的死亡率为0%,但磺胺二氮平银组死亡率为80%至100%,未治疗组死亡率为100%。烧伤大鼠也获得了类似结果。 酸化亚硝酸盐已被证明是多种皮肤病原体(包括白色念珠菌和金黄色葡萄球菌)的有效抗菌治疗[73]。它通过局部释放一氧化氮和其他活性氮中间体,形成一种被称为“氮应激”的现象[244]。 噬菌体疗法早在1920年代就已被发现[245],并被认为是治疗烧伤感染的一种可能方法。缺点被认为是噬菌体对特定细菌物种和菌株的专一性较窄。McVay 等人。[74] 发现三种噬菌体组合可显著降低热损伤感染P. aeruginosa小鼠的死亡率。Malik 和 Chhibber [246] 在一个小鼠模型中展示了从环境中分离出的肺炎克菌特异性噬菌体 KO1 具有保护作用,该模型由肺炎 K. 诱导的烧伤伤口感染。在用噬菌体制剂处理后,血液、腹膜灌洗和肺组织中的细菌负荷显著下降。一项专利授予了一种用于局部施用的抗金黄色假孔杆菌噬菌混合物[247]。 Ipaktchi等人[75]在感染P. aeruginosa的大鼠烧伤模型中局部应用p38线粒原蛋白激活促蛋白激酶(MAPK)抑制剂。他们发现,使用局部p38 MAPK抑制剂治疗的动物中,细菌伤口生长显著减弱。他们得出结论,过度消减烧伤伤口炎症信号可能防止真皮屏障的次级损伤,并减少机会性病原体的生长。 益生菌疗法利用“好”细菌来竞争,甚至在某些情况下主动杀死有害的致病菌。乳酸杆菌属会产生“抗生素”,即属于细菌素大类的抗菌蛋白。一项专利是关于一种与莫匹洛星联合使用的抗微生物药,作为局部抗菌剂[248]。在一项针对感染性二度和三度烧伤患者的临床试验中,一种由Lactobacillus plantarum组成的制剂相当于银磺胺嗪[76]。 蜂蜜长期以来被认为是天然存在的抗菌制剂[249]。它甚至被认为是烧伤的“民间疗法”[250]。其抗菌特性源于高渗透压和蜂蜜中葡萄糖氧化酶缓释产生的过氧化氢。只有当蜂蜜被伤口液体稀释时,它才会被激活。非过氧化物的抗菌活性源于甲基草醛和一种未明确的协同成分。在一项临床试验中[77],蜂蜜敷料与煮土豆皮敷料作为两组随机分配患者中新鲜部分厚度烧伤的覆盖物进行了比较。在50名使用蜂蜜治疗的患者中,90%的伤口在7天内变得无菌,而50名使用煮土豆皮敷料治疗的患者感染持续7天。用蜂蜜治疗的伤口中,15天内100%愈合,而用煮土豆皮敷料治疗的伤口只有50%。已有多项专利与蜂蜜作为抗菌敷料的局部涂抹相关[251–255]。 另一种替代烧伤疗法被提出使用植物精油[78]。Citricidal是一种葡萄柚种子提取物,作为抗菌香水成分获得了专利[256]。广藿香、茶树、天竺葵、薰衣草精油和Citicidal与金黄色葡萄球菌在体外烧伤敷料中进行了比较。柠檬油、天竺葵油和茶树油的组合效果最为显著。 湿性暴露烧伤软膏(MEBO)源自中医[257]。它含有芝麻油、β-植物甾醇、黄连素及其他少量植物成分。黄连素长期以来被认为是一种抗菌化合物[258]。MEBO已在临床试验中测试覆盖身体表面积不足40%的部分厚度热烧伤,并被证明与传统治疗相当[257]。 由于非洲大多数地区烧伤管理资源有限,传统非洲医学在许多方面都扮演着重要角色。Carica木瓜[80]目前在冈比亚作为烧伤敷料的主要成分,木瓜果肉被捣碎后每天涂抹于全层及感染烧伤处。它似乎能有效去除坏死组织,预防烧伤感染,并提供适合分层皮肤移植的颗粒状伤口。可能的作用机制包括蛋白酶壶叶酸和淀粉酶的活性,以及抗菌活性。 有大量多样化的外用抗菌药物已被批准、测试或提议用于预防和/或治疗烧伤感染。烧伤的特殊病理生理使其易感染多种病原体,经验表明局部治疗比传统全身性抗生素效果更好。此外,多重药物耐药性的不断扩散也凸显了有效且安全的局部治疗的重要性。这些局部抗菌方法的发展对大小生物技术公司来说都是肥沃的领域,这可从本综述涵盖的专利数量中看出。我们相信,局部抗菌剂领域的研究只会持续为先进社会生产更有效的高科技产品,以及为第三世界提供经济实惠且传统的制剂。 银作为抗菌剂具有多种作用机制,包括细菌细胞壁的渗透化和细胞内活性氧的生成。1. 引言
1.1. 历史
1.2. 烧伤的生理学
图1。燃烧的程度。
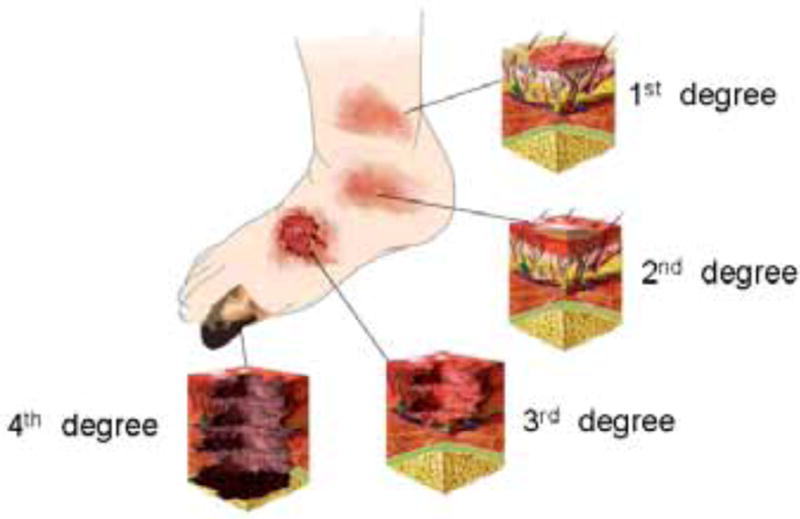
图2。伦德与布劳德图表。
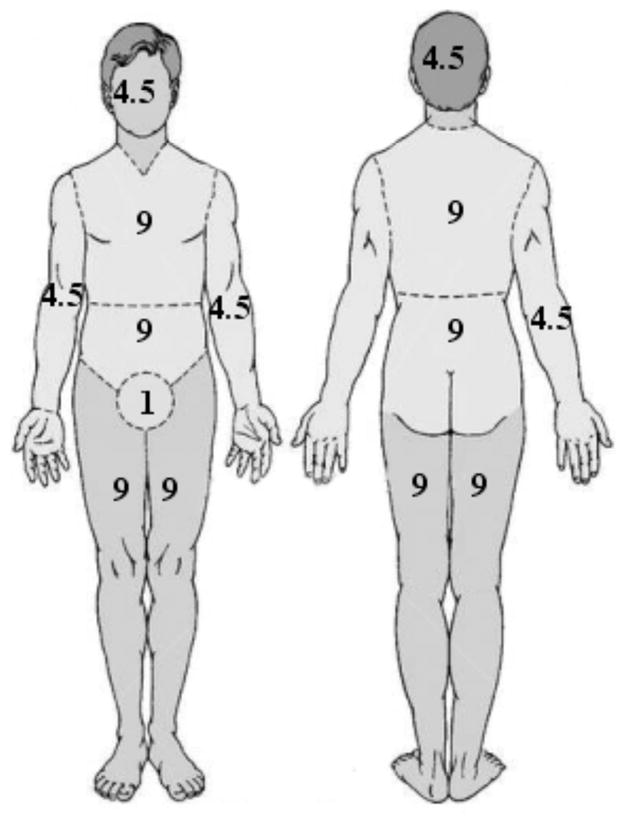
图3。烧伤后炎症信号导致免疫抑制。
1.3. 烧伤感染的微生物学
表1。
集团 物种 耐药性 革兰氏阳性菌 金黄色葡萄球菌 耐甲氧西林金黄色葡萄球菌 按定义 凝血酶阴性葡萄球菌 MRSE递增[7] 肠球菌属 万古霉素耐药肠球菌 按定义 革兰氏阴性菌 铜绿假单胞菌 高先天抗性 大肠杆菌 ESBL递增 肺炎克雷伯氏菌 ESBL递增 塞拉蒂亚·马尔塞森斯 递增 肠道杆菌属 ESBL递增 [8] Proteus属。 ESBL递增[9] 不动杆菌属 非常常见 Bacteroides 属 不常见 真菌 念珠菌属 氮氧化阻力和排流泵增加 [10] 曲霉属 递增 [11] 镰刀菌属 农业中常见 [12] Alternaria 属 农业中常见 ]13] 根瘤花属 抗性抗性 [14] Mucor属。 阿唑抗性 [15] 病毒 单纯疱疹病毒 巨细胞病毒 水痘带状疱疹病毒 图4。细胞壁结构。
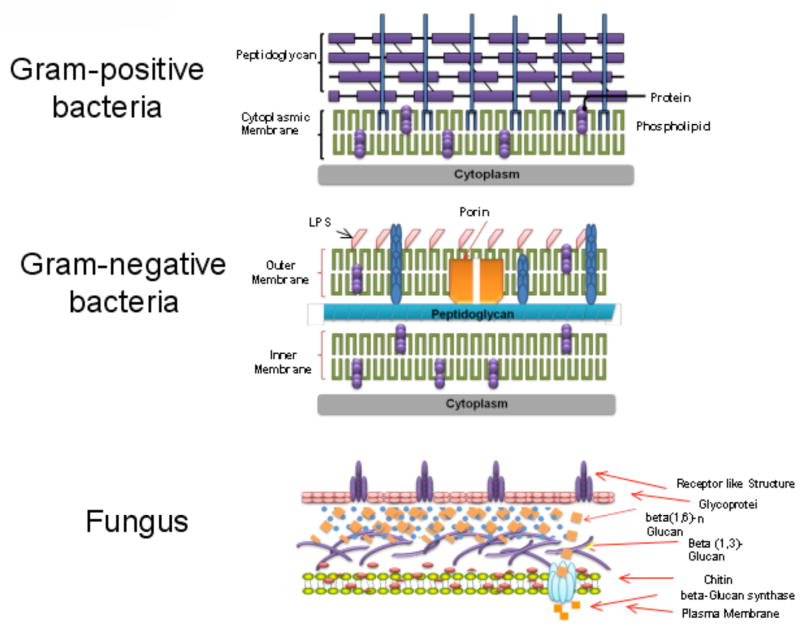
1.4. 烧伤感染的生理学
1.5. 抗生素耐药性
1.6. 局部抗菌剂
表2。
代理级 特定代理 应用 参考资料 皮肤替代品 十二叶 临床二度烧伤 [25] 跨细胞 临床二度烧伤 [26] 全维动物 临床二度烧伤 [27] 上皮 临床二度烧伤 [28] 埃皮加德 临床二度烧伤 [29] SYSpur-derm 临床二度烧伤 [30] 生物膜 临床二度烧伤 [31] 氙兽 临床二度烧伤 [32] 外用抗生素 醋酸马芬化物 临床二度/三度烧伤 [33] 杆菌素 临床二度/三度烧伤 [34] 穆匹罗星 临床二度/三度烧伤 [35] 新霉素 临床二度/三度烧伤 [36] 多菌素B 临床二度/三度烧伤 [37] 硝基呋喃酮 临床二度/三度烧伤 [38] 制糖素 临床上二度/三度烧伤,真菌感染 [35] 银牌 硝酸银 临床二度/三度烧伤 [39] 银磺胺茯 临床二度/三度烧伤 [40] 银泡沫(Contreet,Allevyn) 临床二度/三度烧伤 [41] 火焰铱 临床二度/三度烧伤 [42] 动衣7号 临床二度/三度烧伤 [43] 水质农业 临床二度/三度烧伤 [44] 银赛尔 临床二度/三度烧伤 [45] 银色羊膜( 临床二度/三度烧伤 [46] 碘 聚维酮碘 临床二度/三度烧伤 [47] 碘胺(碘吸附) 临床慢性伤口 [48] 脂质体碘,Repithel 临床二度烧伤 [49] 种族灭绝 口腔感染 [50] 光动力治疗 待命 小鼠伤口感染 [51] PEI-CE6 小鼠烧伤感染(A. baumannii) [52] XF73 体外皮肤感染 [53] BB6 体外小鼠伤口感染 [54] 西尔森斯B 金黄色葡萄球菌小鼠烧伤感染 [55] DP/hemin 豚鼠烧伤感染金黄色葡萄球菌 [56] 猫电脑 体外动物感染 [57] EtNBSe 体外受精 [58] 千民三 水凝胶 临床二度烧伤 [59] 电影 兔子二度烧伤 [60] 绷带 鼠烧伤感染(鼠性脓疱病,变形虫) [61] 抗菌肽 防御者 体外受精 [62] 德梅格尔 铜绿假单胞菌感染的老鼠烧伤 [63] 直结H1.2 铜绿假单胞菌感染的老鼠烧伤 [64] Cecropin B 铜杆菌感染小鼠伤口 [65] rBPI 临床试验二度烧伤 [66] 细胞蛋白 体外受精 [67] 其他 氯己定(LM Miller) 感染性老鼠烧伤,临床试验 [ 68,69] 过氧化水 体外受精 [70] BCTP纳米乳剂 体外受精 [71] FPQC 老鼠烧伤,长假单胞菌 [72] 酸化亚硝酸盐 体外受精 [73] 噬菌体疗法 老鼠烧伤,长假单胞菌 [74] p38MAPK抑制剂 鼠烧,假单胞菌 [75] 益生菌,乳酸杆菌 临床试验,二级,三级 [76] 亲爱的 二级临床试验 [77] 精油 体外受精 [78] MEBO 二级临床试验 [79] 木瓜 临床试验,二级,三级 [80] 2. 烧伤感染的动物模型
2.1. 梅森-沃克燃烧模型
2.2. 斯蒂里茨-持枪点火模型
2.3. 其他燃烧模型
图5。三度烧伤感染小鼠模型。

2.4. 感染的生物发光成像
图6。利用生物发光成像处理转基因细菌和真菌在烧伤感染中的应用。
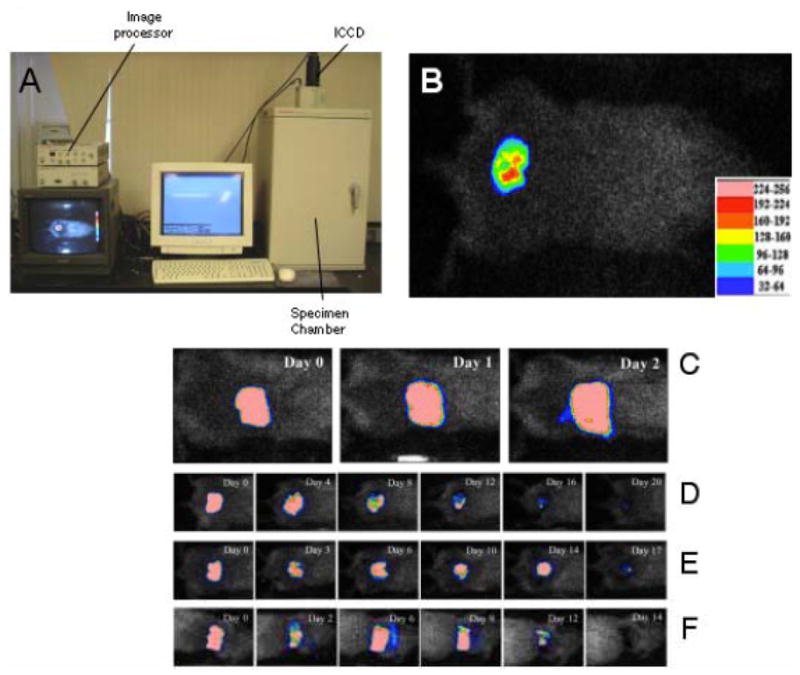
3. 皮肤替代品
3.1. 多翼部
3.2. 全貌者
3.3. 上层
3.4. Epigard 和 SYSpur-Derm
3.5. 生物膜
3.6. 移植与皮肤移植
3.7. 异皮动物与异皮动物
3.8. 其他皮肤替代品
4. 外用抗生素
图7。用于烧伤局部抗菌治疗的抗生素化学结构。
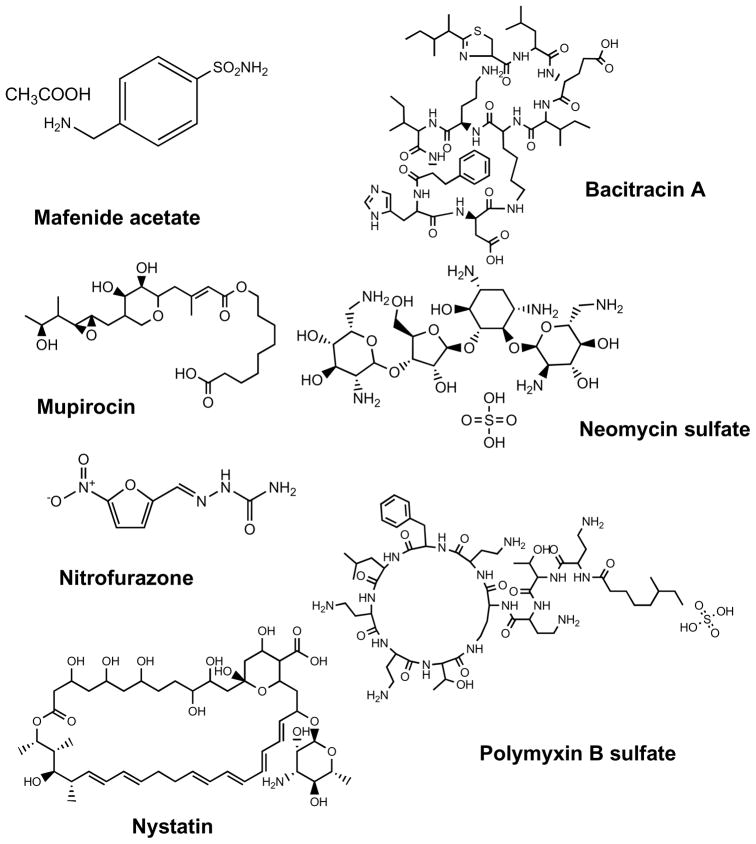
4.1. 醋酸马非奈德
4.2. 巴西拉辛
4.3. 莫匹洛星
4.4. 新孢素
4.5. 多粘菌素B
4.6. 硝基呋喃酮
4.7. 制糖素
5. 外用银制剂
5.1. 硝酸银
5.2. 银磺胺肼
5.3. 硝酸铈-固态硬盘
5.4. 持续白银释放系统
5.5. 银浸生物材料
6. 碘制剂
6.1. 聚维酮-碘
6.2. 脂质体碘(Repithel)
6.3. 卡德克聚碘(碘吸附)
6.4. 其他碘制剂
7. 光动力治疗
图9。抗菌光动力疗法的概念。
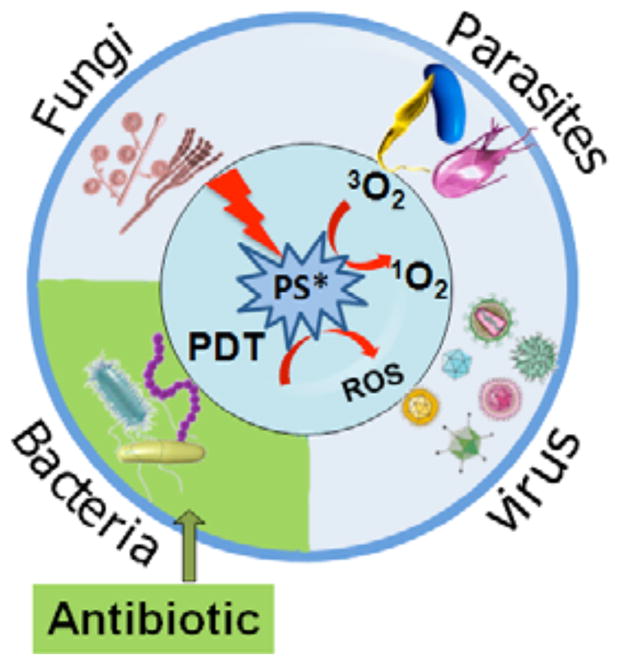
图10。抗菌应用中光敏剂的化学结构。
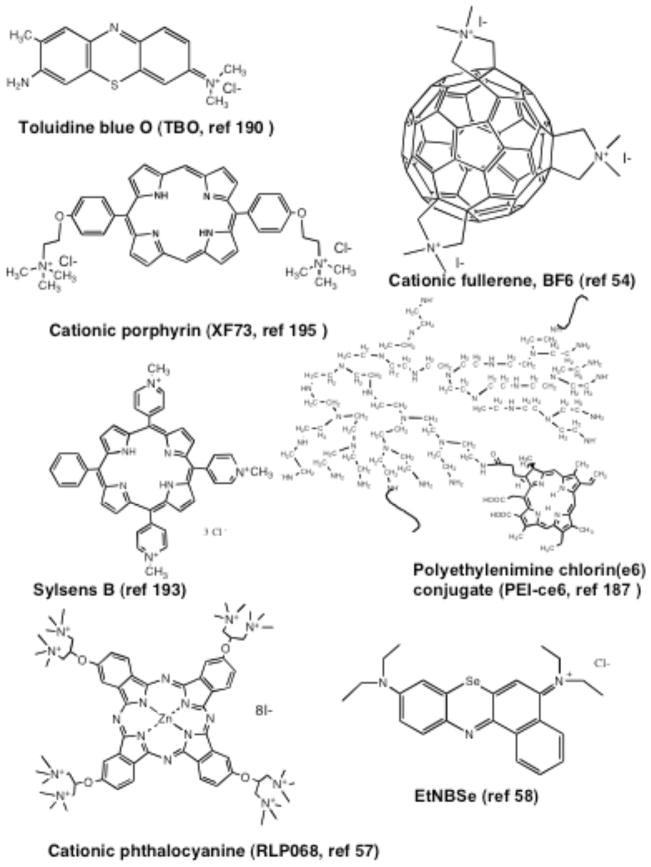
7.1. 抗菌PDT专利
7.2. 烧伤感染的PDT
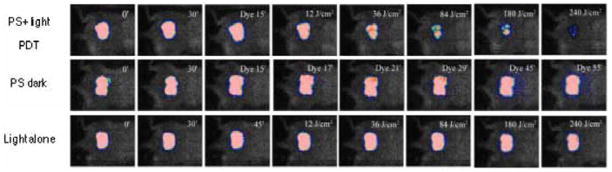
图11。使用PDT治疗由生物发光的鲍曼单胞菌引起的小鼠烧伤感染。
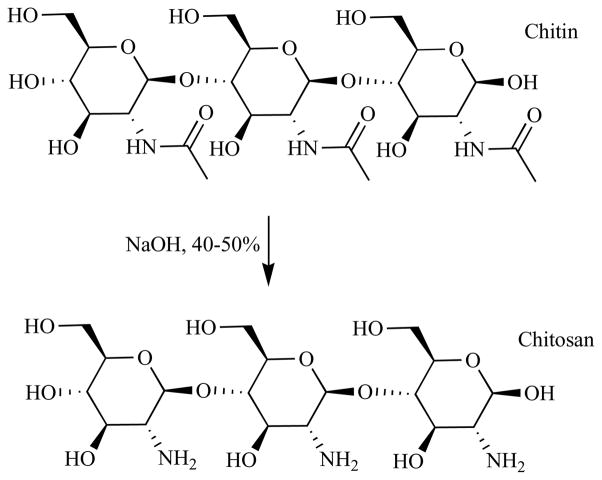
8. 千多三岛的准备
图12。几丁质和壳藻的化学结构。
8.1. 抗菌千食制剂专利
8.2. 烧伤感染的千寿司
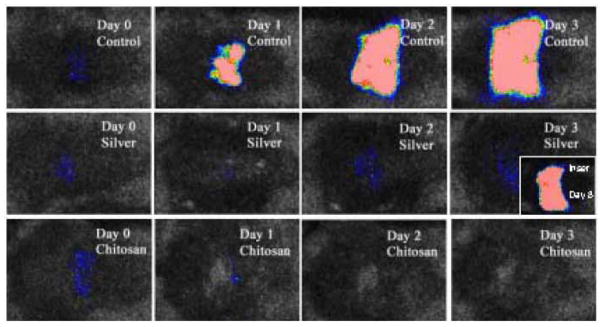
图13。使用醋酸千寿绷带治疗小鼠烧伤感染。
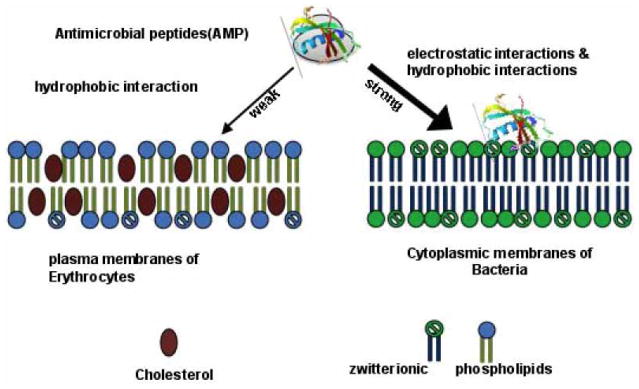
9. 抗菌肽
图14。抗菌肽的抗菌作用。
9.1. 防御者
9.2. 德梅格尔
9.3. 组石H1.2
9.4. 天宫素B
9.5. 重组杀菌/通透性增强蛋白(rBPI21)
9.6. 角毛蛋白
9.7. 其他AMP
10. 杂项局部抗菌药物
11. 当前与未来发展
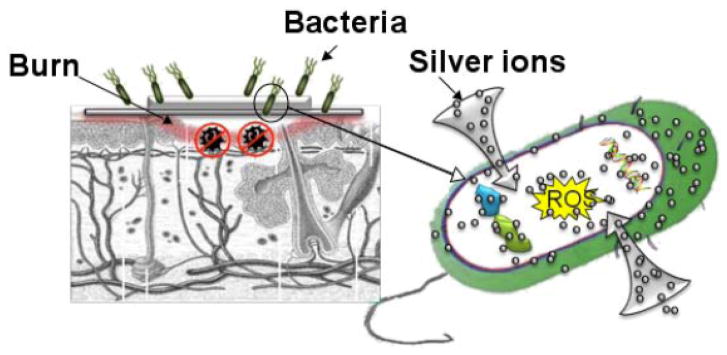
图8。银作为烧伤局部抗菌剂的使用。